SACHVERSTÄNDIGENBÜRO

Ausbildungsplattform (Tier-Notruf)
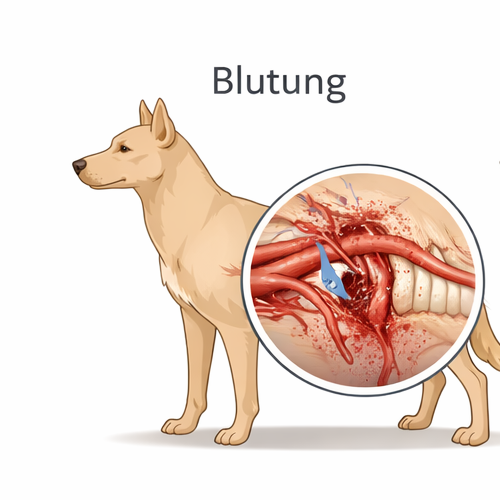
Ziel: in Sekunden Blutung kontrollieren und Transportpriorität festlegen.
Kapitel 4 fokussiert Trauma, Blutungen und Wundmanagement – zentrale Kernaufgaben der präklinischen Tierrettung. In traumatischen Situationen entscheidet nicht die ästhetisch perfekte Verbandtechnik, sondern die konsequente Prioritätensetzung: lebensbedrohliche Blutungen stoppen, Oxygenierung sichern, Hypothermie vermeiden und den Patienten ohne Zeitverlust einer definitiven Versorgung zuführen. Präklinisches Handeln ist dabei zeitkritische Schadensbegrenzung. Ziel ist Stabilisierung, nicht vollständige chirurgische Versorgung.
Blutungen werden nach Mechanismus, Lokalisation und Gefährdungspotenzial unterschieden. Arterielle Blutungen sind typischerweise hellrot und pulsierend; sie können in sehr kurzer Zeit zu kritischem Volumenverlust führen. Venöse Blutungen erscheinen meist dunkelrot und kontinuierlich fließend; sie sind ebenfalls gefährlich, insbesondere bei großen Gefäßen oder ausgedehnten Weichteilverletzungen. Kapilläre Blutungen sicken flächig und sind isoliert selten lebensbedrohlich, treten jedoch häufig begleitend auf. Entscheidend ist nicht allein das sichtbare Blut, sondern die Gesamtbeurteilung von Perfusion und Kreislaufstatus.
Ein zentrales Ausbildungsziel ist das frühzeitige Erkennen innerer Blutungen. Thorax-, Abdomen- oder Beckenverletzungen können erhebliche Blutverluste verursachen, ohne dass äußerlich viel sichtbar ist. Klinische Warnzeichen sind Tachykardie, verlängerte Kapillarfüllzeit, blasse oder graue Schleimhäute, kalte Extremitäten, schwacher peripherer Puls sowie Veränderungen der mentalen Lage. Besonders tückisch sind kompensierte Stadien: Der Blutdruck kann initial im Referenzbereich liegen, während die Mikrozirkulation bereits insuffizient ist. Deshalb wird die Verlaufsbeobachtung betont – wiederholte Befunderhebung im Minutenabstand, Trenddokumentation und konsequente Reevaluation.
Die Trauma-Physiologie verknüpft Blutverlust, Hypothermie und Gerinnungsstörung zu einem selbstverstärkenden Kreislauf. Schon eine moderate Auskühlung beeinträchtigt enzymatische Gerinnungsprozesse. Blutverlust reduziert die Gewebeperfusion und begünstigt Azidose, welche wiederum die Koagulation weiter verschlechtert. Diese Dynamik – häufig als traumatische Trias beschrieben – kann eine Blutungsspirale auslösen. Präklinisch lässt sich diese Entwicklung beeinflussen: sofortiger Wärmeschutz, konsequente Blutungskontrolle und Vermeidung unnötiger Verzögerungen sind essenziell.
Die effektivste Maßnahme bei äußerer Blutung ist in der Regel der direkte Druck. Ein korrekt angelegter Druckverband kann massive Blutverluste verhindern. Bei tiefen Wunden kann eine gezielte Tamponade sinnvoll sein. Tourniquets sind nur bei klarer Indikation und entsprechender Qualifikation anzuwenden, da sie Gewebeschäden verursachen können. Der didaktische Fokus liegt auf „low risk, high benefit“: direkter Druck, adäquater Verband, Wärmeschutz, rascher Transport. Invasive Schritte bleiben spezialisierten Teams vorbehalten.
Eine Besonderheit in der Tierrettung ist das Verhalten des Patienten. Angst, Schmerz und Abwehrreaktionen können Blutungen verstärken, etwa durch Schütteln, Laufen oder panisches Zerren am Verband. Bewegung erhöht den Blutdruck lokal und kann Koagel destabilisieren. Deshalb sind sichere Fixierung, stressarme Annäherung und klare Teamrollen integraler Bestandteil des medizinischen Konzeptes. Eine Person hält konstanten Druck, eine bereitet Verbandmaterial vor, eine überwacht Vitalparameter und koordiniert Kommunikation und Transport.
Fallbeispiel: Ein Hund nach Bissverletzung präsentiert eine scheinbar begrenzte Wunde. Innerhalb von 10–15 Minuten entwickelt er Tachykardie, die Schleimhäute werden blass, die Kapillarfüllzeit verlängert sich. Gleichzeitig blutet die Wunde stärker, weil das Tier unruhig ist und sich schüttelt. Die korrekte präklinische Reaktion besteht in sofortigem direktem Druck, Anlage eines stabilen Druckverbandes, konsequentem Wärmeschutz, ruhiger Lagerung und rascher Transportentscheidung mit Voranmeldung. Die Dynamik lässt an fortschreitenden Volumenverlust oder zusätzliche innere Blutung denken.
In der Praxis ist die sichere Lagerung häufig genauso relevant wie das verwendete Verbandmaterial. Jede unnötige Bewegung kann eine Blutung erneut eröffnen oder ein Hämatom vergrößern. Stressreduktion wirkt hier unmittelbar medizinisch: Ein ruhiger Patient blutet weniger, toleriert Verbände besser und bleibt hämodynamisch stabiler. Daher ist Deeskalation kein „weicher“ Faktor, sondern ein Teil der physiologischen Stabilisierung.
Blutungskontrolle ist kein einmaliger Akt. Verbände können durchweichen, Hämatome können wachsen, und ein zunächst stabiler Patient kann sich im Verlauf verschlechtern. Jede Maßnahme muss mit einer Reevaluation verknüpft werden: Ist die Blutung gestoppt? Verbessert sich die Perfusion? Bleibt die Kapillarfüllzeit stabil? Ändert sich die mentale Lage? Diese wiederholte Bewertung ist entscheidend, um ein Abrutschen in einen dekompensierten Schock rechtzeitig zu erkennen.
Zeitkritik ist ein leitendes Prinzip. Definitive Versorgung – chirurgische Exploration, Blutprodukte, Bildgebung – erfolgt in der Klinik. Präklinisch wird Stabilität gewonnen und Zeitverlust vermieden. Längere Versuche, komplexe Wunden vor Ort vollständig zu versorgen, sind kontraproduktiv, wenn sie den Transport verzögern. Die Qualität präklinischer Arbeit bemisst sich daran, wie effizient Stabilisierung und Übergabe organisiert werden.
Eine strukturierte Übergabe umfasst mehr als die Beschreibung der sichtbaren Verletzung. Sie beinhaltet Blutungsart, Lokalisation, angewandte Verbandtechnik, Zeitpunkt der Maßnahmen, Trend der Vitalparameter sowie vermutete Risiken (z. B. mögliche innere Blutung). Diese Informationen ermöglichen der Zielklinik eine zielgerichtete Vorbereitung – Operationssaal, Blutprodukte, Bildgebung.
Die häufigsten Fehler im präklinischen Blutungsmanagement sind unzureichender direkter Druck, instabile Verbandtechnik, verspätetes Erkennen innerer Blutungen und fehlender Wärmeschutz. Ebenso problematisch ist das Unterschätzen kompensierter Stadien. Ein scheinbar stabiler Patient kann rasch dekompensieren, wenn Volumenverlust fortschreitet oder Stress zunimmt.
Didaktisch wird trainiert, unter Stress handlungsfähig zu bleiben: klare Reihenfolge, klare Kommunikation, klare Dokumentation. Trauma-Management ist Teamarbeit. Gerinnung, Temperatur und Perfusion bilden ein funktionelles System – wird ein Faktor vernachlässigt, destabilisiert sich das Gesamtsystem. Konsequente Priorisierung, konsequente Reevaluation und konsequenter Transport sind die tragenden Säulen präklinischer Traumaversorgung.
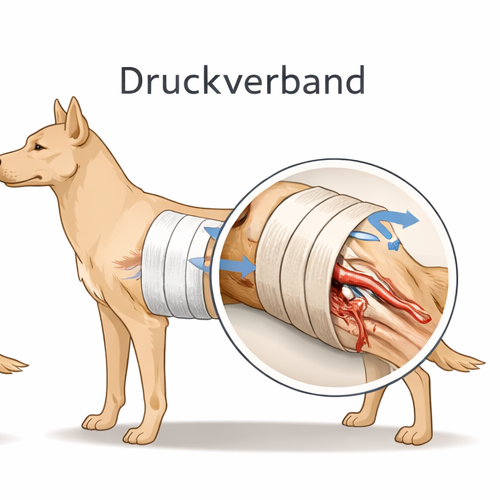
Die effektivste präklinische Maßnahme zur Blutungskontrolle ist direkter Druck. Diese Maßnahme wirkt mechanisch unmittelbar auf die verletzten Gefäße, reduziert den Blutfluss und ermöglicht die Bildung eines stabilen Gerinnsels. Obwohl das Prinzip einfach erscheint, entstehen in der Praxis genau hier die häufigsten Fehler: zu geringer Druck, zu kurze Applikationsdauer, wiederholtes „Nachsehen“ mit Ablösen bereits gebildeter Koagel oder instabile Verbandtechnik. Ziel der Ausbildung ist daher ein standardisiertes, reproduzierbares Handlungsprotokoll.
Das Vorgehen folgt einer klaren Sequenz. Erstens: Identifikation der Blutungsquelle, sofern dies ohne relevanten Zeitverlust möglich ist. Zweitens: Applikation eines saugfähigen Materials direkt auf die Wunde – Kompresse, Verbandpäckchen oder notfalls sauberes Textil. Drittens: konsequenter, konstanter Druck. Dabei reicht es nicht, das Material lediglich aufzulegen; es muss aktiv komprimiert werden. Der Druck wird über mehrere Minuten gehalten, ohne den Verband anzuheben. Viertens: Nach deutlicher Reduktion der Blutung wird ein stabiler Druckverband aufgebaut.
Ein Druckverband besteht aus einem Druckkörper direkt über der Wunde (z. B. gerollte Kompresse), darüber mehrere straffe Fixierlagen. Die Spannung muss ausreichend sein, um den Druck zu erhalten, darf jedoch die distale Durchblutung nicht kompromittieren. Deshalb gehört die Kontrolle der peripheren Perfusion zur Standardmaßnahme: Temperatur der Gliedmaße, Schleimhautfarbe, Kapillarfüllzeit und – sofern tastbar – peripherer Puls distal der Bandage. Eine kalte, blasse oder pulslos erscheinende Extremität erfordert eine unmittelbare Anpassung des Verbandes.
Ein zentrales Prinzip lautet: Ein Verband wird nicht routinemäßig geöffnet, um „nachzuschauen“. Das Ablösen zerstört fragile Koagel und führt häufig zu erneuter Blutung. Wenn der Verband durchblutet erscheint, wird zusätzliches Material aufgesetzt und erneut komprimiert, anstatt die gesamte Konstruktion zu entfernen. Diese Technik reduziert Re-Traumatisierung und erhält die Gerinnungsstabilität.
Bei Tierpatienten spielt die Ruhigstellung eine besondere Rolle. Bewegung kann Druck reduzieren, Verbände verschieben und Blutungen reaktivieren. Angst, Schmerz und Abwehrreaktionen verstärken diesen Effekt. Stressreduktion ist daher kein Nebenfaktor, sondern ein direkter medizinischer Wirkmechanismus. Ruhige Annäherung, klare Kommunikation mit dem Halter, sichere Fixierung sowie geeignete Tragehilfen oder Decken sind integraler Bestandteil der Blutungskontrolle.
Fallbeispiel: Ein Hund mit Risswunde an der Vordergliedmaße zeigt eine venöse Blutung. Der Halter möchte die Wunde wiederholt betrachten und „reinigen“. Die korrekte präklinische Strategie besteht darin, den konstanten Druck zu erklären und aufrechtzuerhalten, einen stabilen Druckverband anzulegen, die distale Durchblutung zu kontrollieren, Wärmeschutz zu gewährleisten und umgehend den Transport zu organisieren. Das wiederholte Öffnen würde die Blutung verstärken und wertvolle Zeit verlieren.
Bei massiven Blutungen oder Verdacht auf Verletzung größerer Gefäße ist Zeit ein entscheidender Faktor. Präklinisch wird nicht perfektioniert, sondern stabilisiert. Definitive chirurgische Versorgung, Gefäßrekonstruktion oder Transfusion erfolgen in der Klinik. In fortgeschrittenen Ausbildungssettings wird auch die Wundtamponade bei tiefen Verletzungen thematisiert. Diese Technik erfordert jedoch Materialkenntnis, klare Indikation und Kompetenzgrenzen. Patientensicherheit steht stets im Vordergrund.
Gerinnung, Temperatur und Perfusion bilden ein funktionelles System. Hypothermie verschlechtert enzymatische Gerinnungsprozesse. Blutverlust reduziert die Gewebeperfusion und begünstigt metabolische Azidose, welche die Koagulation weiter beeinträchtigt. Jede präklinische Maßnahme muss daher auch den Wärmeerhalt berücksichtigen. Wärmeschutz ist kein Komfortfaktor, sondern ein Bestandteil der Blutungs- und Schockkontrolle.
Blutungskontrolle ist kein einmaliger Akt, sondern ein dynamischer Prozess. Verbände können durchweichen, Hämatome können expandieren, und ein zunächst kompensierter Patient kann dekompensieren. Jede Maßnahme wird mit Reevaluation verknüpft: Ist die Blutung gestoppt? Verbessert sich die Perfusion? Bleiben Vitalparameter stabil? Ist der Transport priorisiert? Diese systematische Rückkopplung verhindert Fehleinschätzungen.
Die häufigsten Fehler sind unzureichender Druck, instabile Verbandtechnik, verspätetes Erkennen innerer Blutungen und fehlender Wärmeschutz. Ebenso problematisch ist das Ignorieren von Trends. Eine stabile Schleimhautfarbe zu Beginn schließt eine spätere Verschlechterung nicht aus. Dokumentation von Zeitpunkten, Maßnahmen und Reaktionen ist daher Teil der Patientensicherheit.
Eine strukturierte Übergabe an die Klinik umfasst Blutungsart (arteriell/venös/unklar), Lokalisation, angewandte Technik (direkter Druck, Druckverband, Tamponade), Zeitpunkt der Maßnahmen, Trend der Vitalparameter sowie vermutete Risiken wie mögliche innere Blutung. Diese Informationen ermöglichen der Klinik eine zielgerichtete Vorbereitung von OP, Bildgebung oder Blutprodukten.
Zusammenfassend folgt das präklinische Blutungsmanagement dem Prinzip „low risk, high benefit“: direkter Druck, stabiler Druckverband, Wärmeschutz und rascher Transport. Invasive Maßnahmen erfolgen nur bei entsprechender Qualifikation. Strukturierte Reihenfolge, klare Kommunikation und konsequente Reevaluation sichern die Wirksamkeit – und verhindern, dass vermeidbare Fehler den Verlauf verschlechtern.
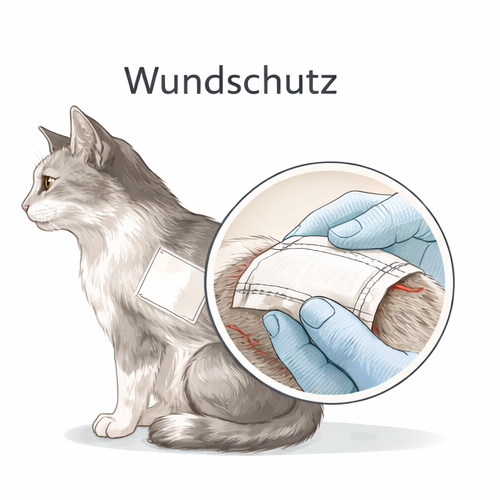
Wundmanagement in der präklinischen Tierrettung verfolgt grundlegend andere Ziele als die chirurgische Versorgung in der Klinik. Während dort eine definitive Wundtoilette, ein strukturiertes Debridement, bildgebende Diagnostik, Drainagenanlage, Gefäßrekonstruktion und antibiotische Strategien umgesetzt werden können, liegt der präklinische Schwerpunkt auf Schadensbegrenzung. Die Leitprinzipien lauten: Blutung kontrollieren, Gewebe schützen, weitere Kontamination minimieren, Schmerzen und Stress reduzieren sowie Komplikationen während des Transports verhindern. Präklinische Maßnahmen sind temporär, aber entscheidend für Prognose und Überlebenswahrscheinlichkeit.
Die Prioritäten sind klar hierarchisiert. Zuerst steht die Blutungskontrolle. Eine ästhetische Reinigung ist nachrangig, wenn aktiver Blutverlust besteht. Hygiene ist wichtig, darf jedoch niemals die hämodynamische Stabilität gefährden. Bei starker Blutung wird nicht gewaschen oder intensiv gespült. Stattdessen erfolgt sterile oder zumindest saubere Abdeckung und konsequenter Druck. Bei moderater Blutung kann eine grobe, oberflächliche Reinigung mit sauberem Material sinnvoll sein, jedoch ohne aggressives Schrubben, tiefes Spülen oder Manipulation in unkontrolliertem Umfeld. Jede unnötige Manipulation erhöht das Infektionsrisiko und kann Koagel destabilisieren.
Ein zentraler Ausbildungsinhalt ist der korrekte Umgang mit Fremdkörpern. Stecken Äste, Metallteile oder andere Objekte in einer Wunde, werden diese in der Regel nicht entfernt. Fremdkörper können verletzte Gefäße tamponieren und so Blutungen temporär begrenzen. Eine unkontrollierte Entfernung kann massive Blutungen auslösen. Stattdessen wird der Fremdkörper stabilisiert: Polsterung ringsum, vorsichtige Fixierung zur Minimierung von Bewegung, sterile Abdeckung und sofortige Transportpriorisierung. Die definitive Entfernung erfolgt unter kontrollierten Bedingungen im Operationssaal.
Offene Bauch- oder Thoraxverletzungen gelten als absolute zeitkritische Notfälle. Hier steht die sterile Abdeckung, Vermeidung weiterer Kontamination, konsequenter Wärmeschutz und schnellstmöglicher Transport im Vordergrund. Bei eventrierten Organen wird nicht versucht, diese aggressiv zu repositionieren. Stattdessen erfolgt feuchte sterile Abdeckung, Schutz vor Austrocknung und mechanischer Belastung. Hypothermie ist bei solchen Verletzungen besonders wahrscheinlich und verschlechtert Gerinnung sowie Prognose erheblich.
Wunden sind häufig nicht isoliert, sondern mit Frakturen, Gefäß- oder Nervenverletzungen kombiniert. Daher wird die neurovaskuläre Kontrolle gelehrt. Dazu gehören Prüfung der Sensibilität (Schmerzreaktion), Beurteilung der Motorik, sofern möglich, Palpation distaler Pulse, Kontrolle von Temperatur und Hautfarbe distal der Verletzung. Veränderungen können auf Gefäßkompression oder -verletzung hinweisen und beeinflussen die Dringlichkeit. Eine Immobilisation der betroffenen Extremität reduziert Schmerzen, schützt Gefäße und verhindert sekundäre Gewebeschäden.
Praxisbeispiel: Ein Hund mit großer Schnittwunde am Unterschenkel, sichtbare Sehnen. Die präklinisch korrekte Handlung besteht nicht in kosmetischer Reinigung, sondern in sauberer Abdeckung, effektiver Blutungskontrolle, Immobilisation der Extremität, konsequentem Wärmeschutz und priorisiertem Transport in eine chirurgisch ausgestattete Klinik. Der Halter wird sachlich über das Infektionsrisiko, mögliche Sehnenschädigung und die Notwendigkeit operativer Versorgung informiert. Klare Kommunikation reduziert Panik und fördert Kooperation.
Ein weiterer wesentlicher Faktor ist Stress. Tierpatienten reagieren auf Schmerz, Angst und ungewohnte Umgebung mit Abwehr, Fluchtversuch oder aggressivem Verhalten. Diese Reaktionen können Wunden verschlimmern, Blutungen verstärken und Verbandtechniken destabilisieren. Stressreduktion ist daher ein medizinischer Wirkfaktor. Ruhige Umgebung, strukturierte Teamarbeit, gegebenenfalls Maulkorbentscheidung nach Risikoabwägung und sichere Lagerung erhöhen die Effektivität aller Maßnahmen.
Die Übergabe an die Klinik ist strukturiert und präzise. Sie umfasst: Zeitpunkt der Verletzung, Blutungsverlauf, angewandte Verbandtechnik, neurovaskuläre Befunde, Schmerzverhalten, Art möglicher Kontamination (Erde, Meerwasser, Bissverletzung), bereits eingetretene Veränderungen sowie Trends der Vitalparameter. Diese Informationen ermöglichen der Klinik eine gezielte Vorbereitung von OP, Bildgebung und Antibiotikastrategie.
Ein Verband ist nur dann funktionell, wenn er den Transport übersteht, die Durchblutung nicht kompromittiert und die Wunde zuverlässig schützt. Zu lockere Verbände verlieren ihre Wirkung, zu straffe Verbände gefährden die Perfusion. Deshalb gehört die Reevaluation zur Standardroutine: Ist die Blutung weiterhin kontrolliert? Bleibt die distale Extremität warm und durchblutet? Zeigt der Patient neue Schockzeichen? Jede Maßnahme ist an eine erneute Beurteilung gekoppelt.
Die Ausbildung betont, dass Blutungskontrolle und Wundschutz keine einmaligen Schritte sind. Verbände können durchweichen, Hämatome expandieren, Schockzeichen können sich verzögert manifestieren. Gerinnung, Temperatur und Perfusion bilden ein interdependentes System. Hypothermie verschlechtert Koagulation, Blutverlust reduziert Perfusion, Azidose behindert die Gerinnung weiter. Wärmeschutz ist daher integraler Bestandteil des Wundmanagements.
Der Fokus liegt konsequent auf „low risk, high benefit“: direkter Druck, stabiler Verband, Fremdkörperstabilisierung, Immobilisation, Wärmeschutz und rascher Transport. Invasive Schritte erfolgen nur bei entsprechender Qualifikation und klarer Indikation. Präklinische Perfektion ist nicht das Ziel; funktionelle Stabilität ist es. Zeitmanagement wird zur medizinischen Intervention – jede unnötige Verzögerung verschlechtert die Prognose.
Typische Fehler sind unzureichender Druck, instabile Verbandtechnik, verspätetes Erkennen innerer Blutungen, fehlender Wärmeschutz und übermäßige Manipulation aus „Reinigungsdrang“. Ebenso problematisch ist das Unterschätzen kompensierter Stadien. Ein zunächst stabil wirkender Patient kann sich rasch verschlechtern. Daher werden klare Reihenfolge, klare Kommunikation und klare Dokumentation trainiert, um auch unter Stress handlungsfähig zu bleiben.
Zusammenfassend bedeutet präklinisches Wundmanagement Schutz statt Perfektion. Ziel ist es, weitere Schäden zu verhindern, physiologische Stabilität zu erhalten und die Brücke zur definitiven chirurgischen Versorgung zu schlagen. Konsequente Priorisierung, strukturierte Reevaluation und präzise Übergabe sind die tragenden Säulen einer sicheren und effektiven Versorgung.
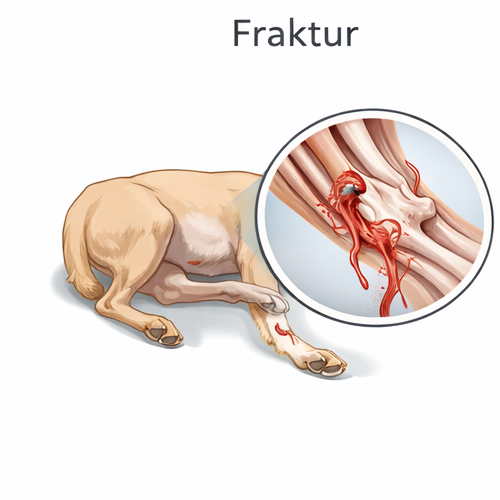
Immobilisation im traumatischen Einsatz ist keine isolierte orthopädische Technik, sondern ein integraler Bestandteil des präklinischen Gesamtkonzeptes aus Schockmanagement, Schmerzreduktion, Blutungskontrolle und Komplikationsprophylaxe. Jede unkontrollierte Bewegung einer Fraktur kann Gefäße erneut eröffnen, bestehende Blutungen verstärken, umliegende Weichteile zerreißen oder Nerven irreversibel schädigen. Gleichzeitig führt Schmerz zu einer ausgeprägten Stressreaktion mit Tachykardie, erhöhtem Sauerstoffverbrauch und gesteigerter Katecholaminausschüttung. Diese physiologische Antwort kann bei bereits kompromittierter Perfusion den Übergang vom kompensierten in den dekompensierten Schock beschleunigen. Präklinische Immobilisation bedeutet daher: sekundäre Traumafolgen verhindern und physiologische Stabilität sichern.
Das Ziel ist ausdrücklich nicht die definitive Frakturbehandlung. Reposition, Osteosynthese oder chirurgische Exploration gehören in die Klinik. Präklinisch wird funktionell stabilisiert. Die Grundprinzipien lauten: möglichst wenig Manipulation, achsengerechte Lagerung, ausreichende Polsterung, sichere Fixierung und kontinuierliche Reevaluation. Jede Maßnahme muss in das ABCDE-Schema eingebettet bleiben. Eine Extremitätenfehlstellung darf niemals dazu führen, dass Atemweg, Atmung oder Kreislauf vernachlässigt werden. Die Priorität bleibt die Vitalfunktion.
Frakturen werden präklinisch als Arbeitsdiagnose anhand klinischer Zeichen vermutet. Dazu zählen ausgeprägte Schmerzreaktion, Fehlstellung, pathologische Beweglichkeit, rasche Schwellung, Hämatombildung, Belastungsverweigerung oder Verkürzung einer Extremität. Krepitation kann auftreten, wird jedoch nicht provoziert. Das absichtliche Bewegen einer vermuteten Fraktur zur „Bestätigung“ ist kontraindiziert, da dadurch Gefäße oder Nerven verletzt werden können. Die Ausbildung legt Wert auf visuelle und funktionelle Beurteilung ohne aggressive Palpation.
Wirbelsäulenverletzungen müssen bei jedem relevanten Trauma mitgedacht werden. Verkehrsunfälle, Stürze aus Höhe, Tritte oder massive Gewalteinwirkung bergen das Risiko instabiler Läsionen. Neurologische Auffälligkeiten wie Ataxie, Paresen, Paralyse, fehlende Tiefenschmerzreaktion oder Inkontinenz erhöhen die Wahrscheinlichkeit spinaler Beteiligung. Präklinisch wird keine forciert gerade Lagerung erzwungen, wenn dadurch Atmung beeinträchtigt würde. Vielmehr wird das Tier in der Position stabilisiert, in der es effektiv ventilieren kann, während Rotations- und Beugebewegungen minimiert werden. Trageboards, stabile Unterlagen oder straff gespannte Decken dienen der achsengerechten Umlagerung.
Bei Extremitätenfrakturen ist eine improvisierte Schienung häufig ausreichend. Geeignet sind formstabile Materialien wie Kunststoffschienen, Holzleisten, dicke Kartonstücke oder zusammengerollte Magazine. Entscheidend ist großzügige Polsterung, um Drucknekrosen zu vermeiden. Die Schiene sollte das betroffene Segment sowie mindestens ein angrenzendes Gelenk einschließen. Zu enge Fixierungen sind zu vermeiden, da sie die distale Perfusion gefährden können. Ziel ist Stabilität, nicht maximale Kompression.
Die Kontrolle der distalen Durchblutung ist obligatorisch. Temperatur, Schleimhautfarbe, Kapillarfüllzeit der Zehen, Sensibilität und – sofern möglich – Palpation distaler Pulse geben Hinweise auf Perfusionsstatus. Zunehmende Schwellung, starke Schmerzprogression oder kühle, blasse distale Abschnitte können auf ein drohendes Kompartmentsyndrom oder eine Gefäßkompromittierung hinweisen. In solchen Fällen muss die Fixierung überprüft und gegebenenfalls gelockert werden. Reevaluation erfolgt unmittelbar nach Immobilisation und im Verlauf des Transports.
Immobilisation reduziert nicht nur Schmerzen, sondern beeinflusst auch die Blutungssituation. Bewegungsarme Fraktursegmente verursachen weniger mechanische Irritation verletzter Gefäße. Gleichzeitig verhindert eine stabile Lagerung weitere Weichteilschäden. Besonders bei Beckenfrakturen oder proximalen Femurverletzungen kann bereits durch ruhige, flächige Lagerung auf einer festen Unterlage eine relevante Stabilisierung erreicht werden.
Fallbeispiel: Ein mittelgroßer Hund nach Sturz aus dem zweiten Stock zeigt eine deutliche Fehlstellung der Hintergliedmaße, starke Schmerzreaktion und Tachykardie. Das Vorgehen beginnt mit ABCDE-Priorisierung. Atemweg und Atmung werden geprüft, offensichtliche Blutungen kontrolliert. Anschließend erfolgt eine achsengerechte Lagerung auf einer stabilen Unterlage. Die Hintergliedmaße wird großzügig gepolstert und funktionell fixiert. Distale Perfusion wird kontrolliert. Wärmeschutz wird eingeleitet, da Trauma und Immobilisation das Risiko der Hypothermie erhöhen. Der Transport erfolgt koordiniert mit mindestens zwei Helfern, um Rotationsbewegungen zu minimieren. Eine forcierte Reposition unterbleibt ausdrücklich.
Transport und Immobilisation sind untrennbar verbunden. Selbst die beste Schiene verliert ihren Nutzen, wenn der Patient ruckartig bewegt oder unsachgemäß angehoben wird. Die Ausbildung umfasst daher standardisierte Hebe- und Trage-Techniken. Kommandos werden klar und eindeutig gegeben. Eine Person koordiniert die Bewegung, um gleichzeitiges Heben sicherzustellen. Bei großen Hunden ist eine Dreipunkt- oder Vierpunkt-Technik sinnvoll, um Wirbelsäule und Extremitäten stabil zu halten.
Stressmanagement bleibt ein zentraler Faktor. Tierpatienten reagieren häufig mit Abwehr oder Panik. Diese Reaktionen können Immobilisationsmaßnahmen erschweren und Verletzungen verschlimmern. Ruhige Ansprache, strukturierte Teamarbeit und gegebenenfalls kontrollierte Fixierung reduzieren die physiologische Stressantwort. Stressreduktion ist medizinisch relevant, da sie Herzfrequenz, Sauerstoffverbrauch und Muskelspannung beeinflusst.
Die physiologische Trias aus Hypothermie, Azidose und Koagulopathie ist auch im Kontext der Immobilisation bedeutsam. Immobilisierte Tiere verlieren durch Schock und Umgebungseinflüsse rasch Körperwärme. Hypothermie verschlechtert die Gerinnungsfähigkeit und verschärft Blutungsverläufe. Daher ist Wärmeschutz integraler Bestandteil jeder Immobilisationsstrategie. Decken, isolierende Unterlagen und Minimierung von Nässe reduzieren Wärmeverlust effektiv.
Typische Fehler sind übermäßige Manipulation, Zeitverlust durch komplexe Improvisationen, fehlende Polsterung, zu straffe Fixierung oder mangelnde Reevaluation. Ebenso problematisch ist das Übersehen von Begleitverletzungen. Eine offensichtliche Fraktur darf nicht von inneren Blutungen, Thoraxtrauma oder abdominalen Verletzungen ablenken. Immobilisation ersetzt keine systematische Gesamtbeurteilung.
Die strukturierte Übergabe an die Klinik beinhaltet Unfallmechanismus, neurologische Auffälligkeiten, durchgeführte Immobilisationsmaßnahmen, distale Perfusionsbefunde, Schmerzverhalten sowie Trends der Vitalparameter. Diese Informationen ermöglichen der Klinik eine gezielte Vorbereitung auf Bildgebung, Analgesie, operative Stabilisierung oder intensivmedizinische Betreuung.
Zusammenfassend ist Immobilisation im präklinischen Setting ein funktionelles Instrument zur Reduktion sekundärer Schäden und zur Stabilisierung physiologischer Parameter. Sie verbindet Schmerzmanagement, Blutungskontrolle, Schockprävention und Transportorganisation. Präklinisch wird nicht perfektioniert, sondern stabilisiert. Klare Prioritäten, strukturierte Durchführung, konsequente Reevaluation und koordinierter Transport bilden die Grundlage für Patientensicherheit und optimales Outcome.
Trauma-Triage und Einsatzprioritäten bilden das operative Bindeglied zwischen den Modulen Atemwegsmanagement, respiratorische Stabilisierung, Schockbehandlung und Blutungskontrolle. In realen Einsatzsituationen liegen Verletzungen selten isoliert vor. Häufig handelt es sich um komplexe Mehrfachverletzungen, bei denen äußere, sichtbare Schäden mit inneren, zunächst verborgenen Problemen konkurrieren. Präklinische Triage bedeutet daher strukturierte Priorisierung unter Zeitdruck, Unsicherheit und oftmals emotionaler Dynamik am Einsatzort. Ziel ist nicht die abschließende Diagnose, sondern das frühzeitige Erkennen lebensbedrohlicher Muster, die sofortige Einleitung hochwirksamer Basismaßnahmen und der konsequente Zeitgewinn bis zur definitiven klinischen Versorgung.
Grundlage jeder Triage ist die stringente Anwendung der ABCDE-Logik. A (Airway) und B (Breathing) besitzen Vorrang vor jeder lokalen Wundversorgung. Ein Patient mit respiratorischer Insuffizienz kann nicht warten, bis ein Verband technisch perfekt angelegt ist. C (Circulation) integriert die Beurteilung von Pulsqualität, Herzfrequenz, Schleimhautfarbe, Kapillarfüllzeit, Extremitätentemperatur sowie das aktive Management äußerer Blutungen. Lebensbedrohliche Blutungen werden sofort mit direktem Druck kontrolliert – idealerweise parallel zur Atemwegs- und Atmungsbeurteilung. Die Ausbildung betont daher das Prinzip des simultanen Handelns: Denken in Prioritäten, Arbeiten im Team, parallele Maßnahmen statt sequenzieller Abarbeitung.
Entscheidungsregeln erleichtern die Einsatzpriorisierung. Zeichen schwerer Dyspnoe, manifeste Schocksymptome, Bewusstseinsstörungen, relevante Thorax- oder Abdomenverletzungen, Polytrauma, instabile Frakturen oder unstillbare Blutungen bedeuten höchste Transportdringlichkeit. In diesen Situationen werden ausschließlich Maßnahmen durchgeführt, die unmittelbar lebensrettend oder prognoserelevant sind: direkter Druck oder Druckverband, Sauerstoffgabe, achsengerechte Lagerung, Wärmeschutz. Jede weiterführende Intervention muss sich der Frage stellen: Verzögert sie den Transport ohne signifikanten Zusatznutzen?
Weniger kritische Verletzungen erlauben kurze, gezielte Interventionen vor Ort – beispielsweise die Stabilisierung eines Fremdkörpers, eine einfache Immobilisation oder strukturierte Dokumentation. Dennoch bleibt Zeit ein limitierender Faktor. Definitive chirurgische Blutstillung, Thoraxdrainage, Laparotomie, Bildgebung oder Transfusion sind ausschließlich klinische Maßnahmen. Präklinische Triage ist daher immer auch konsequentes Zeitmanagement.
Ein häufiges Praxisproblem ist die „Tunnel-Vision“. Dramatische äußere Wunden ziehen Aufmerksamkeit auf sich und können dazu führen, dass respiratorische oder neurologische Probleme übersehen werden. Die strukturierte Ganzkörperbeurteilung (E – Exposure/Environment) dient dazu, weitere Verletzungen systematisch zu identifizieren. Sie erfolgt jedoch erst nach Stabilisierung der vitalen Parameter. Exposure bedeutet vollständige Inspektion unter Beachtung von Wärmeschutz, um Hypothermie zu vermeiden, die Gerinnung und Prognose negativ beeinflusst.
Fallbeispiel 1: Ein Hund nach Verkehrsunfall zeigt eine stark blutende Extremitätenverletzung, gleichzeitig flache Atmung und blasse Schleimhäute. Die korrekte Strategie kombiniert Maßnahmen: sofortiger direkter Druck zur Blutungskontrolle, parallele Sauerstoffgabe, Wärmeschutz und unverzügliche Transportentscheidung. Eine isolierte Konzentration auf die Extremität würde das respiratorische Risiko unterschätzen. Parallelität und Priorisierung sind hier entscheidend.
Fallbeispiel 2: Eine Katze nach Sturz aus Höhe weist nur eine kleine Hautläsion auf, ist jedoch apathisch, tachykard und zeigt verlängerte Kapillarfüllzeit. Die Diskrepanz zwischen äußerem Befund und physiologischem Zustand weist auf mögliche innere Blutung oder thorakale Verletzung hin. In dieser Konstellation bestimmt das Gesamtbild – nicht die sichtbare Wunde – die Transportpriorität. Präklinisch wird stabilisiert und sofort transportiert.
Qualität in der Trauma-Triage zeigt sich in der Fähigkeit, zwischen sichtbarer Dramatik und physiologischer Relevanz zu unterscheiden. Wiederholte Reevaluation ist zentral: Verbessert sich die Perfusion nach Blutungskontrolle? Reduziert sich die Atemarbeit unter Sauerstoff? Bleibt der mentale Status stabil? Trendbeobachtung ersetzt die isolierte Einzelmessung.
Die pathophysiologische Trias aus Hypothermie, Azidose und Koagulopathie ist bei traumatisierten Tierpatienten von besonderer Bedeutung. Hypothermie verschlechtert die Gerinnung, Blutverlust reduziert die Gewebeperfusion, metabolische Azidose beeinträchtigt enzymatische Prozesse der Koagulationskaskade. Diese Faktoren verstärken sich gegenseitig. Konsequenter Wärmeschutz, effektive Blutungskontrolle und schneller Transport unterbrechen diese Spirale präklinisch am effektivsten.
Stress und Schmerz wirken zusätzlich destabilisiertend. Angstbedingte Abwehrreaktionen erhöhen Herzfrequenz, Sauerstoffbedarf und Muskelspannung. Stressreduktion ist daher medizinisch relevant. Ruhige Kommunikation, klare Aufgabenverteilung im Team und strukturierte Abläufe senken kognitive Belastung und erhöhen Patientensicherheit.
Die häufigsten Fehler in der Trauma-Triage sind falsche Priorisierung, übermäßige Detailmaßnahmen vor Ort, unzureichender Druck bei massiver Blutung, verspätetes Erkennen innerer Verletzungen, fehlender Wärmeschutz und mangelnde Reevaluation. Ebenso kritisch ist eine unstrukturierte Übergabe, die wichtige Informationen auslässt.
Die Übergabe an die Klinik ist integraler Bestandteil der Triage. Strukturierte Kommunikation – beispielsweise nach dem SBAR-Prinzip (Situation, Background, Assessment, Recommendation) – ermöglicht gezielte Ressourcenplanung. Übermittelt werden Unfallmechanismus, Zeitpunkte, Trends der Vitalparameter, vermutete Verletzungen, durchgeführte Maßnahmen und beobachtete Veränderungen. Eine präzise Voranmeldung kann OP-Vorbereitung, Transfusionsbereitschaft oder intensivmedizinische Kapazitäten optimieren.
Didaktisch wird betont, dass präklinische Tierrettung Stabilisierung und Zeitgewinn bedeutet – nicht definitive Chirurgie. Erfolg misst sich an klarer Prioritätensetzung, konsequenter Umsetzung von Basismaßnahmen, strukturierter Reevaluation und schneller Übergabe an eine geeignete Klinik. Trauma-Triage ist damit kein isolierter Schritt, sondern ein dynamischer Prozess, der kontinuierlich an die physiologische Entwicklung des Patienten angepasst wird.
Single-Choice: pro Frage eine richtige Antwort. Bestehensgrenze: 70%.
Ziel: Blutung korrekt priorisieren (Druck → Verbandstrategie → Wärmeschutz/Transport).
Ausbildungsplattform (Tier-Notruf)

Ziel: Atemwegssituation in Sekunden einschätzen und die nächste Priorität festlegen (O₂/Transport/Eskalation).
Kapitel 3 widmet sich dem respiratorischen Notfallmanagement in der präklinischen Tierrettung. Atemwegs- und Atmungsprobleme zählen zu den häufigsten und zugleich zeitkritischsten Notfallsituationen, weil Hypoxie innerhalb weniger Minuten zu Bewusstseinsverlust, Arrhythmien und Kreislaufkollaps führen kann. Die besondere Herausforderung liegt darin, dass „Atemnot“ kein eigenständiges Krankheitsbild ist, sondern die gemeinsame Endstrecke sehr unterschiedlicher Pathologien. Obere Atemwegsobstruktion, thorakale Restriktion, pulmonale Parenchymschädigung, kardiale Dekompensation, metabolische Azidose oder massive Schmerzen können das Atemmuster verändern. Präklinische Entscheidungslogik bedeutet daher, Atemnot nicht als isoliertes Symptom zu behandeln, sondern systematisch zu analysieren und entlang eines strukturierten Schemas zu priorisieren.
Im ABCDE-Ansatz steht zunächst A – Airway im Fokus. Die zentrale Frage lautet: Ist der Atemweg frei, durchgängig und geschützt? Bei Hund und Katze können Fremdkörper, Erbrochenes, Blut, Schwellungen, Tumoren, Larynxparalyse oder traumatische Veränderungen den oberen Atemweg beeinträchtigen. Gleichzeitig besteht bei reduzierter Bewusstseinslage ein erhöhtes Aspirationsrisiko. Präklinisch ist eine differenzierte Abwägung erforderlich: Eine vorsichtige visuelle Inspektion ist sinnvoll, sofern sie stressarm und ohne Manipulationsrisiko durchgeführt werden kann. Tiefe manuelle Eingriffe, unkontrollierte Maulöffnung oder aggressive Fixierung können jedoch Obstruktionen verschlimmern, Würgereflexe auslösen oder zu Bissverletzungen führen. Typische Zeichen einer oberen Atemwegsobstruktion sind inspiratorischer Stridor, Maulatmung, ausgeprägte Atemanstrengung, Speichelfluss, Panikreaktion und Zyanose. Ein entscheidender Lernpunkt ist hier die Stressphysiologie: Angst und Fixation steigern Sauerstoffverbrauch und Atemarbeit und können innerhalb kürzester Zeit zur Dekompensation führen. Stressreduktion ist somit kein „weicher Faktor“, sondern integraler Bestandteil der Atemwegssicherung.
Praktisch bedeutet das: ruhige Umgebung, gedämpfte Reize, kurze und zielgerichtete Handgriffe, Kopf- und Halsposition in gerader Achse, Vermeidung unnötiger Maulkorbanwendung und frühzeitige Sauerstoffgabe. Flow-by-Sauerstoff, Sauerstoffbox oder -maske werden so eingesetzt, dass zusätzliche Unruhe vermieden wird. Bei brachyzephalen Rassen ist besondere Vorsicht geboten, da anatomische Engstellen (verlängertes Gaumensegel, enge Nasenöffnungen, hypoplastische Trachea) eine rasche Verschlechterung begünstigen. Hier kann jede forcierte Manipulation den Kollaps verstärken. Ein klassisches Fallbeispiel ist der brachyzephale Hund nach Hitzeexposition mit massivem Hecheln, Stridor und Zyanose: Die korrekte Strategie besteht aus moderater Kühlung, sofortiger Sauerstoffgabe, Minimierung von Stress und raschem Transport in eine Klinik mit Sedierungs- und Intubationsmöglichkeit.
B – Breathing bewertet nicht nur die Atemfrequenz, sondern die Qualität und Effektivität der Ventilation. Entscheidend sind Atemtiefe, Thoraxexkursion, Einsatz der Bauchpresse, Atemgeräusche (Stridor, Giemen, Rasseln), Atemmuster (inspiratorisch vs. exspiratorisch erschwert), Zyanose und Zeichen von Erschöpfung. Thorakale Restriktionen wie Pneumothorax, Hämatothorax, Rippenserienfraktur oder Lungenkontusion verändern die Atemmechanik deutlich. Pulmonale Ursachen wie Ödeme, Pneumonien oder Aspiration beeinträchtigen den Gasaustausch auf alveolärer Ebene. Gleichzeitig können metabolische Störungen – etwa eine schwere Azidose – zu kompensatorischer Tachypnoe führen, ohne dass primär eine pulmonale Erkrankung vorliegt. Die präklinische Herausforderung besteht darin, Atemarbeit, Atemgeräusche und Perfusionszeichen gemeinsam zu interpretieren.
Ein zentrales didaktisches Prinzip lautet: Dyspnoe ist ein Alarmzeichen, keine Beobachtungsdiagnose. Unterschätzung von Atemnot gehört zu den häufigsten Fehlern in der Notfallpraxis. Tiere kompensieren oft lange, bevor sie abrupt dekompensieren. Zeichen wie zunehmende Atemanstrengung, verlängerte Inspiration, Nasenflügeln, Zyanose oder Erschöpfung weisen auf eine kritische Situation hin. Gleichzeitig darf Hyperventilation bei Stress nicht automatisch als „stabil“ interpretiert werden; sie kann ein Vorbote einer drohenden Erschöpfung sein. Jede respiratorische Intervention – Sauerstoffgabe, Lagerungsänderung, Wärmemanagement – muss durch eine unmittelbare Reevaluation begleitet werden: Wird die Atemarbeit geringer? Verbessert sich die Schleimhautfarbe? Sinkt die Unruhe?
Bei respiratorischen Notfällen gilt das Prinzip „Struktur vor Geschwindigkeit“ – dennoch entscheidet bei schwerer respiratorischer Insuffizienz jede Minute über die Prognose. Struktur bedeutet, dass trotz Zeitdruck das ABCDE-Schema nicht verlassen wird. Geschwindigkeit bedeutet, dass Prioritäten klar gesetzt werden: Atemweg sichern, Sauerstoff zuführen, Stress minimieren und Transport organisieren. Eine übermäßige Diagnostik vor Ort kann wertvolle Zeit kosten. Präklinische Maßnahmen überbrücken die kritische Phase; definitive Diagnostik (Röntgen, Ultraschall, Blutgasanalyse) und invasive Therapien erfolgen in der Klinik.
Ein weiterer didaktischer Schwerpunkt ist die Unterscheidung zwischen Hypoxie (unzureichende Sauerstoffversorgung), Hyperkapnie (erhöhtes CO₂ durch Hypoventilation) und Kreislaufdekompensation. Diese Prozesse sind eng miteinander verknüpft. Hypoxie führt zu Tachykardie und Unruhe, später zu Bewusstseinsminderung. Hyperkapnie kann Desorientierung und Atemmusterveränderungen verursachen. Kreislaufdekompensation wiederum verschlechtert die pulmonale Perfusion und damit den Gasaustausch. Präklinisch ist es daher essenziell, Atem- und Kreislaufparameter gemeinsam zu beurteilen und Trends zu dokumentieren.
Für die Ausbildung ist die Kopplung von Pathophysiologie und praktischer Umsetzung zentral. Theorie erklärt, warum Hypoxie in Minuten lebensbedrohlich wird; Praxis trainiert das Erkennen von Atemarbeit, den sicheren Umgang mit Sauerstoffsystemen und die stressarme Lagerung. Materialkunde – von Flow-by-Systemen über Sauerstoffmasken bis zur Box – ist ebenso relevant wie die Fähigkeit, ohne Technik klinische Zeichen korrekt zu interpretieren. Bei Hund und Katze ist die wiederholte klinische Beurteilung häufig aussagekräftiger als isolierte Messwerte, sofern sie konsequent erhoben und im Trend dokumentiert wird.
Fehlerquellen im respiratorischen Notfallmanagement sind wiederkehrend: Unterschätzung von Dyspnoe, unnötige Manipulation, fehlender Wärmeschutz, unstrukturierte Teamarbeit und verzögerter Transport. Hypothermie verschlechtert Kreislauf und Gerinnung und erhöht den Sauerstoffbedarf; Wärmemanagement ist daher integraler Bestandteil der respiratorischen Stabilisierung. Unnötige Manipulation kann Atemwegsobstruktionen verschlimmern oder Stress-induzierten Kollaps auslösen. Verzögerter Transport verhindert rechtzeitige definitive Therapie. Präklinische Qualität bedeutet daher, sich auf das Wesentliche zu konzentrieren und Ablenkungen zu vermeiden.
Teamorganisation spielt auch hier eine zentrale Rolle. Klare Aufgabenverteilung – beispielsweise Airway/O₂, Monitoring, Transportvorbereitung, Kommunikation – reduziert kognitive Last und verhindert Doppelarbeit. Closed-Loop-Kommunikation stellt sicher, dass Anweisungen verstanden und ausgeführt werden. Parallel wird eine knappe, aber konsistente Dokumentation geführt: Zeitpunkte, Befunde, Maßnahmen, Reaktionen. Die Übergabe an die Klinik umfasst Problem, klinische Einschätzung, durchgeführte Maßnahmen, Reaktion auf Interventionen und bestehende Risiken – nicht nur Einzelwerte. Dadurch kann die Zielklinik Intubationsbereitschaft, Bildgebung oder Intensivplatz vorbereiten.
Ein zentrales Lernprinzip lautet: Eine Intervention ist erst abgeschlossen, wenn ihre Wirkung überprüft wurde. Sauerstoffgabe ohne Reevaluation ist keine abgeschlossene Maßnahme. Lagerungsänderung ohne erneute Beurteilung der Atemarbeit bleibt unvollständig. Das zyklische Prüfen – Intervenieren – Prüfen schützt vor schleichender Verschlechterung. Besonders bei Tieren kann eine scheinbare Stabilität eine fragile Kompensation darstellen, die bei zusätzlichem Stress abrupt kollabiert.
Zusammenfassend verlangt das respiratorische Notfallmanagement in der präklinischen Tierrettung strukturiertes Denken, stressarme Handhabung, konsequente Sauerstoffstrategie und klare Kommunikation. Atemnot ist immer ein potenzieller Vorbote des Kreislaufversagens. Wer Pathophysiologie versteht, klinische Zeichen sicher erkennt und Interventionen systematisch reevaluieren kann, schafft die entscheidende Brücke zwischen Einsatzort und definitiver klinischer Versorgung.

Leitsatz: FiO₂-Gewinn darf nicht durch Stress „aufgefressen“ werden.
Unter B (Breathing) wird die Atmung als funktionelles System beurteilt: Wie effektiv ist der Gasaustausch, und wie hoch ist die Atemarbeit, die das Tier dafür aufbringen muss? Eine reine Frequenzmessung ist hierfür unzureichend und kann sogar in die Irre führen, weil sowohl Stress als auch Schmerz die Atemfrequenz erhöhen können, während eine Erschöpfung im Spätstadium zu einer scheinbar „normalen“ oder sogar sinkenden Frequenz führt. Deshalb wird die Atmung immer als Gesamteindruck bewertet: Thoraxexkursion und -symmetrie, Atemtiefe, Einsatz der Bauchpresse, orthopnoische Haltung (Kopf/Hals vorgestreckt, Ellenbogen abduziert), Nasenflügeln, Atemgeräusche (Stridor, Giemen, Rasseln), Zyanose sowie die Fähigkeit, in Ruhe zu atmen und sich ohne Panik zu regulieren. Ergänzend wird auf Anzeichen von Erschöpfung geachtet, z. B. flacher werdende Atemzüge trotz hoher Atemarbeit, wechselnde Atemmuster oder ein Nachlassen der Aufmerksamkeit bei weiterhin ausgeprägter Dyspnoe. Diese Befunde liefern in der Präklinik häufig mehr Informationswert als einzelne Messgeräteparameter.
Die präklinische Beurteilung beginnt mit der pragmatischen Differenzierung: Liegt primär ein Oxygenierungsproblem (Hypoxämie) oder ein Ventilationsproblem (Hyperkapnie) vor – oder beides? Hypoxämie entsteht typischerweise durch Störungen des alveolären Gasaustauschs (z. B. Lungenödem, Pneumonie, Aspiration, Kontusion, Pleuraerguss), während Hyperkapnie eher Ausdruck einer unzureichenden Ventilation ist (z. B. obere Atemwegsobstruktion, schwere Bronchokonstriktion, neuromuskuläre Schwäche, Erschöpfung). Klinisch sind diese Zustände nicht immer sauber trennbar, aber bestimmte Muster sind typisch: Zyanose, zunehmende Atemarbeit und Unruhe sprechen für eine kritische Oxygenierungsstörung; eine „pumpende“ Atmung mit ineffektiver Ventilation, eventuell begleitet von Bewusstseinsveränderungen, kann auf Hyperkapnie und Erschöpfung hinweisen. Hecheln kann Hypoxie maskieren, weil es die Dynamik der Atembewegung verändert, ohne zwingend den alveolären Gasaustausch ausreichend zu verbessern. Umgekehrt ist eine sinkende Atemfrequenz bei weiter bestehender Atemnot ein Spätzeichen und deutet häufig auf Erschöpfung hin – diese Konstellation ist präklinisch besonders gefährlich.
Sauerstofftherapie ist in der präklinischen Versorgung häufig die wichtigste und zugleich niedrigschwellige Maßnahme, weil sie die Hypoxie reduziert, den arteriellen Sauerstoffgehalt erhöht und wertvolle Zeit bis zur definitiven Therapie gewinnt. Die Sauerstoffgabe ist jedoch nur dann wirksam, wenn sie die Stresslast nicht erhöht. Bei vielen Tieren ist der physiologische Nutzen einer hohen FiO₂ geringer als der Schaden, der durch Panik, Abwehr und Stress-induzierte Dekompensation entsteht. Die praktische Entscheidungsregel lautet daher: O₂ so früh wie möglich – aber so stressarm wie möglich. Je nach Temperament, Atemnotgrad und Handling-Toleranz wird das geeignete System ausgewählt. In der Ausbildung wird deshalb nicht nur die Indikation, sondern vor allem die Applikationsstrategie trainiert.
Flow-by-Sauerstoff ist häufig der erste Schritt, weil er ohne direkte Fixation am Tier eingesetzt werden kann. Je nach Abstand und Flow lässt sich die inspiratorische Sauerstoffkonzentration moderat erhöhen. Vorteil ist die geringe Invasivität und die hohe Akzeptanz bei ängstlichen oder dyspnoischen Tieren. Nachteil ist die begrenzte und schwankende FiO₂, insbesondere bei starkem Hecheln oder wenn das Tier den Kopf bewegt. Dennoch ist Flow-by in vielen Situationen die beste initiale Maßnahme, weil er stabilisiert, ohne eine Stressspirale auszulösen.
Sauerstoffmaske kann bei tolerierten Tieren eine deutlich höhere FiO₂ erreichen. Sie ist allerdings nur sinnvoll, wenn das Tier die Maske akzeptiert und die Handhabung ruhig bleibt. Eine Maske, die Abwehrverhalten, Panik oder Würgen provoziert, verschlechtert die Ventilation, steigert den Sauerstoffverbrauch und erhöht das Risiko eines Stresskollapses. Daher gilt präklinisch: Maskenapplikation ist nicht „Standard“, sondern eine Option für Tiere, die kooperieren oder sich unter ruhigen Bedingungen führen lassen. In der Ausbildung wird besonders darauf geachtet, dass Personal die Grenze zwischen sinnvoller Unterstützung und schädlicher Fixation zuverlässig erkennt.
Nasenkatheter können in geübten Händen eine effektive Sauerstoffgabe bei relativ guter FiO₂ liefern und sind für längere Transporte relevant. Sie erfordern jedoch Material, Fixierung und eine sichere Technik. Präklinisch sind sie daher eher eine Maßnahme für Teams mit entsprechender Ausbildung und Ausrüstung. Die Entscheidungslogik lautet hier: Wenn ein Nasenkatheter sicher gelegt werden kann, ohne das Tier zu destabilisieren, ist er eine sinnvolle Option; wenn die Anlage Stress, Abwehr oder Verzögerung erzeugt, ist Flow-by oder Box häufig überlegen.
Sauerstoffboxen bieten eine ruhige Umgebung und ermöglichen eine stressarme Oxygenierung, weil das Tier nicht unmittelbar manipuliert werden muss. Sie sind besonders geeignet für Katzen oder sehr ängstliche Hunde, die Maske und Fixation nicht tolerieren. Gleichzeitig muss die Box ausreichend belüftet sein, da bei unzureichender Ventilation CO₂ ansteigen kann. In der Praxis wird daher auf kurze Öffnungsintervalle, angemessenen Flow und eine Beobachtung des klinischen Verlaufs geachtet. Der Vorteil der Box liegt nicht nur in der FiO₂, sondern in der Reduktion von Stress – und damit in einer realen Senkung des Sauerstoffbedarfs.
Ein didaktisch zentraler Punkt ist: Sauerstoff allein behebt keine mechanische Ursache. Ein Pneumothorax, ein Pleuraerguss, eine schwere obere Atemwegsobstruktion oder eine ausgeprägte Bronchokonstriktion können trotz O₂-Gabe zu fortschreitender Erschöpfung führen. Deshalb ist die Re-Evaluation der Kern des präklinischen Atemmanagements. Nach Beginn der Sauerstofftherapie werden Schleimhautfarbe, Atemarbeit, Atemmuster und mentale Lage erneut geprüft. Verbessert sich die Atemarbeit, sinkt die Unruhe, und wird die Schleimhautfarbe rosiger, spricht das für einen Effekt der Maßnahme. Bleibt die Situation unverändert oder verschlechtert sich, muss die Transportpriorität steigen und die Zielklinik vorab informiert werden, weil eine definitive Intervention (z. B. Entlastung bei Thoraxproblemen, Sedierung/Intubation, weiterführende Diagnostik) notwendig sein kann.
Fallbeispiel: Eine Katze mit akuter Dyspnoe toleriert keine Maske. Bei jeder Annäherung wird sie panisch, hechelt, versucht zu entkommen und entwickelt dabei eine deutlich stärkere Zyanose. In dieser Situation ist der „Kampf“ um die Maske nicht nur ineffektiv, sondern potenziell lebensgefährlich. Die sinnvolle präklinische Lösung ist Flow-by oder eine Sauerstoffbox in ruhiger Umgebung, minimale Manipulation, kurze Handgriffe und der priorisierte Transport. Dieses Beispiel verdeutlicht den Zusammenhang zwischen Stress und respiratorischer Dekompensation: Die technische Maßnahme ist nur dann hilfreich, wenn sie physiologisch entlastet und nicht durch Stress kompensatorisch „aufgefressen“ wird.
Für den Einsatz bedeutet das: Struktur vor Geschwindigkeit – dennoch entscheidet bei respiratorischer Insuffizienz jede Minute über die Prognose. Struktur heißt, dass Atemnot systematisch abgearbeitet wird (A/B im Zentrum), während Geschwindigkeit bedeutet, dass Zeit nicht in unnötige Maßnahmen investiert wird. Eine Intervention ist erst dann abgeschlossen, wenn ihre Wirkung überprüft wurde. Die klinische Beurteilung bei Hund und Katze ist häufig aussagekräftiger als einzelne Messwerte, sofern sie konsequent wiederholt und im Trend dokumentiert wird. Dokumentiert werden sollten insbesondere: Atemmuster (z. B. inspiratorisch/exspiratorisch), Atemarbeit, Schleimhautfarbe, Reaktionslage, angewendetes Sauerstoffsystem und erkennbare Veränderung nach Intervention.
Teamorganisation verbessert die Patientensicherheit maßgeblich. Eine klare Rollenverteilung (Airway/O₂, Monitoring, Transport, Kommunikation) reduziert kognitive Last, verhindert Doppelarbeit und erleichtert die zyklische Reevaluation. Parallel wird eine knappe, aber konsistente Dokumentation geführt: Zeitpunkt der ersten Beobachtung, Beginn der Sauerstoffgabe, System/Flow, klinische Reaktion, Veränderungen im Verlauf. Eine stressarme Lagerung und eine ruhige Umgebung sind bei Tieren häufig genauso wirksam wie technische Maßnahmen, weil sie Atemarbeit und Sauerstoffverbrauch senken. Diese Grundprinzipien werden in der Ausbildung gezielt trainiert: Erkennen von Atemarbeit, sichere Anwendung der O₂-Systeme, Vermeidung von Stress-induziertem Kollaps und konsequente Reevaluation.
Die sichere Übergabe an die Klinik umfasst Problem, Befunde, Maßnahmen, Reaktion und Risiken – nicht nur Einzelwerte. Für das respiratorische Notfallmanagement bedeutet das konkret: Verdachtsdiagnose bzw. Hauptproblem (z. B. obere Obstruktion, thorakales Problem, Parenchymschaden), klinische Zeichen (Atemarbeit, Zyanose, Geräusche, Haltung), eingesetzte Sauerstoffform, Reaktion auf O₂ und relevante Trends (besser/schlechter, stabil/instabil). Eine frühzeitige Voranmeldung ermöglicht der Zielklinik, Ressourcen vorzubereiten (Intubation, Bildgebung, Thoraxentlastung, Intensivmonitoring) und Verzögerungen zu vermeiden.

Wenn A/B instabil: Vor-Ort-Zeit minimieren, keine Diagnostik erzwingen.
Thoraxtraumata gehören in der präklinischen Tierrettung zu den häufigsten und gleichzeitig gefährlichsten Verletzungsmustern. Typische Auslöser sind Verkehrsunfälle, Stürze aus Höhe, Tritte, Quetschungen oder Bissverletzungen. Atemnot entsteht dabei nicht durch „ein“ Problem, sondern durch mehrere mögliche Mechanismen: Pneumothorax, Hämatothorax, Pleuraerguss, Lungenkontusion, Rippenfrakturen mit instabiler Thoraxwand sowie sekundäre Komplikationen wie schmerzbedingte Hypoventilation oder aspirative Ereignisse. Für das präklinische Management ist entscheidend, dass bei Thoraxtrauma die respiratorische Situation innerhalb kurzer Zeit kippen kann – entweder sofort (z. B. Spannungspneumothorax) oder verzögert über Stunden (z. B. Kontusionsprogression). Der klinische Fokus liegt daher auf frühzeitiger Erkennung, konsequenter Oxygenierung, stressarmer Handhabung und der raschen Zuführung in eine Einrichtung, die definitive Diagnostik und Interventionen (Thoraxdrainage, Thorakozentese, Analgesie, Beatmung, Monitoring) durchführen kann.
Pathophysiologisch ist die Rolle des Pleuraspalts zentral. Im Normalzustand besteht zwischen Lunge und Thoraxwand ein Unterdruck, der die Lunge entfaltet hält. Gelangt Luft in diesen Spalt, geht der Unterdruck verloren und die betroffene Lunge kollabiert partiell oder vollständig. Der resultierende Pneumothorax reduziert die ventilierte Alveolarfläche, verschlechtert den Gasaustausch und erhöht die Atemarbeit deutlich. Viele Tiere kompensieren anfangs durch erhöhte Atemfrequenz und Atemtiefe, wirken dabei aber bereits deutlich angestrengt. Je nach Ausmaß kommt es rasch zu Hypoxie, Unruhe, Zyanose und Erschöpfung. Klinisch sind typische Hinweise eine akute Dyspnoe, flache schnelle Atmung, orthopnoische Haltung, Angst/Panik, ggf. einseitig verminderte Thoraxexkursion und abgeschwächte Atemgeräusche. Das Muster ist nicht immer eindeutig, weil Fell, Körperbau, Stress und Umgebungsgeräusche die Auskultation erschweren können. Dennoch gilt: Einseitig deutlich reduzierte Atemgeräusche in Kombination mit Trauma und zunehmender Dyspnoe sind präklinisch hochverdächtig.
Beim Spannungspneumothorax entwickelt sich die Situation dramatischer. Durch eine Ventilmechanik (Luft gelangt hinein, kann aber nicht entweichen) steigt der intrathorakale Druck progressiv an. Das hat zwei lebensbedrohliche Effekte: Erstens verschlechtert sich die Ventilation durch zunehmenden Lungenkollaps; zweitens wird der venöse Rückstrom zum Herzen komprimiert. Dadurch sinkt die Vorlast, das Herzzeitvolumen fällt ab, und es entsteht ein obstruktiver Schock. Das erklärt, warum bei Spannungspneumothorax nicht nur respiratorische, sondern auch kardiovaskuläre Zeichen auftreten: fadenförmiger Puls, kalte Extremitäten, verlängerte Rekapillarisierungszeit, Bewusstseinsveränderung und rasche Kreislaufinstabilität. Präklinisch ist dies eine Lage, in der Minuten zählen. Entscheidend ist, die Kombination aus akuter Dyspnoe und sich verschlechternden Perfusionszeichen als Warnsignal zu erkennen und den Transport unmittelbar zu priorisieren.
Ein weiterer zentraler Mechanismus ist der Hämatothorax oder ein traumatisch bedingter Pleuraerguss. Flüssigkeit im Pleuraspalt verdrängt die Lunge, reduziert das funktionelle Lungenvolumen und erhöht die Atemarbeit. Klinisch kann das Bild dem Pneumothorax ähneln, wobei Auskultationsbefunde oft gedämpft wirken. Klassisch ist beim Erguss eine stärkere Dämpfung ventral, während beim Pneumothorax Atemgeräusche eher dorsal reduziert sind. In der Praxis ist diese Abgrenzung jedoch unsicher und darf präklinisch nicht zur Verzögerung führen. Die Schwere der Dyspnoe und der Verlauf (Trend) sind entscheidender als die „perfekte“ Differenzialdiagnose am Einsatzort.
Besonders tückisch sind Lungenkontusionen. Sie entstehen durch stumpfe Gewalteinwirkung mit Einblutung und Ödembildung im Lungengewebe. Der klinische Verlauf ist häufig verzögert: Das Tier kann initial „noch“ kompensieren und scheinbar stabil wirken, verschlechtert sich aber über Stunden durch zunehmende Ödematisierung, inflammatorische Reaktion und gestörten Gasaustausch. Diese Dynamik ist didaktisch wichtig: Ein unauffälliger erster Eindruck schließt eine lebensbedrohliche Progression nicht aus. Für die Präklinik folgt daraus die Notwendigkeit konsequenter Reevaluation und eine niedrige Schwelle zur Transportentscheidung, insbesondere wenn Atemarbeit, Schleimhautfarbe oder mentale Lage auch nur leicht grenzwertig sind.
Präklinisch steht bei Thoraxtrauma die Kombination aus Oxygenierung, Wärmeschutz, schmerzreduzierender, schonender Lagerung und schnellem Transport im Vordergrund. Sauerstofftherapie wird so angewendet, dass Stress minimiert wird: Flow-by oder Sauerstoffbox sind oft besser als eine Maske, die als Bedrohung empfunden wird. Wärmeerhalt ist essenziell, weil Hypothermie die Kompensationsfähigkeit verschlechtert und – insbesondere bei Trauma – zur Verschärfung von Gerinnungsstörungen beiträgt. Lagerung bedeutet in der Praxis: so wenig Umlagern wie möglich, Atemmechanik unterstützen (häufig sternal oder in der Position, die das Tier selbst wählt), Druck auf den Thorax vermeiden, Kopf/Hals in neutraler Position halten und eine sichere, ruhige Umgebung schaffen. Schonende Handhabung reduziert nicht nur Schmerz, sondern auch die Stressantwort, die den Sauerstoffverbrauch und die Atemarbeit erhöht.
Eine invasive Entlastung, insbesondere die Thorakozentese (Nadelentlastung/Entlastungspunktion), ist eine fortgeschrittene Maßnahme. Sie ist präklinisch nicht Routine, sondern eine Option unter klar definierten Kriterien: schwerste Dyspnoe, hochgradiger Verdacht auf Pneumothorax, rasche klinische Verschlechterung und fehlende Alternative durch unmittelbare Klinikintervention. Voraussetzung sind entsprechende Ausbildung, steriles Material, geeignete Kanülen/Schläuche, Verständnis der Anatomie sowie die Fähigkeit, Risiken (Fehllage, Blutung, iatrogene Verletzung, Verschlechterung durch Stress) zu kontrollieren. Didaktisch ist wichtig, dass Teams lernen, wann nicht zu punktieren: wenn die Indikation unsicher ist, wenn die Durchführung die Lage destabilisiert oder wenn ein schneller Transport verfügbar ist. In vielen Fällen ist der zeitkritische Transport mit Sauerstoff und minimaler Manipulation die sicherere Strategie.
Fallbeispiel: Ein Hund nach Autounfall atmet oberflächlich, ist zyanotisch, und rechts sind Atemgeräusche deutlich abgeschwächt. Der Puls wird zunehmend fadenförmig, die Rekapillarisierungszeit verlängert sich. Dieses Muster ist kompatibel mit Pneumothorax und drohendem obstruktivem Schock. Präklinische Konsequenz: sofortige Sauerstoffgabe (stressarm), Wärmeschutz, möglichst geringe Manipulation, Lagerung zur Atemerleichterung und unmittelbarer Transport. Die Voranmeldung an die Zielklinik lautet nicht „Hund im Schock“, sondern strukturiert: „Thoraxtrauma, hochgradiger Verdacht Pneumothorax, zunehmende Kreislaufinstabilität, O₂ läuft, Trend schlechter“. Damit kann die Klinik Thoraxentlastung, Drainageanlage und Intensivmonitoring ohne Verzögerung vorbereiten.
In der Ausbildung wird zudem die Abgrenzung zu anderen Ursachen gelehrt, um typische Fehlentscheidungen zu vermeiden. Pleuraerguss zeigt klinisch häufig gedämpfte Atemgeräusche ventral und eingeschränkte Thoraxexkursion; Pneumothorax eher dorsal reduzierte Geräusche und eine „hohle“ Auskultation. Kontusionen können zunächst relativ unspezifisch sein und später progredient. Entscheidend ist jedoch, dass präklinische Unsicherheit normal ist und kein Grund für Zögern sein darf. Die Transportentscheidung orientiert sich an der Schwere der Dyspnoe, an Perfusionszeichen und am Trend, nicht an einer perfekten Differenzialdiagnose vor Ort. Ein Tier, das „noch“ kompensiert, kann innerhalb weniger Minuten oder Stunden kippen – besonders bei Thoraxverletzungen.
Qualität im Thoraxtrauma-Management entsteht durch wiederholte klinische Beurteilung und konsequente Priorisierung. Die häufigsten Fehler sind Unterschätzung von Dyspnoe, fehlender Wärmeschutz, unnötige Manipulation und verzögerter Transport. Daher wird das Prinzip „Intervention – Reevaluation“ konsequent umgesetzt: Nach Sauerstoffgabe werden Schleimhautfarbe, Atemarbeit und mentale Lage erneut geprüft; nach Lagerung und Wärmeschutz werden Atemmuster und Perfusionszeichen beurteilt. Parallel bleibt der Blick auf mögliche Kreislaufdekompensation wichtig, weil ein Spannungspneumothorax rasch in einen obstruktiven Schock übergehen kann. In der Teamarbeit werden Rollen klar verteilt (Airway/O₂, Monitoring, Transport, Kommunikation), um kognitive Last zu reduzieren und die Re-Evaluation sicherzustellen. Die Übergabe an die Klinik umfasst Problem, Befunde, Maßnahmen, Reaktion und Risiken – nicht nur Einzelwerte.
Zusammengefasst ist Thoraxtrauma präklinisch ein „Zeit- und Trendproblem“: Die Schwere der Atemarbeit, die Dynamik der Verschlechterung und die Gefahr eines obstruktiven Schocks bestimmen die Prioritäten. Oxygenierung, Wärmeschutz und stressarme Handhabung schaffen die Brücke zur definitiven Therapie; invasive Maßnahmen bleiben fortgeschrittenen Teams und klarer Indikation vorbehalten. Eine ruhige Umgebung und schonende Lagerung sind dabei oft genauso wirksam wie technische Maßnahmen, weil sie Atemarbeit und Sauerstoffverbrauch reduzieren und damit die fragile Kompensation stabilisieren.

Merksatz: O₂ kann SpO₂ verbessern, aber Hyperkapnie bleibt möglich, wenn Ventilation versagt.
Ventilation beschreibt im engeren physiologischen Sinn die effektive CO₂-Elimination und ist damit von der Oxygenierung zu unterscheiden. Während Sauerstoffgabe primär das arterielle O₂-Angebot erhöht, hängt die Entfernung von Kohlendioxid vom Atemminutenvolumen, vom Totraumanteil und von der Leistungsfähigkeit der Atemmuskulatur ab. Ein Tier kann daher trotz adäquater Sauerstoffzufuhr hyperkapnisch werden, wenn die Ventilation unzureichend ist. Ursachen sind unter anderem Erschöpfung der Atemmuskulatur, neuromuskuläre Erkrankungen, schwere obere Atemwegsobstruktionen, ausgeprägte bronchiale Verengungen, thorakale Restriktionen oder massive Parenchymschädigungen. Präklinisch ist es entscheidend, diese Unterscheidung zu verstehen: Sauerstoff verbessert nicht automatisch die Ventilation.
Das Atemminutenvolumen ergibt sich aus Atemfrequenz multipliziert mit Atemzugvolumen. Entscheidend ist jedoch nicht die bloße Anzahl der Atemzüge, sondern deren Effektivität. Kleine, flache Atemzüge erhöhen vor allem die Totraumventilation – also den Anteil der Luft, der die leitenden Atemwege belüftet, ohne am Gasaustausch teilzunehmen. In dieser Situation kann die Atemfrequenz hoch sein, während CO₂ nicht ausreichend eliminiert wird. Die Folge ist eine zunehmende Hyperkapnie mit respiratorischer Azidose. Klinisch äußert sich dies in Unruhe, später Desorientierung, zunehmender Müdigkeit bis hin zur Bewusstseinseintrübung. In schweren Fällen kommt es zu einer paradoxen Atmung oder zu einer sichtbaren Diskrepanz zwischen Atemarbeit und tatsächlichem Luftaustausch.
Klinische Hinweise auf eine drohende ventilatorische Erschöpfung sind besonders relevant. Dazu gehören eine paradoxe Atmung (Einziehen des Thorax bei Inspiration), eine abnehmende Atemfrequenz trotz weiterhin hoher Atemanstrengung, ein Wechsel von hektischer Unruhe zu plötzlicher „Ruhe“, zunehmende Bewusstseinstrübung sowie ein sogenannter „silent chest“ bei schwerer bronchialer Obstruktion. Letzteres bedeutet, dass kaum noch Atemgeräusche hörbar sind – nicht weil die Situation sich gebessert hätte, sondern weil kaum noch Luft bewegt wird. Dieses Zeichen wird präklinisch häufig fehlinterpretiert. Ein ruhigeres Tier mit sinkender Atemfrequenz ist bei schwerer Dyspnoe kein Zeichen der Besserung, sondern ein potenzielles Zeichen des bevorstehenden Atemversagens.
Bei Hunden ist starkes Hecheln physiologisch zur Thermoregulation, kann jedoch auch pathologisch sein. Bei respiratorischer Insuffizienz ist häufig eine orthopnoische Haltung zu beobachten: Kopf und Hals werden vorgestreckt, die Ellenbogen abgespreizt, um die Atemmechanik zu optimieren. Katzen zeigen oft subtilere Zeichen, etwa eine reduzierte Aktivität, verstecktes Verhalten oder eine stille, angestrengte Atmung mit minimaler Thoraxexkursion. Präklinisch ist daher nicht nur das offensichtliche „Schnaufen“ relevant, sondern auch leise, flache, aber angestrengte Atembewegung.
Ein zentrales Prinzip lautet: Ventilation ist ein dynamischer Prozess. Wenn ein Tier trotz Sauerstoffgabe nicht stabiler wird oder sich sogar verschlechtert, darf nicht abgewartet werden. Die Eskalation muss rechtzeitig erfolgen. Das bedeutet konkret: Transport priorisieren, Zielklinik voranmelden und darauf hinweisen, dass möglicherweise Sedierung, Intubation oder Beatmung erforderlich werden. Präklinisch sind kurze Eingriffszeiten, eine Lagerung mit freier Thoraxbewegung, Minimierung von Druck auf den Brustkorb und kontinuierliche Reevaluation essenziell. Jede Manipulation, die Stress erhöht, steigert den Sauerstoffverbrauch und verschlechtert die ventilatorische Situation zusätzlich.
Fallbeispiel: Ein Hund mit schwerer allergischer Reaktion zeigt zunächst starkes Hecheln und ausgeprägte Unruhe. Nach einigen Minuten wird er plötzlich ruhig, die Atemfrequenz sinkt, die Schleimhäute werden grau, und der Blick wirkt leer. Diese Konstellation ist kein „Besserwerden“, sondern ein Zeichen der Erschöpfung und drohenden Ateminsuffizienz. Präklinisch darf hier nicht gezögert werden: Sauerstoff läuft weiter, Stress wird minimiert, Transport wird sofort priorisiert und die Klinik vorab informiert, dass ein respiratorisches Versagen wahrscheinlich ist.
Technische Monitoringverfahren können die klinische Einschätzung unterstützen, ersetzen sie jedoch nicht. Die Pulsoxymetrie (SpO₂) gibt Hinweise auf die arterielle Sauerstoffsättigung, kann jedoch bei Ventilationsstörungen trügerisch normal erscheinen, solange die Oxygenierung noch ausreichend ist. Gleichzeitig kann CO₂ bereits ansteigen. Die Kapnographie, sofern verfügbar, liefert wertvolle Informationen zur CO₂-Elimination und damit zur Ventilation. Ein steigender endtidaler CO₂-Wert (ETCO₂) oder eine veränderte Kurvenform können frühzeitig auf Hypoventilation hinweisen. Dennoch bleibt das klinische Bild maßgeblich: Atemarbeit, Bewusstseinslage, Schleimhautfarbe und Trendbeurteilung sind entscheidend.
Für den Einsatz gilt: Struktur vor Geschwindigkeit – dennoch entscheidet bei respiratorischer Insuffizienz jede Minute über die Prognose. Struktur bedeutet, dass Hypoxie, Hyperkapnie und Kreislaufdekompensation stets gemeinsam gedacht werden. Hyperkapnie kann zur Vasodilatation und Kreislaufbelastung beitragen; Hypoxie verschlechtert Myokardfunktion und Bewusstsein; Kreislaufdekompensation wiederum reduziert die pulmonale Perfusion. Diese Wechselwirkungen verstärken sich gegenseitig. Deshalb ist es notwendig, Atem- und Kreislaufparameter parallel zu beobachten und regelmäßig neu zu bewerten.
Typische Fehler im ventilatorischen Notfallmanagement sind die Unterschätzung von Dyspnoe, fehlender Wärmeschutz, unnötige Manipulation und verzögerter Transport. Hypothermie verschlechtert die Atemmuskelfunktion und die Kreislaufkompensation. Unnötige Umlagerung oder Fixierung kann Stress-induzierten Kollaps auslösen. Verzögerungen entstehen häufig durch die falsche Annahme, das Tier „beobachten“ zu können, obwohl es bereits Zeichen der Erschöpfung zeigt. Eine Intervention ist erst dann abgeschlossen, wenn ihre Wirkung überprüft wurde. Reevaluation ist kein formaler Schritt, sondern die Sicherheitsbarriere gegen Fehleinschätzungen.
Didaktisch ist die Kopplung von Pathophysiologie und praktischer Umsetzung zentral. Theorie erklärt, warum Totraumventilation CO₂ nicht effektiv eliminiert oder warum eine sinkende Atemfrequenz bei schwerer Dyspnoe alarmierend ist. Praxis trainiert das Erkennen von Atemarbeit, den stressarmen Umgang mit Sauerstoffsystemen und die sichere Organisation des Transports. Eine klare Teamrolle (Airway/O₂, Monitoring, Transport, Kommunikation) reduziert kognitive Last und erhöht die Sicherheit. Die Übergabe an die Klinik umfasst Problem, Befunde, Maßnahmen, Reaktion und Risiken – nicht nur Einzelwerte.
Zusammenfassend ist Ventilation mehr als „viel atmen“. Entscheidend ist die Effektivität des Gasaustauschs und die Fähigkeit des Organismus, CO₂ auszuscheiden. Ein scheinbar ruhiger Patient kann kurz vor dem respiratorischen Versagen stehen. Wer die Zeichen der Erschöpfung erkennt und rechtzeitig eskaliert, verhindert das Abrutschen in eine irreversible Situation. Präklinisches Atemmanagement bedeutet daher: früh erkennen, stressarm stabilisieren, konsequent reevaluieren und ohne Verzögerung die definitive Therapie ermöglichen.
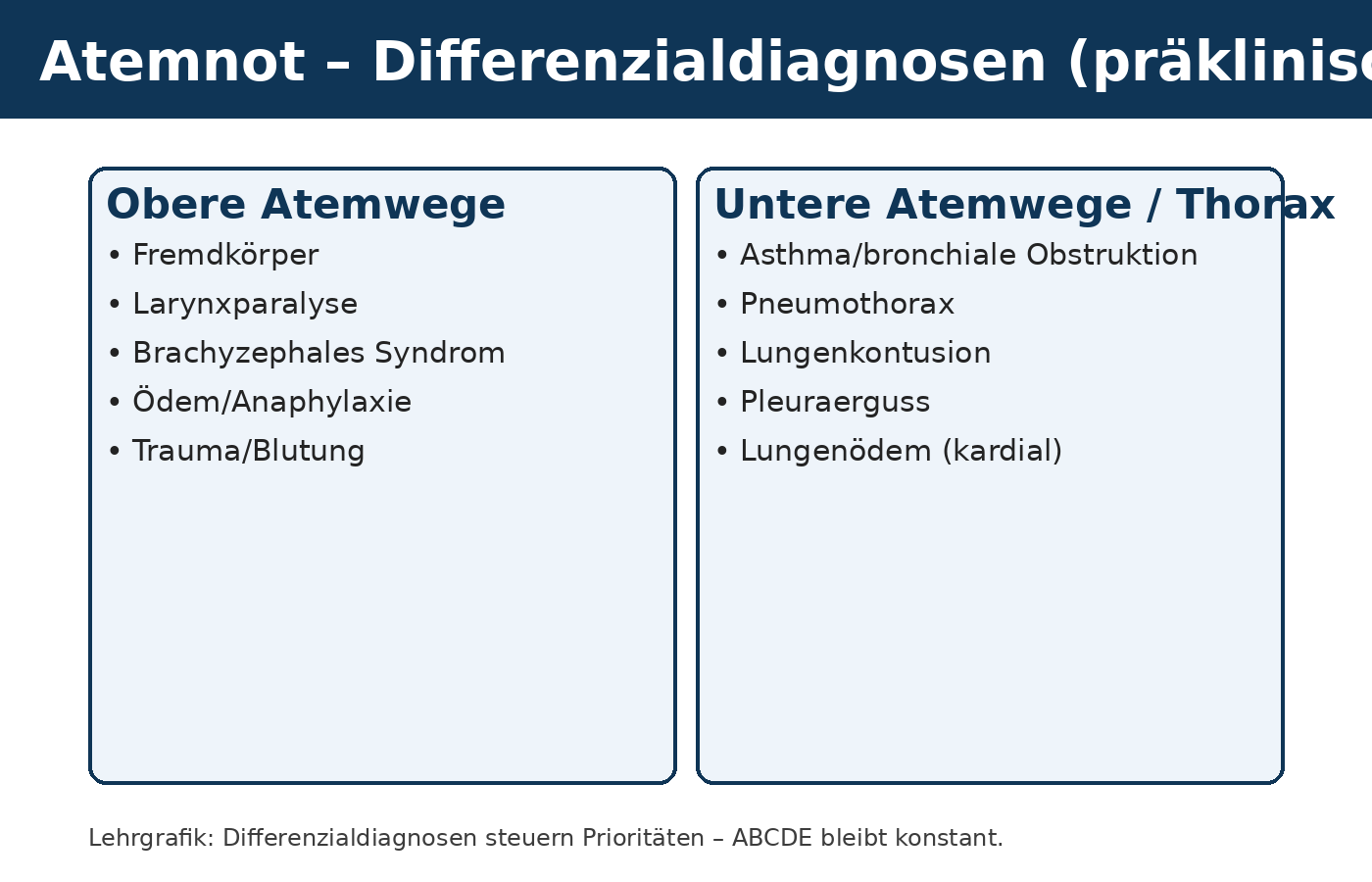
Ziel: nicht „perfekt diagnostizieren“, sondern Risiko und Transportpriorität ableiten.
Die präklinische Differenzialdiagnostik der Atemnot verfolgt kein akademisches Ziel, sondern dient der Priorisierung unter Zeitdruck. Entscheidend ist nicht, vor Ort jede Ursache zweifelsfrei zu identifizieren, sondern gefährliche Muster zu erkennen, reversible Bedrohungen frühzeitig zu adressieren und Maßnahmen mit hohem Nutzen bei geringem Risiko einzuleiten. Die leitende Frage lautet: Welche Pathophysiologie ist wahrscheinlich, welche ist akut lebensbedrohlich, und welche Intervention verschafft dem Tier mit minimaler Belastung Zeit bis zur definitiven Therapie?
Systematisch lassen sich respiratorische Notfälle in mehrere funktionelle Kategorien einteilen: obere Atemwegsobstruktion, untere Atemwegserkrankung, thorakale Restriktion, kardiale Ursache und metabolische Störung. Diese Einteilung erleichtert die Orientierung, auch wenn Mischformen häufig sind. Bei oberen Atemwegsproblemen – etwa Fremdkörpern, Larynxparalyse, brachyzephalem Atemnotsyndrom oder entzündlichem Ödem – steht die mechanische Behinderung des Luftstroms im Vordergrund. Klinisch dominieren inspiratorischer Stridor, Maulatmung, Speichelfluss, Panik und rasche Zyanose. Hier ist Stressreduktion essenziell, da jede Aufregung den Atemwegswiderstand erhöht und den Sauerstoffverbrauch steigert. Atemwegsschutz und minimal-invasive Sauerstoffgabe sind Maßnahmen mit hohem Nutzen und geringem Risiko.
Untere Atemwegserkrankungen wie felines Asthma oder bronchiale Obstruktion zeigen typischerweise eine exspiratorische Dyspnoe mit verlängertem Ausatmen, Giemen und erhöhter Atemarbeit. Das Tier presst aktiv aus, um Luft aus verengten Bronchien zu befördern. Ein „silent chest“ bei schwerer Obstruktion ist ein Spätzeichen und darf nicht als Besserung interpretiert werden. Auch hier gilt: Stressarme Umgebung, Sauerstoff, schnelle Transportentscheidung. Eine forcierte Fixierung oder unnötige Manipulation kann einen vollständigen Kollaps auslösen.
Thorakale Ursachen wie Pneumothorax, Hämatothorax oder Pleuraerguss beeinträchtigen die Lungenentfaltung mechanisch. Die Thoraxexkursion ist reduziert, Atemgeräusche sind je nach Verteilung dorsal oder ventral abgeschwächt. Beim Pneumothorax findet sich häufig dorsal eine verminderte Auskultation, beim Erguss eher ventral – diese Orientierung kann helfen, ersetzt jedoch keine Bildgebung. Klinisch steht die Schwere der Dyspnoe im Vordergrund. Eine sichere Differenzierung ist präklinisch oft nicht möglich, weshalb die Transportpriorität am Trend und am Allgemeinzustand ausgerichtet wird.
Kardiale Ursachen wie ein akutes Lungenödem präsentieren sich häufig mit Tachypnoe, Husten und gegebenenfalls schaumigem Nasen- oder Maulsekret. Die Schleimhäute können blass oder leicht zyanotisch sein. Entscheidend ist hier das Verständnis der Pathophysiologie: Eine aggressive Volumengabe ist kontraindiziert, da sie die pulmonale Stauung verstärken kann. Die präklinische Maßnahme besteht primär in Sauerstoffgabe, Stressminimierung und zügiger Übergabe an eine Einrichtung mit Möglichkeit zur diuretischen und intensivmedizinischen Therapie.
Metabolische Ursachen, insbesondere eine metabolische Azidose, führen zu kompensatorischer Hyperventilation. Diese tiefe, regelmäßige Atmung dient der CO₂-Elimination zur pH-Stabilisierung. Hier liegt das Problem nicht primär in der Lunge, sondern im Stoffwechsel. Dennoch kann die Atemarbeit hoch sein und zur Erschöpfung führen. Auch in diesem Fall entscheidet die Trendbeobachtung: Verschlechtert sich das Bewusstsein oder sinkt die Atemfrequenz trotz fortbestehender Belastung, ist dies ein Alarmzeichen.
Didaktisch wird vermittelt, dass präklinische Diagnosen häufig Wahrscheinlichkeiten darstellen. Die klinische Realität erlaubt selten vollständige Sicherheit. Daher stehen Mustererkennung und Risikostratifizierung im Vordergrund. Zyanose, zunehmende Erschöpfung, massiv erhöhte Atemarbeit, Bewusstseinsveränderung oder Kreislaufzeichen sind Eskalationsindikatoren – unabhängig von der exakten Ursache. Die Entscheidung zum sofortigen Transport basiert auf Gefährdungsgrad und Dynamik, nicht auf diagnostischer Perfektion.
Fallbeispiel: Eine Katze mit plötzlich einsetzender Dyspnoe sitzt orthopnoisch, Hals gestreckt, atmet flach und toleriert keinerlei Manipulation. Differentialdiagnostisch kommen Asthma oder eine Pleuraerkrankung in Betracht. Präklinisch ist die Strategie identisch: Sauerstoffbox oder Flow-by, minimale Handhabung, ruhige Umgebung, sofortiger Transport mit Voranmeldung. Die definitive Abklärung (Ultraschall, Röntgen, Thorakozentese) erfolgt in der Klinik. Jede unnötige Manipulation vor Ort würde das Risiko einer Dekompensation erhöhen.
Zweites Fallbeispiel: Ein Hund nach Trauma zeigt Dyspnoe kombiniert mit fadenförmigem Puls und blassen Schleimhäuten. Hier muss an Pneumothorax oder intrathorakale Blutung gedacht werden. Die Kombination aus respiratorischer und hämodynamischer Instabilität ist besonders gefährlich. Präklinisch sind Sauerstoff, Wärmeschutz, stressarme Lagerung und sofortiger Transport mit klarer Voranmeldung („Verdacht Thoraxtrauma mit respiratorischer Beeinträchtigung“) indiziert.
Ein zentrales Qualitätsmerkmal präklinischer Arbeit ist die wiederholte Reevaluation. Eine Intervention ist erst abgeschlossen, wenn ihre Wirkung überprüft wurde. Verbessern sich Atemarbeit, Schleimhautfarbe und mentale Lage? Bleibt die Situation stabil oder verschlechtert sie sich? Trendbeurteilung ist wichtiger als Einzelmesswerte. Bei Hund und Katze ist die klinische Beobachtung häufig aussagekräftiger als isolierte technische Parameter, insbesondere wenn diese unter Stressbedingungen erhoben werden.
Die häufigsten Fehler in der Differenzialdiagnostik der Atemnot sind die Unterschätzung von Dyspnoe, fehlender Wärmeschutz, unnötige Manipulation und verzögerter Transport. Hypothermie verschlechtert die Kreislauf- und Atemmuskelfunktion. Übermäßige Untersuchungshandlungen erhöhen den Stress und damit den Sauerstoffverbrauch. Zeitverlust entsteht häufig durch den Versuch, vor Ort eine exakte Diagnose zu erzwingen. Präklinische Exzellenz bedeutet dagegen, Gefahren früh zu erkennen und sichere Basismaßnahmen konsequent umzusetzen.
Eine klare Teamstruktur reduziert kognitive Belastung: Eine Person fokussiert Atemweg und Sauerstoff, eine überwacht Parameter und dokumentiert Trends, eine organisiert Transport und Kommunikation. Die strukturierte Übergabe an die Klinik umfasst Problem, vermutete Ursache, klinische Befunde, durchgeführte Maßnahmen, Reaktion des Patienten und potenzielle Risiken. Diese strukturierte Kommunikation ist integraler Bestandteil der medizinischen Qualität.
Zusammenfassend verbindet die präklinische Differenzialdiagnostik der Dyspnoe Theorie und Einsatzrealität. Ziel ist nicht die vollständige ätiologische Klärung, sondern die sichere Navigation durch Unsicherheit. Wer gefährliche Muster erkennt, Stress minimiert, Sauerstoff effizient einsetzt und ohne Verzögerung die definitive Versorgung organisiert, verbessert Prognose und Patientensicherheit signifikant. Struktur geht vor Geschwindigkeit – doch bei respiratorischer Insuffizienz entscheidet jede Minute.
Single-Choice: pro Frage eine richtige Antwort. Bestehensgrenze: 70%.
Merksatz: Transport ist Therapie, wenn definitive Maßnahmen nur in der Klinik möglich sind.
Ausbildungsplattform (Tier-Notruf)
Ziel: Trend erkennen (besser/schlechter) statt Einzelwerte „schönrechnen“.
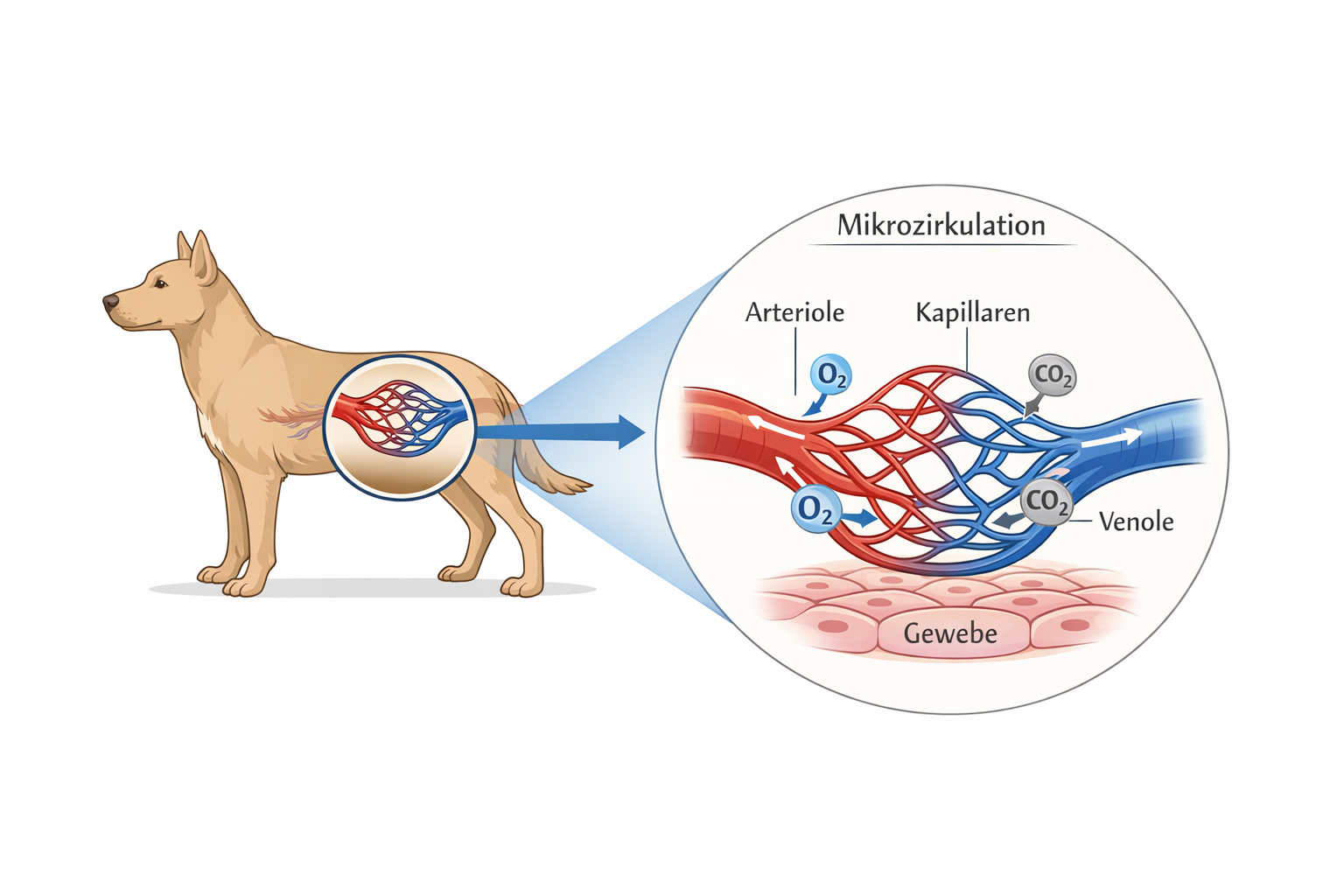
Der Schock stellt in der tiermedizinischen Notfallversorgung kein isoliertes Krankheitsbild dar, sondern ein zeitkritisches, potenziell letales Syndrom, das durch eine unzureichende effektive Gewebeperfusion und damit durch ein Missverhältnis zwischen Sauerstoffangebot (DO₂) und Sauerstoffbedarf der Zellen gekennzeichnet ist. Entscheidend ist das Verständnis, dass ein „akzeptabler Blutdruck“ nicht automatisch eine adäquate Mikrozirkulation bedeutet. Makrozirkulatorische Parameter wie systolischer Druck oder tastbarer Puls können noch im Normbereich liegen, während die Kapillardurchblutung bereits erheblich eingeschränkt ist und die zelluläre Sauerstoffextraktion versagt. Klinische Stabilität kann daher eine trügerische Momentaufnahme sein.
Physiologisch ergibt sich das Sauerstoffangebot aus dem Herzzeitvolumen multipliziert mit dem arteriellen Sauerstoffgehalt. Das Herzzeitvolumen wiederum ist das Produkt aus Herzfrequenz und Schlagvolumen. Das Schlagvolumen hängt von Vorlast, Nachlast und myokardialer Kontraktilität ab. Der arterielle Sauerstoffgehalt wird primär durch die Hämoglobinkonzentration und die Sauerstoffsättigung bestimmt; der physikalisch gelöste Sauerstoff spielt demgegenüber eine untergeordnete Rolle. Jede Störung entlang dieser Kette – Blutverlust, Hypoxämie, Pumpversagen oder ausgeprägte Vasodilatation – kann zu einer Reduktion des effektiven Sauerstoffangebotes führen.
In frühen Schockstadien dominieren kompensatorische Mechanismen des sympathoadrenalen Systems. Durch Freisetzung von Noradrenalin und Adrenalin steigen Herzfrequenz und Kontraktilität, während der systemische Gefäßwiderstand zunimmt. Diese Reaktion stabilisiert kurzfristig den arteriellen Blutdruck, geht jedoch mit einer Umverteilung des Blutflusses einher. Periphere Kompartimente wie Haut, Skelettmuskulatur und Splanchnikusgebiet werden zugunsten lebenswichtiger Organe wie Herz und Gehirn minderdurchblutet. Klinisch äußert sich diese Zentralisation durch blasse oder graue Schleimhäute, verlängerte Rekapillarisierungszeit, kalte Extremitäten, Tachykardie und einen schmalen, häufig „fadenförmigen“ Puls.
Parallel werden das Renin-Angiotensin-Aldosteron-System sowie das antidiuretische Hormon (ADH) aktiviert, um intravasales Volumen zu erhalten. Natrium- und Wasserretention stabilisieren vorübergehend die Kreislaufsituation, können jedoch bei persistierender Ursache die Mikrozirkulation zusätzlich beeinträchtigen. Vasokonstriktion auf Kapillarebene verschlechtert die Gewebeperfusion trotz scheinbar stabiler Makroparameter. Diese Diskrepanz zwischen Makro- und Mikrozirkulation ist klinisch bedeutsam und erklärt, weshalb Hypotonie häufig erst als Spätzeichen eines bereits fortgeschrittenen Schocks auftritt.
Auf zellulärer Ebene führt anhaltende Hypoperfusion zur Umstellung von aerober oxidativer Phosphorylierung auf anaerobe Glykolyse. Die ATP-Produktion sinkt, während Laktat akkumuliert und eine metabolische Azidose entsteht. Azidose reduziert die myokardiale Kontraktilität und die Gefäßreaktivität auf Katecholamine. Gleichzeitig versagen energieabhängige Ionenpumpen, wodurch intrazelluläres Natrium und Wasser ansteigen und ein Zellödem entsteht. Eine Kalziumüberladung aktiviert proteolytische und lipolytische Enzymkaskaden, die strukturelle Zellschäden verstärken. Persistiert dieser Zustand, entwickelt sich eine mitochondriale Dysfunktion mit fortschreitendem Organversagen.
Das Endothel spielt in diesem Prozess eine aktive Rolle. Die endotheliale Glykokalyx und interzelluläre Tight Junctions werden geschädigt, wodurch die Kapillarpermeabilität zunimmt. Es kommt zur Flüssigkeitsverschiebung ins Interstitium und damit zu einer funktionellen Hypovolämie. Gleichzeitig werden proinflammatorische Zytokine wie TNF-α, IL-1 und IL-6 freigesetzt, die eine systemische inflammatorische Antwort (SIRS) auslösen können. Koagulation und Inflammation sind eng miteinander verknüpft; Mikrothromben auf Kapillarebene verschärfen die Perfusionsheterogenität. Trotz makrozirkulatorischer Stabilisierung bleiben Gewebeinseln ischämisch, was die Diskrepanz zwischen gemessenen Druckwerten und tatsächlicher Sauerstoffversorgung erklärt.
Didaktisch ist die Unterscheidung verschiedener Schockstadien hilfreich. Im kompensierten Stadium erscheinen Blutdruck und Bewusstseinslage häufig noch relativ stabil, während Tachykardie und verlängerte Rekapillarisierungszeit frühe Warnzeichen darstellen. Im dekompensierten Stadium treten Hypotonie, deutliche Bewusstseinsstörungen und ein schwacher Puls hinzu. Das irreversible Stadium ist durch schwere mitochondriale Dysfunktion, therapieresistente Hypotonie und Multiorganversagen gekennzeichnet. Ein praxisrelevanter Merksatz lautet: Hypotonie ist meist ein Spätzeichen, während Tachykardie und veränderte Kapillarfüllzeit oft frühe Hinweise liefern.
Für die präklinische Einschätzung ist die konsequente Integration aller Befunde erforderlich. Die Beurteilung der Schleimhäute hinsichtlich Farbe und Feuchtigkeit sowie die Messung der Rekapillarisierungszeit liefern unmittelbare Hinweise auf Perfusionsqualität und sympathischen Tonus. Gleichzeitig müssen Herzfrequenz, Pulsqualität, Atemmuster und mentale Lage in die Bewertung einbezogen werden. Einzelwerte dürfen nicht isoliert interpretiert werden. Ein klinisch scheinbar stabiler Zustand kann eine fragile Kompensation darstellen, die bei zusätzlicher Belastung – beispielsweise Transportstress oder Blutverlustprogression – abrupt kollabiert.
Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter erheblich verschieben. Eine stressbedingte Tachykardie darf nicht mit adäquater Perfusion verwechselt werden. Umgekehrt kann eine nachlassende Herzfrequenz bei fortschreitender Erschöpfung ein Zeichen drohender Dekompensation sein. Die Aussagekraft steigt erheblich, wenn Befunde wiederholt erhoben und im zeitlichen Verlauf dokumentiert werden. Trendbeobachtungen sind in der Notfallmedizin häufig aussagekräftiger als Einzelmessungen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies: Atemwegssicherung und Oxygenierung, konsequente Blutungskontrolle, Wärmeerhalt zur Vermeidung einer hypothermiebedingten Koagulopathie sowie rascher Transport in eine Einrichtung mit Möglichkeiten zur definitiven Blutungskontrolle, Bildgebung und intensivmedizinischen Therapie. Ziel sind nicht „schöne Zahlen“, sondern die Begrenzung sekundärer Schäden wie Hypoxie, Hypothermie und Azidose.
Eine klare Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. hämorrhagisch, distributiv, kardiogen), Schockform, Stadium, Prioritäten und Transportziel müssen eindeutig benannt werden. Strukturierte Dokumentation unterstützt die klinische Weiterbehandlung und schafft Transparenz im Entscheidungsprozess. Die präklinische Versorgung endet nicht mit einer scheinbaren Stabilisierung von Makroparametern, sondern mit der sicheren Übergabe in eine weiterführende Behandlung.
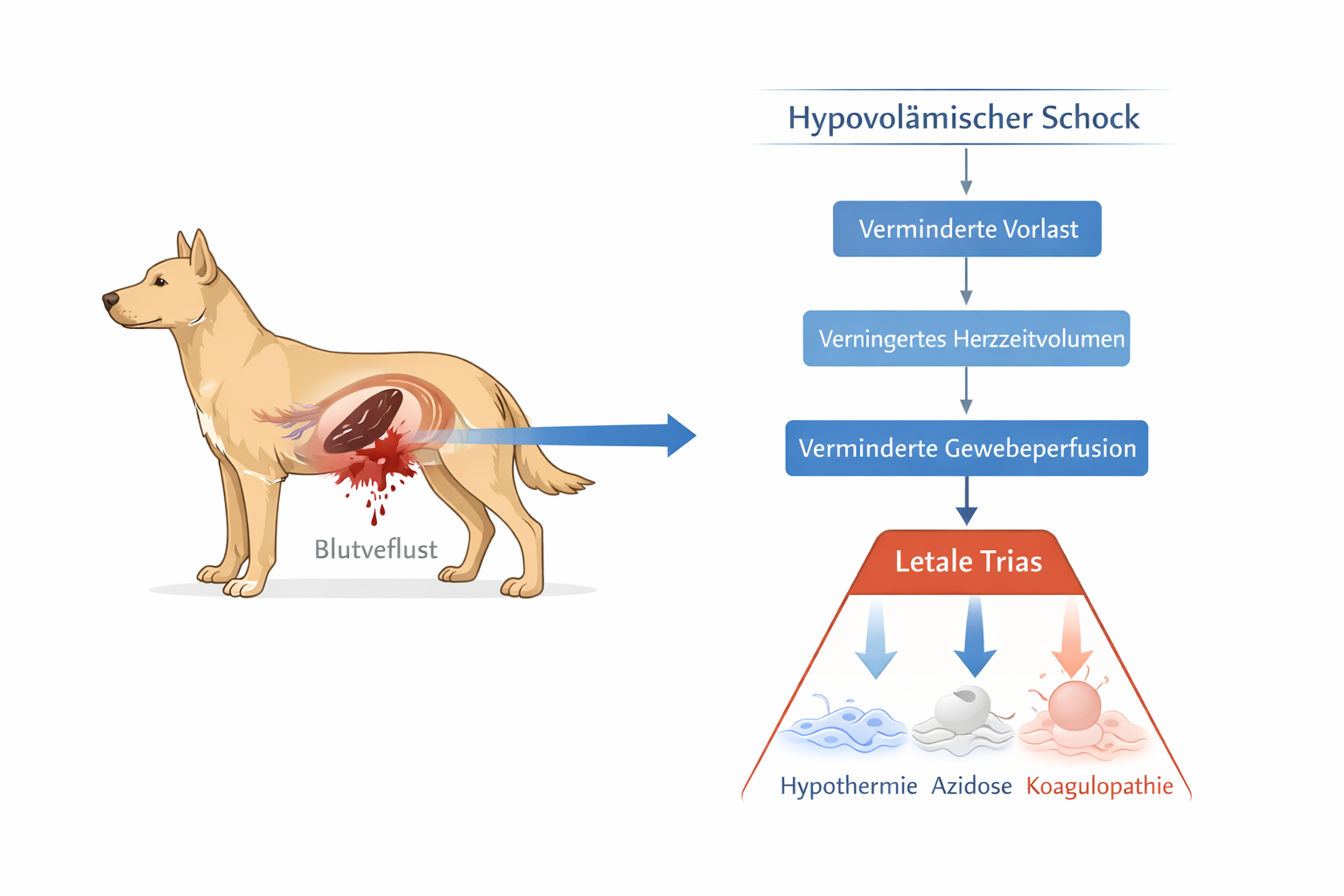
Ziel: „Time to definitive care“ verkürzen – das ist Teil der Therapie.
Der hypovolämische Schock ist in der präklinischen Tierrettung die häufigste und zugleich klinisch bedeutsamste Schockform im Kontext von Trauma, inneren Blutungen oder schwerer Dehydratation. Pathophysiologisch beruht er auf einem absoluten Verlust des intravasalen Volumens. Dieser Volumenverlust kann akut durch äußere oder innere Blutungen entstehen oder subakut durch Flüssigkeitsdefizite, etwa infolge massiver gastrointestinaler Verluste. Entscheidend ist, dass die zirkulierende Blutmenge nicht mehr ausreicht, um eine adäquate Vorlast und damit ein ausreichendes Schlagvolumen zu gewährleisten.
Zu Beginn sinkt der venöse Rückstrom zum Herzen. Die reduzierte Ventrikelfüllung führt unmittelbar zu einer Abnahme des Schlagvolumens und somit des Herzzeitvolumens. Der Organismus reagiert mit einer ausgeprägten Aktivierung des sympathoadrenalen Systems. Herzfrequenz und Kontraktilität steigen, während periphere Gefäße vasokonstrigieren, um den systemischen Gefäßwiderstand zu erhöhen. Gleichzeitig werden Renin-Angiotensin-Aldosteron-System und ADH aktiviert, um Flüssigkeit im Gefäßsystem zu halten. Diese Mechanismen stabilisieren kurzfristig den arteriellen Blutdruck, können jedoch die zugrunde liegende Perfusionsstörung nicht kompensieren. Der Blutdruck kann in frühen Phasen noch im Referenzbereich liegen, obwohl die Mikrozirkulation bereits kompromittiert ist.
Klinisch äußert sich der kompensierte hypovolämische Schock typischerweise durch blasse oder graue Schleimhäute, verlängerte Rekapillarisierungszeit, Tachykardie und einen schwachen peripheren Puls. Kalte Akren sind Ausdruck der peripheren Vasokonstriktion. Tiere wirken häufig unruhig, angespannt oder schmerzreaktiv. Mit fortschreitendem Volumenverlust erschöpfen sich die Kompensationsmechanismen. Es folgen Apathie, Hypotonie, Kollaps und gegebenenfalls Bewusstlosigkeit. Hypotonie ist dabei meist ein Spätzeichen und darf nicht als Frühindikator missverstanden werden.
Besonders kritisch sind innere Blutungen, da sie äußerlich nicht erkennbar sind. Splenische oder hepatische Rupturen, retroperitoneale Blutungen bei Beckenfrakturen oder intrathorakale Blutverluste können innerhalb kurzer Zeit ein erhebliches Defizit verursachen. Ein Tier kann initial noch gehfähig und ansprechbar erscheinen, während die Blutung fortschreitet. Diese scheinbare Stabilität beruht auf einer effektiven, jedoch fragilen Kompensation durch Sympathikusaktivierung. Jede zusätzliche Belastung – Stress, Umlagerung, Transport – kann das Gleichgewicht abrupt kippen lassen.
Mit zunehmendem Blutverlust sinkt die Sauerstofflieferung in die Peripherie. Die Zellen wechseln von aerober Energiegewinnung zur anaeroben Glykolyse, wodurch Laktat akkumuliert und eine metabolische Azidose entsteht. Azidose beeinträchtigt die Myokardkontraktilität und reduziert die Gefäßreaktivität auf Katecholamine. Gleichzeitig verschlechtert sich die Gerinnungsfunktion. An diesem Punkt entwickelt sich die sogenannte „letale Trias“ des Traumas: Hypothermie, Azidose und Koagulopathie. Diese drei Faktoren verstärken sich gegenseitig und bilden einen selbstverstärkenden Kreislauf.
Hypothermie entsteht präklinisch leicht. Schockbedingte periphere Vasokonstriktion reduziert die Wärmeverteilung, während verminderte Stoffwechselaktivität die Wärmeproduktion senkt. Zusätzlich wirken Umgebungseinflüsse wie kalter Untergrund, Nässe oder Wind. Hypothermie hemmt enzymatische Gerinnungsreaktionen und verstärkt die Blutungsneigung. Die Koagulopathie resultiert nicht nur aus Verdünnung durch Flüssigkeitsverschiebungen, sondern auch aus Verbrauch von Gerinnungsfaktoren und endothelialer Schädigung. Mikrothromben können die Mikrozirkulation zusätzlich beeinträchtigen, sodass trotz Makrostabilisierung weiterhin ischämische Gewebeareale bestehen.
Die präklinische Konsequenz ist eindeutig: Blutungskontrolle hat höchste Priorität. Sichtbare Blutungen werden mittels Druckverband oder – bei geeigneter Indikation – Tourniquet versorgt. Tiefe Wunden können tamponiert werden. Gleichzeitig ist konsequenter Wärmeerhalt essenziell, um die letale Trias zu unterbrechen. Sauerstoffgabe unterstützt die Maximierung des arteriellen Sauerstoffgehalts. Stressreduktion und zügiger Transport sind zentrale Maßnahmen, da die definitive Blutungskontrolle in der Regel chirurgisch erfolgen muss. Bei Verdacht auf innere Blutung ist die Zeit bis zur operativen Versorgung prognoseentscheidend. Eine übermäßige Vor-Ort-Diagnostik ohne therapeutische Konsequenz verschlechtert die Überlebenschancen.
Die Unterscheidung zwischen Makro- und Mikrozirkulation bleibt auch beim hypovolämischen Schock bedeutsam. Ein tastbarer Puls oder ein noch akzeptabler systolischer Druck schließen eine kritische Kapillarperfusionsstörung nicht aus. Die Beurteilung der Schleimhäute hinsichtlich Farbe und Feuchtigkeit sowie die Messung der Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Qualität der Gewebeperfusion. Wiederholte Reevaluation im Minutenabstand erhöht die diagnostische Sicherheit erheblich. Trendbeobachtungen sind aussagekräftiger als Einzelwerte.
Gerade bei Hund und Katze können Stress und Schmerz Herz- und Atemfrequenz beeinflussen, ohne dass die zugrunde liegende Perfusionsstörung beseitigt wäre. Eine stressbedingte Tachykardie darf nicht als Zeichen hämodynamischer Stabilität interpretiert werden. Ebenso kann eine scheinbare Beruhigung Ausdruck beginnender Dekompensation sein. Die präklinische Einschätzung erfordert daher stets die Integration aller klinischen Parameter in ein konsistentes Gesamtbild.
Eine klare Begrifflichkeit erleichtert die Kommunikation im Team: Ursache (z. B. hämorrhagisch), Stadium (kompensiert oder dekompensiert), Prioritäten (Blutungskontrolle, Wärmeerhalt, Oxygenierung) und Transportziel müssen eindeutig benannt werden. Jede Maßnahme wird mit einer Reevaluation verknüpft: Verbessert sich die Rekapillarisierungszeit? Wird der Puls kräftiger? Verändert sich die mentale Reaktion? Diese strukturierte Vorgehensweise reduziert das Risiko, kritische Dynamiken zu übersehen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies, sekundäre Schäden zu begrenzen und den Patienten so rasch wie möglich einer Einrichtung zuzuführen, die chirurgische Blutungskontrolle und intensivmedizinische Stabilisierung leisten kann. Ein scheinbar stabiler Zustand darf nicht zu trügerischer Sicherheit führen; die Kompensation kann jederzeit in eine rasche Dekompensation übergehen.
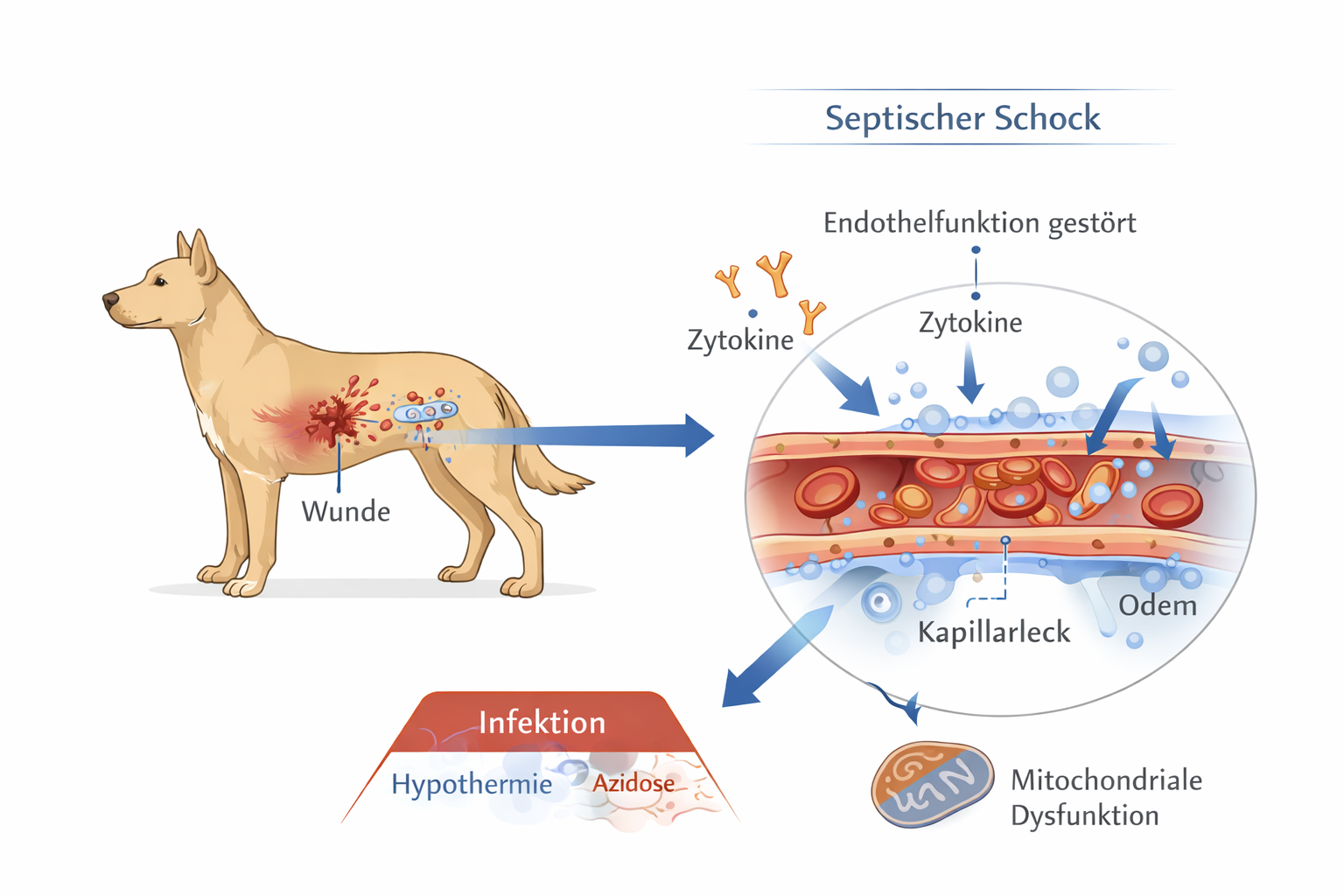
Merksatz: „Warme Extremitäten“ schließen kritische Mikrozirkulationsstörung nicht aus.
Der distributive Schock umfasst Zustände, bei denen das Gesamtvolumen im Organismus nicht primär fehlt, der Gefäßtonus und die intravasale Verteilung jedoch so gestört sind, dass das effektive zirkulierende Volumen abnimmt und die Gewebeperfusion zusammenbricht. Im Gegensatz zum hypovolämischen Schock steht nicht der absolute Volumenverlust am Beginn, sondern eine ausgeprägte Vasodilatation mit Fehlverteilung des Blutflusses („Maldistribution“) und häufig zusätzlich ein Kapillarleck, das sekundär zu einer relativen und absoluten Hypovolämie führt. Klinisch ist entscheidend, dass auch bei scheinbar ausreichendem oder sogar erhöhtem Herzzeitvolumen die Mikrozirkulation und die Sauerstoffextraktion im Gewebe schwer gestört sein können. Typische Formen in der Tiernotfallmedizin sind der anaphylaktische und der septische Schock; seltener treten neurogene Mechanismen oder toxische Vasoplegie als Auslöser in den Vordergrund.
Anaphylaktischer Schock: Beim anaphylaktischen Schock handelt es sich um eine akute, systemische Hypersensitivitätsreaktion, die häufig IgE-vermittelt abläuft. Nach Allergenexposition kommt es zur Mastzell- und Basophilen-Degranulation mit Freisetzung von Mediatoren wie Histamin, Leukotrienen, Prostaglandinen und weiteren vasoaktiven Substanzen. Diese führen zu einer generalisierten Vasodilatation, erhöhter Kapillarpermeabilität (Kapillarleck) und häufig zu Bronchokonstriktion sowie Schleimhautödem. Pathophysiologisch resultiert daraus eine rasche Reduktion des venösen Rückstroms (Vorlastabfall) durch Vasodilatation und Flüssigkeitsverschiebung ins Interstitium, während gleichzeitig die Atemwege durch Ödeme oder Bronchospasmus bedroht sein können. Klinisch können innerhalb von Minuten Schwäche, Kollaps, Tachykardie, Hypotonie, Erbrechen, Durchfall, Hypersalivation, Urtikaria, pruritische Hautreaktionen sowie Dyspnoe auftreten. Bei Hund und Katze ist das Erscheinungsbild variabel: Bei Hunden stehen nicht selten gastrointestinale Symptome und Kreislaufversagen im Vordergrund, während bei Katzen respiratorische Symptome (Bronchokonstriktion, Dyspnoe) stärker betont sein können. Präklinisch muss deshalb stets beides konsequent adressiert werden: Kreislaufstabilisierung und Atemwegssicherung/Oxygenierung, wobei eine rasche Verschlechterung jederzeit möglich ist.
Septischer Schock: Beim septischen Schock liegt eine systemische Infektion mit dysregulierter Immunantwort zugrunde. Pathogenassoziierte Muster (PAMPs) und körpereigene Gefahrensignale (DAMPs) aktivieren über Toll-like-Rezeptoren und andere Sensoren eine Zytokin- und Komplementkaskade. Das Endothel verliert dabei seine Barrierefunktion: Glykokalyx und Tight Junctions werden geschädigt, die Kapillarpermeabilität steigt (Kapillarleck), und es entsteht eine funktionelle Hypovolämie trotz möglicherweise normaler Gesamtkörperflüssigkeit. Parallel entwickelt sich eine ausgeprägte Vasoplegie, bei der die Gefäßmuskulatur auf körpereigene Katecholamine vermindert anspricht (Katecholamin-Refraktärität). Zusätzlich kommt es zu einer tiefgreifenden Störung der Mikrozirkulation: Mikrothromben, endotheliale Dysfunktion und regionale Flussumverteilungen führen zu einer Perfusionsheterogenität, bei der einzelne Kapillargebiete überperfundiert und andere vollständig ischämisch sind. Diese Konstellation erklärt, warum ein „normaler“ oder sogar hyperdynames Kreislauf (frühes, hyperdynamisches Stadium mit hohem Herzzeitvolumen und warmen Extremitäten) die Gewebeoxygenierung keineswegs garantiert. Hinzu kommt, dass die mitochondriale Sauerstoffverwertung beeinträchtigt sein kann („zytopathische Hypoxie“): Sauerstoff wird zwar geliefert, kann aber nicht mehr effizient in ATP umgewandelt werden. Das erhöht das Risiko irreversibler Zellschäden und Multiorganversagen, selbst wenn makrozirkulatorische Parameter vorübergehend günstig erscheinen.
Diagnostisch zeigen Tiere im septischen Schock häufig Tachykardie, Tachypnoe, veränderte Schleimhautfarbe und fortschreitende mentale Veränderungen. Fieber kann auftreten, ist aber nicht obligat; ebenso sind Hypothermie und eine „unangemessene“ Temperatur (kühl trotz Infektion) klinisch hochrelevant und prognostisch ungünstig. Schleimhäute können initial gerötet und feucht wirken („warm shock“), später marmoriert, grau oder blass werden („cold shock“) – insbesondere bei Katzen kann die Präsentation subtil sein, während eine rasche Dekompensation möglich bleibt. Präklinisch ist es didaktisch und operativ wichtig, bei entsprechenden Zeichen nicht nur „Schock“ zu erkennen, sondern die Ursache zu antizipieren: Bissverletzungen mit Abszessbildung, Pyometra, gastrointestinale Perforation, Aspiration, schwere Parodontitis, Harnwegsinfektion im Kontext einer Obstruktion oder andere septische Herde müssen als Auslöser mitgedacht werden, weil sie die Wahl des Transportziels und die Dringlichkeit der Voranmeldung bestimmen.
Ein entscheidendes Merkmal des distributiven Schocks ist seine häufig kombinierte Pathophysiologie. In der klinischen Realität handelt es sich selten um „reine“ Vasodilatation. Vielmehr treffen mehrere Komponenten zusammen: (1) relative Hypovolämie durch Vasodilatation und Pooling, (2) absolute Hypovolämie durch Kapillarleck und Flüssigkeitsverlust ins Interstitium, (3) inflammationsbedingte Myokarddepression mit reduziertem Schlagvolumen und (4) mikroangiopathische Störungen mit Gerinnungsaktivierung und Mikothromben. Diese Kombination führt zu wechselnden klinischen Stadien, die von „warm und tachykard“ bis „kalt, marmoriert und hypotensiv“ reichen können. Deshalb ist die präklinische Versorgung nicht auf eine Einzelmaßnahme reduzierbar, sondern muss als Bündel verstanden werden, das parallel Vitalfunktionen sichert, sekundäre Schäden begrenzt und die definitive Therapie vorbereitet.
Präklinisch bleibt das ABCDE-Vorgehen die Leitstruktur: Atemweg beurteilen und sichern, Oxygenierung optimieren, Kreislaufzeichen engmaschig bewerten, neurologischen Status einschätzen und eine vollständige, aber zielgerichtete Exposition durchführen, ohne Wärmeverlust zu provozieren. Der Wärmeerhalt ist beim distributiven Schock besonders bedeutsam, da Hypothermie die Kreislaufkompensation, die Gerinnungsfähigkeit und die Wirksamkeit von Medikamenten beeinträchtigen kann. Schon geringe Auskühlung verschlechtert die Prognose, insbesondere bei septischen Patienten mit Kapillarleck und eingeschränkter Thermoregulation. Praktisch bedeutet das: konsequente Isolierung vom Boden, Abdeckung, Minimierung unnötiger Manipulationen, und frühzeitiger, priorisierter Transport.
Die präklinische Diagnostik zielt auf rasche Risikoabschätzung, nicht auf endgültige Ursachenklärung. Die Aussagekraft steigt erheblich, wenn relevante Zeichen wiederholt erhoben und als Trends dokumentiert werden. Schleimhautfarbe, Feuchtigkeit, Rekapillarisierungszeit, Pulsqualität, Atemarbeit, Temperatur und mentale Lage bilden in Kombination ein robustes Bild des Perfusionszustands. Einzelwerte – etwa eine einmalige Blutdruckmessung – können beim distributiven Schock irreführend sein, da Vasoplegie und Messartefakte die Interpretation erschweren. Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verschieben, ohne dass die zugrunde liegende Perfusionsstörung aufgehoben wäre. Ein klinisch scheinbar stabiler Zustand kann daher eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert.
Für den Teamerfolg ist eine saubere Begrifflichkeit zentral. Ursache (Verdacht auf Anaphylaxie vs. Sepsis), Schockform, Schockstadium, Hauptbedrohung (Atemweg vs. Perfusion) sowie Prioritäten und Transportziel müssen klar benannt werden. Strukturierte Kommunikation mit der Zielklinik ist essenziell, um definitive Therapie ohne Verzögerung zu ermöglichen: bei Sepsis z. B. frühzeitige Antibiotikagabe, chirurgische Herdsanierung, Vasopressoren und Intensivmonitoring; bei Anaphylaxie ggf. Atemwegsmanagement, antiinflammatorische und antiallergische Therapie sowie enges Kreislaufmonitoring. Die Voranmeldung sollte daher nicht nur „Schock“ melden, sondern Verdachtsdiagnose, Verlauf, Trends und bereits durchgeführte Maßnahmen in kompakter Form übermitteln. Ziel der präklinischen Phase ist, Vitalfunktionen zu sichern, Wärmeverlust zu vermeiden, den Transport zu priorisieren und die Übergabe so vorzubereiten, dass die Klinik nahtlos weiterbehandeln kann.
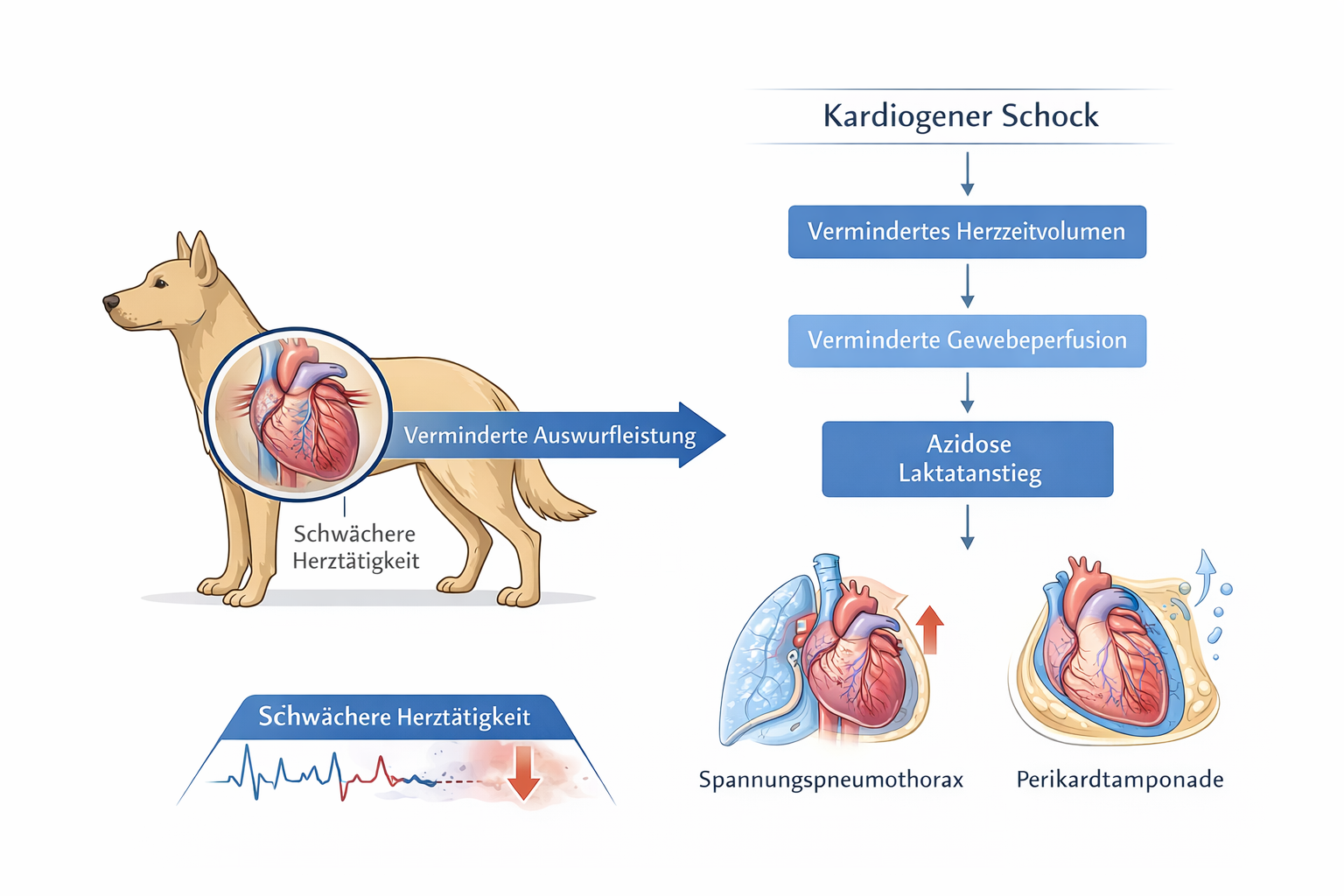
Kardiogener und obstruktiver Schock unterscheiden sich in ihrer Pathophysiologie grundlegend von hypovolämischen oder distributiven Formen. Das primäre Problem liegt weder im absoluten Volumenmangel noch im Gefäßtonus, sondern in der unzureichenden Pumpleistung des Herzens oder in einer mechanischen Behinderung der kardialen Füllung beziehungsweise des Auswurfs. In beiden Fällen resultiert ein vermindertes Herzzeitvolumen mit konsekutiver Reduktion des effektiven Sauerstoffangebotes an die Gewebe. Für die präklinische Einschätzung ist entscheidend, die mechanische Logik zu verstehen: Wenn das Herz nicht ausreichend pumpen kann oder sich nicht ausreichend füllen darf, wird eine rein volumenorientierte Therapie wirkungslos oder sogar schädlich.
Kardiogener Schock: Beim kardiogenen Schock ist die myokardiale Kontraktilität oder das rhythmische Pumpmuster so beeinträchtigt, dass das Herzzeitvolumen nicht mehr ausreicht, um eine adäquate Organperfusion sicherzustellen. Ursachen können schwere Tachyarrhythmien (z. B. ventrikuläre Tachykardie), hochgradige Bradyarrhythmien (z. B. AV-Block III°), akute Myokarditis, dekompensierte dilatative oder hypertrophe Kardiomyopathie sowie akute Klappeninsuffizienzen sein. Pathophysiologisch führt die reduzierte Schlagleistung zu einem Rückstau im venösen System und zu einer Minderdurchblutung peripherer Organe. Klinisch zeigen sich häufig schwache Pulse, verlängerte Rekapillarisierungszeit, kalte Extremitäten und Zeichen der Hypoperfusion. Gleichzeitig können pulmonale Stauungszeichen wie Dyspnoe, Tachypnoe oder Rasselgeräusche bei Lungenödem auftreten.
Ein zentrales klinisches Problem besteht darin, dass aggressive Volumengaben bei kardiogenem Schock die Situation verschlechtern können. Durch die eingeschränkte Pumpfunktion steigt der hydrostatische Druck im Lungenkreislauf, was die Entwicklung oder Progression eines Lungenödems begünstigt. Die Folge sind zunehmende Dyspnoe und Hypoxämie, die wiederum die Myokardfunktion weiter beeinträchtigen. Präklinisch bedeutet dies, dass eine Volumentherapie nur mit großer Zurückhaltung erfolgen darf und die Priorität auf Oxygenierung, Stressreduktion und raschem Transport liegt. Jede Manipulation muss so schonend wie möglich erfolgen, da Stress und Katecholaminanstieg Arrhythmien verstärken können.
Obstruktiver Schock: Der obstruktive Schock entsteht durch eine mechanische Behinderung des venösen Rückstroms oder des kardialen Auswurfs. Klassische Ursachen sind der Spannungspneumothorax, die Perikardtamponade oder – seltener präklinisch diagnostizierbar – die massive Lungenembolie. Beim Spannungspneumothorax erhöht sich der intrathorakale Druck so stark, dass große Venen komprimiert werden. Die Vorlast sinkt abrupt, das Herzzeitvolumen fällt ab, und es entwickelt sich rasch eine Kreislaufinstabilität. Klinisch zeigen sich akute Dyspnoe, reduzierte Thoraxexkursion, häufig einseitig abgeschwächte oder fehlende Atemgeräusche sowie Tachykardie und Hypotonie. Zyanose und Agitation können hinzukommen.
Die Perikardtamponade beruht auf einer Flüssigkeitsansammlung im Herzbeutel, die die diastolische Füllung mechanisch behindert. Auch hier sinkt die Vorlast trotz unverändertem Gesamtvolumen. Typische Zeichen können gedämpfte Herztöne, schwache Pulse und eventuell juguläre Stauung sein, wobei diese Befunde beim Tier oft subtil oder schwer zu interpretieren sind. Eine massive Lungenembolie blockiert den pulmonalen Kreislauf, erhöht die rechtsventrikuläre Nachlast und führt sekundär zu einem Abfall des linksventrikulären Auswurfs. Die Differenzierung dieser Ursachen ist präklinisch oft nicht sicher möglich; entscheidend ist das Erkennen der mechanischen Problematik und die Priorisierung des Transports.
Didaktisch zentral ist das Verständnis, dass „mehr Druck“ oder „mehr Volumen“ bei mechanischer Obstruktion nicht die Ursache beseitigt. Wenn Blut nicht zum Herzen zurückkehren kann oder das Herz sich nicht füllen darf, muss die Obstruktion entlastet werden. Eine Notfallentlastung bei Spannungspneumothorax ist eine fortgeschrittene Maßnahme und darf nur bei entsprechender Ausbildung und Ausrüstung durchgeführt werden. In allen anderen Fällen stehen Sauerstoffgabe, stressarme Lagerung, Minimierung von Manipulationen und schnellstmöglicher Transport in eine geeignete Einrichtung im Vordergrund.
Mischformen sind insbesondere im Trauma häufig. Ein Tier kann gleichzeitig einen hypovolämischen Schock durch Blutverlust, einen obstruktiven Schock durch Pneumothorax und eine distributive Komponente infolge inflammatorischer Reaktion entwickeln. Daher ist die wiederholte strukturierte Reevaluation wichtiger als das Festhalten an einer einmal gestellten Schockform-Hypothese. Jede Verschlechterung von Atemarbeit, Pulsqualität oder mentaler Lage muss als Hinweis auf eine dynamische Veränderung interpretiert werden.
Für die präklinische Einschätzung bleibt die Integration aller Befunde entscheidend. Die Unterscheidung zwischen Makrozirkulation (Blutdruck, Puls, Herzzeitvolumen) und Mikrozirkulation (Kapillardurchfluss, Sauerstoffextraktion, Endothelfunktion) hilft, Fehleinschätzungen zu vermeiden. Schleimhautfarbe, Feuchtigkeit und Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Perfusionsqualität. Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verändern, ohne dass die zugrunde liegende Perfusionsstörung behoben wäre. Ein scheinbar stabiler Zustand kann eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert.
Wärmeerhalt ist auch bei kardiogenem und obstruktivem Schock integraler Bestandteil der Versorgung. Hypothermie verschlechtert die Myokardfunktion, beeinflusst die Gerinnung und kann Arrhythmien begünstigen. Schonende Lagerung, Minimierung von Stress und eine ruhige Umgebung sind insbesondere bei kardial vorbelasteten Tieren essenziell. Jede unnötige Manipulation kann die hämodynamische Situation destabilisieren.
Eine präzise Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. Pneumothorax, HCM-Dekompensation), Schockform (kardiogen oder obstruktiv), Stadium, Prioritäten (Atemweg, Oxygenierung, Entlastung, Transport) und Transportziel müssen klar benannt werden. Die Aussagekraft steigt erheblich, wenn Befunde wiederholt erhoben und Trends dokumentiert werden. Einzelwerte dürfen nicht isoliert interpretiert werden, sondern müssen im Kontext des Gesamtbildes stehen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies, die Ursache zu antizipieren, sekundäre Schäden zu vermeiden und den Patienten rasch einer Einrichtung zuzuführen, die definitive diagnostische und therapeutische Maßnahmen durchführen kann. Die Qualität der Versorgung bemisst sich dabei an der strukturierten Reevaluation, der klaren Kommunikation und der konsequenten Priorisierung lebensrettender Schritte.
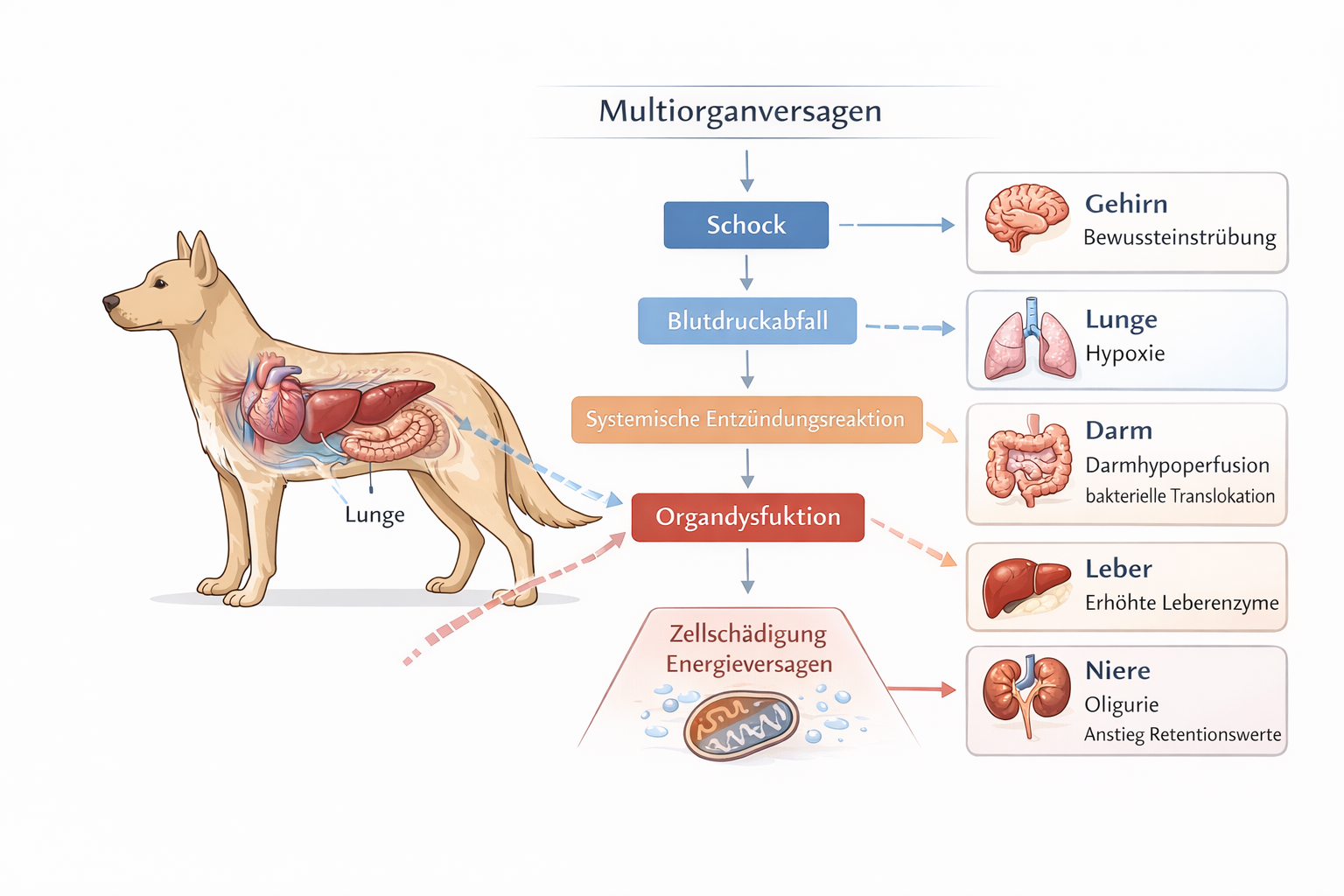
Ziel: Progression in die irreversible Phase verhindern durch frühe Stabilisierung.
Das Multiorganversagen (Multiple Organ Dysfunction Syndrome, MODS) stellt die Endstrecke eines anhaltenden oder wiederkehrenden Schockgeschehens dar und ist Ausdruck einer fortschreitenden systemischen Dysregulation. Es entsteht nicht abrupt, sondern entwickelt sich als dynamischer Prozess infolge kombinierter Hypoperfusion, inflammatorischer Fehlsteuerung, endothelialer Schädigung und zellulärem Energiemangel. Pathophysiologisch ist MODS das Resultat eines Missverhältnisses zwischen Sauerstoffangebot und -verwertung, das über einen kritischen Zeitraum persistiert. Jede Episode von Hypotonie, Hypoxie, Hypothermie oder unkontrollierter Blutung erhöht die Wahrscheinlichkeit, dass kompensatorische Mechanismen erschöpfen und Organsysteme in eine funktionelle Dekompensation übergehen.
Frühe Organfunktionsstörungen sind häufig subtil und werden leicht übersehen. Die Niere reagiert besonders empfindlich auf Durchblutungsmangel. Bereits kurze Phasen reduzierter Perfusion können eine akute Nierenfunktionsstörung initiieren. Klinisch zeigt sich zunächst eine abnehmende Harnproduktion (Oligurie), die präklinisch nur indirekt über Anamnese (kein Urinabsatz), trockene Schleimhäute oder Zeichen der Dehydratation erfasst werden kann. Persistiert die Minderperfusion, droht ein akutes Nierenversagen mit Elektrolytverschiebungen und metabolischer Entgleisung.
Die Leber verliert bei anhaltender Hypoperfusion ihre zentrale Rolle in Entgiftung, Metabolismus und Synthese. Gerinnungsfaktoren werden vermindert gebildet, toxische Metabolite akkumulieren, und die Glukosehomöostase kann gestört sein. In Kombination mit systemischer Inflammation entsteht eine komplexe Koagulopathie, die sowohl Blutungsneigung als auch Mikrothrombenbildung begünstigt. Diese Mikrothromben verschlechtern wiederum die Mikrozirkulation und verstärken die Organischämie.
Die Lunge ist durch ihre ausgedehnte Kapillaroberfläche besonders anfällig für endotheliale Schädigung. Kapillarleck und inflammatorische Prozesse führen zu einem ARDS-ähnlichen Bild mit interstitieller und alveolärer Flüssigkeitsansammlung. Der Gasaustausch wird zunehmend ineffektiv. Klinisch manifestiert sich dies durch Tachypnoe, steigenden Sauerstoffbedarf, Dyspnoe und im Spätstadium Zyanose. Selbst bei scheinbar stabilen Blutdruckwerten kann die Sauerstoffversorgung der Gewebe kritisch reduziert sein.
Das zentrale Nervensystem reagiert sensibel auf globale Perfusionsveränderungen. Frühe Zeichen sind Unruhe, Desorientierung oder veränderte Reaktionslage. Im weiteren Verlauf folgen Apathie, reduzierte Bewusstseinslage bis hin zum Koma. Diese neurologischen Veränderungen sind häufig ein Spiegel der globalen zerebralen Perfusion und sollten als Warnsignal für eine systemische Verschlechterung verstanden werden.
Eine Schlüsselrolle im Prozess des MODS spielt das Endothel. Die Schädigung der endothelialen Glykokalyx führt zu erhöhter Gefäßpermeabilität, interstitieller Flüssigkeitsverschiebung und Verlust der Barrierefunktion. Gleichzeitig entsteht eine prokoagulatorische Oberfläche, die Mikrothromben begünstigt und die Perfusionsheterogenität verstärkt. Selbst wenn makrozirkulatorische Parameter – etwa Blutdruck oder Herzfrequenz – vorübergehend normal erscheinen, kann die Mikrozirkulation weiterhin gestört bleiben. Hinzu kommt eine mögliche mitochondriale Dysfunktion: Trotz ausreichender Sauerstofflieferung gelingt die ATP-Produktion nicht mehr effizient („zytopathische Hypoxie“). Dadurch persistiert die Organfunktionsstörung auch nach scheinbarer Kreislaufstabilisierung.
Didaktisch ist entscheidend, MODS als Prozess zu verstehen, nicht als singuläres Ereignis. Jede Phase unzureichender Perfusion erhöht das Risiko irreversibler Zellschäden. Zeitmanagement wird damit selbst zur medizinischen Intervention. Rasche, strukturierte Entscheidungen und frühzeitige Übergabe in eine intensivmedizinisch ausgestattete Einrichtung sind pathophysiologisch begründet. Je länger Hypoperfusion und Inflammation unkontrolliert bestehen, desto geringer wird die Reversibilität.
Für die Präklinik ergeben sich daraus klare Prinzipien: Schock frühzeitig erkennen, Oxygenierung konsequent sichern, Wärmeerhalt gewährleisten und zusätzliche Stressoren vermeiden. Hypothermie verschlechtert Gerinnung, Myokardfunktion und Medikamentenwirkung und begünstigt die Progression zum Multiorganversagen. Ebenso muss jede vermeidbare Verzögerung minimiert werden. Eine strukturierte Reevaluation entlang eines festen Schemas reduziert das Risiko, kritische Veränderungen zu übersehen.
Die Unterscheidung zwischen Makro- und Mikrozirkulation bleibt auch im Kontext von MODS zentral. Ein „normaler“ Blutdruck bedeutet nicht zwangsläufig adäquate Gewebeoxygenierung. Schleimhautfarbe, Feuchtigkeit und Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Perfusionsqualität und den sympathischen Tonus. Die Aussagekraft steigt erheblich, wenn diese Zeichen wiederholt erhoben und im Verlauf dokumentiert werden. Trendbeobachtungen sind aussagekräftiger als isolierte Einzelmessungen.
Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verändern, ohne die zugrunde liegende Perfusionsstörung zu beheben. Ein klinisch scheinbar stabiler Zustand kann daher eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert. Die präklinische Einschätzung erfordert stets die Integration aller Befunde in ein konsistentes Gesamtbild. Einzelwerte dürfen nicht isoliert interpretiert werden.
Eine klare Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. Trauma, Sepsis), Schockform, Stadium, betroffene Organsysteme, Prioritäten und Transportziel müssen eindeutig benannt werden. Jede Intervention wird mit einer Reevaluation verknüpft: Verbessern sich mentale Lage, Atemarbeit oder Perfusionszeichen? Bleiben kritische Parameter bestehen? Diese strukturierte Vorgehensweise erhöht die Handlungssicherheit und unterstützt die klinische Kontinuität.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Wird dieses Gleichgewicht nicht rechtzeitig wiederhergestellt, entwickelt sich aus der zunächst reversiblen Organdysfunktion ein irreversibles Multiorganversagen. Die präklinische Phase ist daher ein entscheidender Zeitabschnitt, in dem durch konsequente Stabilisierung, Wärmeschutz, Oxygenierung und priorisierten Transport die Weichen für Prognose und Überleben gestellt werden.
Merksatz: „Intervention ohne Reevaluation“ ist unvollständig.
Präklinische Entscheidungslogik im Schockmanagement bedeutet, unter Zeitdruck und in einer hochdynamischen Lage innerhalb weniger Minuten belastbare Prioritäten zu setzen. Ziel ist nicht, vor Ort eine vollständige Diagnose zu „lösen“, sondern lebensbedrohliche Störungen früh zu erkennen, zu überbrücken und den Patienten so rasch wie möglich in eine geeignete Einrichtung zu überführen. In der Tiernotfallmedizin ist diese Logik besonders wichtig, weil Stress, Schmerz und Umgebungseinflüsse Vitalparameter verfälschen können und weil Schockzustände häufig anfangs kompensiert erscheinen. Der Rahmen für dieses Vorgehen ist das ABCDE-Schema, angepasst an die tiermedizinischen Besonderheiten und konsequent als zyklisches Arbeitsmodell verstanden: beurteilen – intervenieren – erneut beurteilen.
A – Airway (Atemweg): Im ersten Schritt wird geprüft, ob der Atemweg frei und funktionell ist. Dazu gehört die Beurteilung von Schutzreflexen (Schlucken, Husten), das Risiko einer Aspiration sowie mögliche Obstruktionen durch Blut, Erbrochenes, Fremdkörper, Schwellungen oder Zungenlage. Tierartspezifisch relevant sind zudem Maulkorb- und Fixationsprobleme: Sicherungsmaßnahmen dürfen die Ventilation nicht behindern. Die Entscheidungslogik lautet hier: Ein unsicherer Atemweg gefährdet alle nachfolgenden Schritte, weil Hypoxie binnen kurzer Zeit zu Kreislaufkollaps und neurologischem Schaden führt. Deshalb hat die Sicherung eines freien Atemwegs Vorrang vor detaillierten Messungen oder Dokumentationsaufgaben.
B – Breathing (Atmung): Atmung wird nicht nur als Frequenz bewertet, sondern als Atemarbeit und Effektivität. Entscheidend sind Thoraxexkursion, Atemtiefe, Einsatz der Bauchpresse, Atemgeräusche (Stridor, rasselnde Geräusche), Hecheln außerhalb thermoregulatorischer Situationen, Zyanose und Zeichen von Luftnot. Bei Trauma muss früh an thorakale Ursachen gedacht werden (Pneumothorax, Hämatothorax, Lungenkontusion, Rippenverletzungen). Die präklinische Logik lautet: Eine „passable“ Kreislaufsituation nützt nichts, wenn die Ventilation mechanisch oder funktionell versagt. Daher darf bei akuter Dyspnoe der Fokus nicht ausschließlich auf Kreislaufzahlen liegen; Atemmechanik und Oxygenierung sind dann die zeitkritischen Determinanten.
C – Circulation (Kreislauf): Im Schockmanagement ist die Kreislaufbeurteilung primär eine Perfusionsbeurteilung. Pulsqualität (kräftig vs. fadenförmig), Pulsfrequenz, Schleimhautfarbe und -feuchtigkeit, Rekapillarisierungszeit (CRT), Temperatur der Extremitäten sowie offensichtliche Blutungsquellen stehen im Vordergrund. Hypotonie ist häufig ein Spätzeichen; frühere Hinweise sind Tachykardie, verlängerte CRT, blasse/graue Schleimhäute und kalte Akren. Gleichzeitig sind bei distributiven Zuständen auch gerötete Schleimhäute und „bounding pulses“ möglich. Die Entscheidungslogik lautet deshalb: Makrozirkulation (Druck, Puls) und Mikrozirkulation (Kapillarfluss, Sauerstoffextraktion) müssen gemeinsam bewertet werden. Ein einzelner Messwert – etwa ein scheinbar akzeptabler systolischer Blutdruck – schließt eine kritische Mikrozirkulationsstörung nicht aus. Sichtbare Blutungen werden sofort kontrolliert, weil Blutungskontrolle eine ursachennahe, lebensrettende Intervention ist. Bei Verdacht auf innere Blutung gilt: „Time to surgery“ ist prognoseentscheidend; die präklinische Phase muss Transportfähigkeit herstellen, nicht Diagnostik verlängern.
D – Disability (Neurologischer Status): Hier wird die Bewusstseinslage (wach, stuporös, komatös), die Reaktionsfähigkeit, das Schmerzverhalten und das Vorliegen von Krampfaktivität beurteilt. Neurologische Veränderungen sind häufig ein Spiegel globaler Perfusion und Oxygenierung. Die Entscheidungslogik lautet: Eine Verschlechterung des Bewusstseins ist ein Alarmzeichen, das die Prioritäten unmittelbar beeinflusst (z. B. erneute Prüfung von A/B, Intensivierung der Oxygenierung, beschleunigter Transport). Bei klinischem Verdacht auf Hypoglykämie kann eine Messung – sofern verfügbar – entscheidend sein; gleichzeitig darf sie nicht dazu führen, dass A/B/C verzögert werden. Schmerzmanagement ist präklinisch stets sorgfältig abzuwägen und an die vorhandene Qualifikation gebunden; unabhängig davon gilt: stressarme Handhabung reduziert Katecholaminbelastung und damit sekundäre Verschlechterungen.
E – Exposure/Environment (Exposition und Umgebung): Abschließend wird der Patient so weit entkleidet/inspektiert, dass relevante Verletzungen nicht übersehen werden, ohne unnötig Wärme zu verlieren. Gleichzeitig werden Umgebungsfaktoren aktiv gemanagt: Hypothermieprophylaxe, Schutz vor Nässe/Kälte, stabile Lagerung, Minimierung von Stressoren und sichere Transportvorbereitung. Die Entscheidungslogik lautet: Hypothermie ist keine „Nebenvariable“, sondern ein Treiber von Koagulopathie und Kreislaufversagen. Wärmeerhalt ist daher eine Therapie, nicht Komfortmaßnahme. Gerade im Schock ist Wärmeverlust schnell und prognostisch relevant.
Ein zentraler Grundsatz der präklinischen Entscheidungslogik ist die Einsicht, dass Schock in der Praxis selten „rein“ auftritt. Ein Trauma kann gleichzeitig hypovolämisch wirken (Blutung), obstruktiv (Pneumothorax/Thoraxdruck), distributiv (inflammatorische Antwort) und sekundär sogar kardiogen (Myokarddepression, Arrhythmien) werden. Die Konsequenz ist ein zyklisches Vorgehen: Nach jeder Intervention werden die Kernparameter erneut geprüft, um eine Trendbeurteilung zu ermöglichen. Damit wird der Fokus von der Momentaufnahme auf die Dynamik verschoben. Praktisch bedeutet das: Nach Sauerstoffgabe wird Atemarbeit und Schleimhautfarbe erneut bewertet; nach Wärmeschutz werden periphere Temperatur und mentale Lage kontrolliert; nach Druckverband werden Pulsqualität und CRT überprüft. Dieses „Intervention–Reevaluation“-Prinzip ist die wichtigste Sicherheitsbarriere gegen Fehleinschätzungen.
Didaktisch hilfreich ist die klare Trennung zwischen Erkennen und definitiv Behandeln. Präklinisch werden lebensbedrohliche Zustände überbrückt: Atemweg sichern, Oxygenierung optimieren, Blutung kontrollieren, Hypothermie verhindern, patientenschonend lagern und Transport organisieren. Definitive Diagnostik und kausale Therapie (Bildgebung, OP, Antibiotikaregime, Vasopressoren, Intensivmonitoring) liegen in der Regel in der Klinik. Diese Trennung schützt vor dem häufigsten Fehler im Schockmanagement: dem „Diagnostik-Sog“, bei dem vor Ort Zeit in Detailabklärungen investiert wird, ohne dass dadurch eine definitive Maßnahme möglich wird. Präklinische Exzellenz ist daher die Fähigkeit, diagnostische Hypothesen so weit zu formulieren, dass die richtige Klinik vorbereitet werden kann – nicht, die Hypothese vor Ort endgültig zu bestätigen.
Kommunikation ist im Schockmanagement ein medizinischer Bestandteil. Eine Voranmeldung an die Zielklinik ist besonders wertvoll, wenn sie strukturiert erfolgt und nicht nur „Schock“ als Etikett meldet. Relevant sind: Verdacht auf Schockform (hypovolämisch/distributiv/obstruktiv/kardiogen), Stadium (kompensiert vs. dekompensiert), wahrscheinliche Ursache (Trauma, Blutung, Sepsis, Anaphylaxie, kardiale Dekompensation), aktuelle klinische Schlüsselbefunde (Atemarbeit, Schleimhautfarbe, CRT, Pulsqualität, Temperatur, mentale Lage), durchgeführte Maßnahmen und – vor allem – Trends: Wird die CRT kürzer oder länger? Wird der Puls kräftiger oder fadenförmiger? Verbessert sich die Atemarbeit unter Sauerstoff? Diese Trendkommunikation erlaubt der Klinik, Ressourcen zu mobilisieren (OP, Intensivplatz, Bildgebung, Labor, Blutprodukte) und verringert Zeitverluste an der Schnittstelle.
Auch die interne Teamkommunikation folgt der Entscheidungslogik. Rollen und Aufgaben werden früh festgelegt (Teamleitung, Airway/O₂, Blutung/Verbände, Dokumentation/Kommunikation). Kurze, eindeutige Closed-Loop-Kommunikation reduziert Missverständnisse. Die Teamleitung steuert die Prioritäten, achtet auf das zyklische Reevaluationsprinzip und verhindert, dass sich das Team in Nebenaufgaben verliert. Gleichzeitig wird eine minimale, aber konsistente Dokumentation geführt: Zeitpunkte, Befunde, Maßnahmen, Reaktionen. Diese Dokumentation ist keine Bürokratie, sondern klinische Sicherheitsreserve, weil sie die Übergabe stützt und spätere Entscheidungen an Trends anknüpfen lässt.
Die präklinische Entscheidungslogik berücksichtigt außerdem typische Fallstricke. Erstens: „Gehfähig“ oder „wach“ schließt Schock nicht aus, weil kompensatorische Mechanismen beim Tier kurzfristig sehr effektiv sein können. Zweitens: Stress und Schmerz können Tachykardie und Tachypnoe verursachen, ohne dass Perfusion ausreichend ist; umgekehrt kann scheinbare Beruhigung eine beginnende Dekompensation anzeigen. Drittens: Blutdruckmessungen sind hilfreich, aber fehleranfällig und häufig spätpathologisch; deshalb werden sie immer in den Kontext von Pulsqualität, CRT, Schleimhäuten und mentaler Lage eingeordnet. Viertens: Bei akuter Dyspnoe nach Trauma muss früh an obstruktive Ursachen gedacht werden; ein „falscher“ Fokus auf Kreislaufzahlen ohne Beachtung der Atemmechanik kostet lebensbedrohliche Minuten.
Zusammengefasst ist präklinische Qualität im Schockmanagement die Summe aus strukturiertem Denken, sauberer Beobachtung, zeitkritischer Priorisierung und klarer Kommunikation. Das ABCDE-Schema liefert die Prioritäten, die zyklische Reevaluation liefert die Sicherheit, und die konsequente Trennung von Überbrückung und definitiver Therapie verhindert Verzögerungen. Wer diese Logik beherrscht, schafft die entscheidende Brücke zwischen Einsatzort und Klinik: Der Patient wird nicht „diagnostiziert“, sondern stabilisiert, richtig zugeordnet und ohne Zeitverlust in definitive Versorgung überführt.
Hinweis: Single-Choice (jeweils eine richtige Antwort). Bestehensgrenze: 70%.
Ziel: in kurzer Zeit korrekte Prioritäten setzen. Die Simulation bewertet Kernentscheidungen (Oxygenierung, Blutungskontrolle, Wärmeschutz, Transport).
Merksatz: „Transport ist Therapie“, wenn definitive Maßnahmen nur in der Klinik möglich sind.
Ausbildungsplattform (Tier-Notruf)
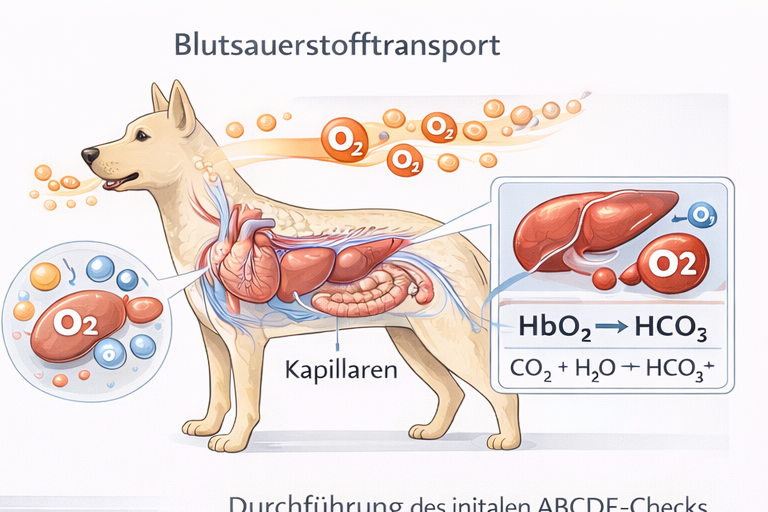
Ziel: in Sekunden eine belastbare Priorität (kritisch/stabil) und Risikoabschätzung erstellen.
Kapitel 1 bildet die systematische Grundlage der Ausbildung in der präklinischen Tierrettung und definiert die fachlichen, organisatorischen sowie rechtlichen Rahmenbedingungen für ein sicheres und effektives Vorgehen. Im Zentrum steht die strukturierte Notfallkette, die sich in die Abschnitte Alarmierung, Einsatzvorbereitung, Eigensicherung, Erstbeurteilung, Stabilisierung, Transportorganisation und qualifizierte Übergabe gliedert. Diese Abfolge ist nicht zufällig, sondern folgt einer prioritätenorientierten Logik, die sicherstellt, dass vitale Gefährdungen frühzeitig erkannt und adressiert werden. Die konsequente Einhaltung dieser Struktur ist im Einsatzalltag bedeutsamer als die isolierte Optimierung einzelner Parameter.
Bereits die Notrufannahme beeinflusst maßgeblich die Qualität des weiteren Einsatzverlaufs. Eine strukturierte Abfrage reduziert Informationsverluste und schafft ein belastbares Lagebild. Wesentliche Parameter sind Tierart, Rasse oder Größe, geschätztes Gewicht, exakter Einsatzort, Zugänglichkeit, aktuelle Gefahrenlage, Bewusstseinszustand, Atmungsmuster, sichtbare Blutungen, vorbestehende Erkrankungen sowie besondere Verhaltensmerkmale. Ziel ist es, innerhalb kurzer Zeit eine einsatztaktische Einschätzung vorzunehmen, geeignete Ressourcen zu disponieren und potenzielle Risiken für Einsatzkräfte und Tier frühzeitig zu identifizieren. Unklare oder unvollständige Informationen erhöhen die Wahrscheinlichkeit taktischer Fehlentscheidungen und können zu Verzögerungen in der Versorgung führen.
Die Eigensicherung besitzt oberste Priorität und ist integraler Bestandteil jeder Einsatzphase. Gefahren ergeben sich typischerweise aus dem Straßenverkehr, unübersichtlichen Unfallstellen, aggressiven oder panischen Tieren, emotional stark belasteten Tierhaltern oder instabilen baulichen Situationen. Auch infektiologische Risiken oder Exposition gegenüber Gefahrstoffen sind zu berücksichtigen. Eine strukturierte Gefahrenanalyse vor Betreten der Einsatzstelle, das Tragen geeigneter persönlicher Schutzausrüstung sowie klare Teamkommunikation sind essenziell. Eine unzureichende Eigensicherung gefährdet nicht nur das Team, sondern kann den gesamten Rettungsablauf unterbrechen und die Patientenversorgung erheblich verzögern.
Der strukturierte Erstcheck dient der raschen Identifikation vital bedrohlicher Störungen und folgt dem Grundsatz „treat first what kills first“. Zunächst werden Bewusstsein, Atemwegssituation, Atmung und Kreislauf beurteilt. Zeichen einer Atemwegsverlegung, respiratorischen Insuffizienz oder massiven Blutung haben höchste Priorität. Ergänzend werden Schleimhautfarbe, Kapillarfüllungszeit, Pulsqualität, Herzfrequenz und Körpertemperatur erhoben. Ziel ist nicht die vollständige Diagnosestellung, sondern die sofortige Erkennung von Zuständen, die ohne unmittelbare Intervention zum Tod führen können. Sobald eine lebensbedrohliche Abweichung identifiziert wird, erfolgt die unmittelbare Maßnahme, bevor weiterführende Differenzierungen vorgenommen werden.
Die Stabilisierung umfasst alle präklinisch verfügbaren Maßnahmen zur Sicherung vitaler Funktionen. Hierzu zählen Atemwegssicherung und Oxygenierung, kontrollierte Blutungskontrolle mittels Druckverband oder Tourniquet bei geeigneter Indikation, Volumenstabilisierung im Rahmen der verfügbaren Mittel, Wärmeerhalt zur Prävention oder Behandlung einer Hypothermie sowie eine schonende, stressreduzierte Lagerung. Bei Hund und Katze ist zu berücksichtigen, dass Stress und Schmerz erhebliche Auswirkungen auf Herzfrequenz, Atemfrequenz und Blutdruck haben können. Die Interpretation einzelner Messwerte erfordert daher stets die Einordnung in den klinischen Gesamtkontext und die Beobachtung von Trends im zeitlichen Verlauf.
Der Transport stellt eine therapeutische Maßnahme dar und ist nicht lediglich logistischer Natur. Definitive Diagnostik wie bildgebende Verfahren, labordiagnostische Analysen oder chirurgische Interventionen stehen präklinisch nicht zur Verfügung. Daher ist die frühzeitige Entscheidung über Transportpriorität und Zielklinik elementarer Bestandteil der Behandlungsstrategie. Kriterien sind Verletzungsschwere, voraussichtlicher Interventionsbedarf, Erreichbarkeit spezialisierter Einrichtungen sowie Transportdauer. Eine strukturierte Voranmeldung mit Angabe von Patientendaten, Verdachtsdiagnose, Vitalparametern und bereits durchgeführten Maßnahmen ermöglicht der Zielklinik, personelle und technische Ressourcen rechtzeitig bereitzustellen.
Die Übergabe an die weiterbehandelnde Einrichtung gewährleistet die Kontinuität der Therapie. Eine strukturierte Kommunikation umfasst neben dem aktuellen Status insbesondere den zeitlichen Verlauf seit Alarmierung, relevante Vorbefunde, beobachtete Veränderungen sowie alle ergriffenen Maßnahmen einschließlich deren Wirkung. Standardisierte Übergabeschemata minimieren Informationsverluste und reduzieren das Risiko von Behandlungsfehlern. Dokumentation ist in diesem Zusammenhang ein zentrales Element der Qualitätssicherung. Sie dient der Nachvollziehbarkeit klinischer Entscheidungen, unterstützt die weitere Therapieplanung und besitzt darüber hinaus rechtliche Relevanz.
Ein weiterer Schwerpunkt der Ausbildung liegt auf Entscheidungsfindung und Priorisierung unter Zeitdruck. Einsatzkräfte müssen in der Lage sein, begrenzte Ressourcen zielgerichtet einzusetzen und Maßnahmen zu begründen. Jede Intervention ist mit einer systematischen Reevaluation zu verbinden: Welche Parameter haben sich verbessert? Bestehen weiterhin kritische Abweichungen? Ergibt sich eine neue Priorität? Diese zyklische Neubewertung erhöht die Patientensicherheit und verhindert, dass relevante Veränderungen übersehen werden.
Teamarbeit und klare Rollenverteilung sind wesentliche Faktoren für eine sichere Einsatzdurchführung. Eine definierte Aufgabenstruktur reduziert kognitive Belastung, vermeidet Doppelarbeit und minimiert Fehlerquellen. Klare Führungsstrukturen sowie standardisierte Kommunikationswege unterstützen eine effiziente Zusammenarbeit auch unter hoher emotionaler Belastung. Gleichzeitig sind rechtliche Rahmenbedingungen zu beachten, insbesondere im Hinblick auf Haftung, Tierschutzrecht, Einwilligungsfragen und Dokumentationspflichten. Die Kenntnis dieser Vorgaben schützt Tier, Halter und Einsatzkräfte gleichermaßen und schafft Handlungssicherheit.
Zusammenfassend verfolgt die präklinische Tierrettung das Ziel, unter Beachtung von Sicherheit, Struktur und Priorisierung eine rasche Stabilisierung zu erreichen und den Patienten ohne vermeidbaren Zeitverlust in eine geeignete weiterführende Versorgung zu überführen. Die Qualität des Einsatzes bemisst sich nicht an der Anzahl durchgeführter Maßnahmen, sondern an der strukturierten Entscheidungsfindung, der konsequenten Re-Evaluation und der lückenlosen Kommunikation entlang der gesamten Notfallkette.
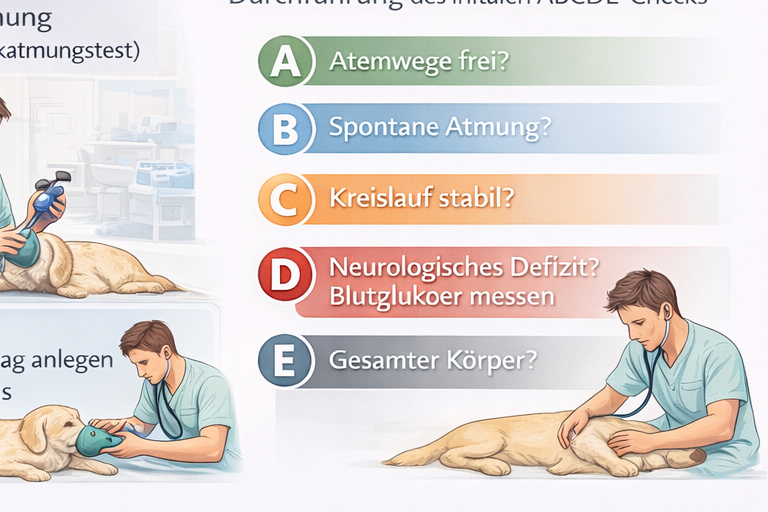
Das ABCDE-Schema bildet das zentrale strukturierende Entscheidungs- und Handlungsmodell im präklinischen Einsatz. Es priorisiert Maßnahmen nach dem Grad unmittelbarer Lebensgefahr und schafft damit ein reproduzierbares, teamübergreifend anwendbares Vorgehen. Die Abfolge ist strikt hierarchisch: Erst wenn ein Abschnitt suffizient beurteilt und – falls erforderlich – behandelt wurde, wird zum nächsten übergegangen. Dieses Prinzip verhindert, dass potenziell letale Störungen durch nachrangige Befunde überlagert werden. Das Schema ist zugleich dynamisch angelegt; nach jeder Intervention erfolgt eine erneute Bewertung beginnend bei A und B, um Veränderungen frühzeitig zu erkennen und Therapieeffekte zu überprüfen.
A – Airway (Atemweg): Im ersten Schritt wird die Durchgängigkeit des Atemwegs geprüft und gesichert. Zu berücksichtigen sind Fremdkörper, Blut, Erbrochenes, Zahn- oder Kieferverletzungen, Weichteilschwellungen, Larynxproblematiken sowie die Zungenlage. Bei Tieren kann zusätzlich ein Maulkorb oder eine provisorische Fixierung die Atemwegssituation beeinträchtigen und muss in die Beurteilung einbezogen werden. Schutzreflexe wie Schluck- und Hustenreflex geben Hinweise auf die Sicherung der Atemwege. Stress, Schmerz und Hypoxie können insbesondere bei Hund und Katze rasch zu Erschöpfung und Kollaps führen. Eine frühzeitige Atemwegssicherung und adäquate Oxygenierung sind daher essenziell, bevor weiterführende Diagnostik erfolgt.
B – Breathing (Atmung): Die Beurteilung der Atmung geht über die reine Frequenzmessung hinaus. Entscheidend ist die Atemarbeit: Thoraxexkursion, Einsatz der Bauchmuskulatur, Atemtiefe, Atemgeräusche wie Stridor oder Rasseln, Hecheln außerhalb thermoregulatorischer Situationen, Zyanose oder vermehrtes Nasenflügeln liefern Hinweise auf respiratorische Insuffizienz. Auch traumatische Ursachen wie Pneumothorax, Hämatothorax oder Rippenserienfrakturen sind differenzialdiagnostisch zu bedenken. Die Auskultation beider Thoraxseiten ermöglicht eine orientierende Beurteilung der Ventilation. Ziel ist die rasche Identifikation einer ventilatorischen oder oxygenatorischen Störung und deren unmittelbare Therapie.
C – Circulation (Kreislauf): Die Kreislaufbeurteilung umfasst mehr als eine isolierte Blutdruckmessung. Pulsqualität, Herzfrequenz, Kapillarfüllungszeit, Schleimhautfarbe, Temperatur der Akren sowie sichtbare oder verborgene Blutungsquellen liefern Hinweise auf Perfusionsstatus und Schockgeschehen. Zeichen der Zentralisation, verlängerte Rekapillarisierungszeit oder blasse bis graue Schleimhäute deuten auf eine kritische Minderperfusion hin. Neben äußeren Blutungen müssen auch innere Blutungen in Betracht gezogen werden, insbesondere bei Trauma. Priorität besitzt die rasche Blutungskontrolle und – im Rahmen der präklinischen Möglichkeiten – die Stabilisierung des Kreislaufs, um sekundäre Organschäden zu vermeiden.
D – Disability (Neurologischer Status): Dieser Abschnitt bewertet Bewusstseinslage, Pupillenreaktion, motorische Funktionen und Schmerzreaktion. Veränderungen können Ausdruck eines Schädel-Hirn-Traumas, metabolischer Entgleisungen oder schwerer Hypoxie sein. Bei Verdacht auf Hypoglykämie, insbesondere bei jungen, kleinen oder geschwächten Tieren, kann eine Blutzuckermessung indiziert und potenziell lebensrettend sein. Krampfaktivität erfordert umgehendes Handeln zur Vermeidung sekundärer Schäden. Ziel ist die frühzeitige Erkennung neurologischer Beeinträchtigungen und deren Einordnung in das Gesamtbild.
E – Exposure/Environment (Exposition und Umgebung): Abschließend wird der Patient vollständig inspiziert, um verdeckte Verletzungen nicht zu übersehen. Dabei ist gleichzeitig auf Wärmeerhalt zu achten, da insbesondere traumatisierte Tiere rasch auskühlen. Hypothermie verschlechtert Gerinnung, Kreislaufstabilität und Prognose. Auch Umgebungsfaktoren wie Nässe, Kälte oder Hitze sind aktiv zu berücksichtigen. Die vollständige Untersuchung erfolgt strukturiert und zügig, ohne die zuvor gesicherten Vitalfunktionen zu gefährden.
Das ABCDE-Schema ist zyklisch angelegt. Nach jeder therapeutischen Maßnahme erfolgt eine erneute Beurteilung beginnend bei den Atemwegen. Dieses Prinzip der kontinuierlichen Reevaluation stellt sicher, dass Verschlechterungen früh erkannt und Therapieerfolge objektiviert werden. Sobald eine lebensbedrohliche Abweichung identifiziert ist, wird unmittelbar gehandelt; differenzialdiagnostische Vertiefungen erfolgen erst nach Stabilisierung der Vitalfunktionen. Die Reihenfolge der Schritte besitzt dabei höhere Priorität als die Perfektion einzelner Messwerte.
Dokumentation ist integraler Bestandteil dieses Prozesses. Sie dient nicht administrativen Zwecken, sondern der Patientensicherheit, der Qualitätssicherung und der rechtlichen Absicherung. Erhobene Befunde, Zeitpunkte, Maßnahmen und beobachtete Trends müssen nachvollziehbar festgehalten werden, um eine lückenlose klinische Weiterbehandlung zu ermöglichen. Gerade bei Hund und Katze können Stress und Schmerz physiologische Parameter deutlich beeinflussen; deshalb ist die Bewertung im Verlauf entscheidend. Einzelwerte ohne Kontext besitzen nur begrenzte Aussagekraft.
Strukturierte Kommunikation innerhalb des Teams sowie mit der aufnehmenden Klinik reduziert Informationsverluste und verbessert die Versorgungsqualität. Eine klare Rollenverteilung senkt die kognitive Belastung in kritischen Situationen und erhöht die Handlungssicherheit. In der Ausbildung wird daher wiederholt trainiert, Befunde zu priorisieren, Entscheidungen fachlich zu begründen und im Verlauf systematisch zu reevaluieren. Rechtliche Rahmenbedingungen – insbesondere im Hinblick auf Tierschutz, Haftung und Dokumentationspflicht – sind bekannt und konsequent einzuhalten, um Tier, Halter und Einsatzkräfte gleichermaßen zu schützen.
Ziel des ABCDE-basierten Vorgehens ist nicht die abschließende Diagnostik am Einsatzort, sondern die rasche Stabilisierung und die strukturierte Vorbereitung auf den Transport in eine geeignete weiterführende Einrichtung. Eine konsequente Priorisierung, kontinuierliche Neubewertung und klare Kommunikation entlang der gesamten Notfallkette bilden die Grundlage für eine sichere und effektive präklinische Versorgung.
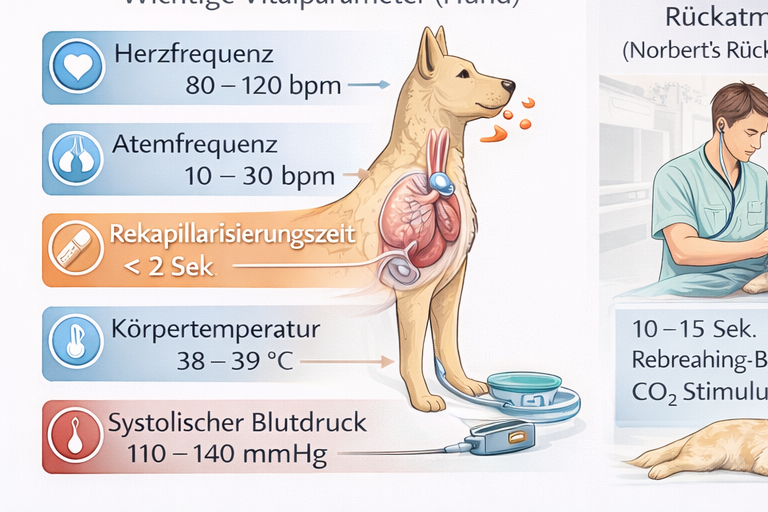
Die fachgerechte Interpretation von Vitalparametern stellt eine zentrale Kernkompetenz in der präklinischen Notfallversorgung dar. Einzelwerte besitzen nur begrenzte Aussagekraft; entscheidend ist ihre Einordnung in den klinischen Kontext sowie die Beurteilung des zeitlichen Verlaufs. Herzfrequenz und Atemfrequenz sind hierbei häufige, jedoch störanfällige Parameter. Ein aufgeregter oder schmerzbelasteter Hund kann eine ausgeprägte Tachykardie zeigen, ohne dass eine hämodynamische Instabilität vorliegt. Umgekehrt kann ein Tier im fortgeschrittenen Schockstadium trotz kritischer Hypoperfusion bradykard erscheinen. Die isolierte Betrachtung der Frequenz ist daher unzureichend; erst in Kombination mit weiteren Perfusionsparametern entsteht ein belastbares Gesamtbild.
Die Schleimhautfarbe und die kapilläre Rekapillarisierungszeit (CRT) liefern unmittelbare Hinweise auf die periphere Perfusion. Eine CRT von mehr als zwei bis drei Sekunden, blasse oder graue Schleimhäute, kalte Akren und ein schwacher, fadenförmiger Puls sprechen für eine relevante Hypoperfusion. Demgegenüber können gerötete Schleimhäute und kräftige, „bounding“ Pulse in frühen distributiven Zuständen beobachtet werden. Diese scheinbar gegensätzlichen Befunde verdeutlichen, dass Schock unterschiedliche Erscheinungsformen annehmen kann und stets differenziert beurteilt werden muss. Die Kombination mehrerer klinischer Zeichen ist hierbei entscheidend.
Die Körpertemperatur besitzt eine doppelte Bedeutung: Sie ist diagnostischer Parameter und therapeutisches Ziel zugleich. Hypothermie verschlechtert Gerinnungsfähigkeit, myokardiale Leistungsfähigkeit und periphere Durchblutung und ist insbesondere bei Trauma- oder Schockpatienten prognostisch ungünstig. Eine aktive Wärmeerhaltung ist daher integraler Bestandteil der präklinischen Versorgung. Gleichzeitig können Hyperthermie oder stressbedingte Temperaturerhöhungen auftreten, die ebenfalls differenziert bewertet werden müssen. Temperaturmessungen sind deshalb stets in Verbindung mit Allgemeinzustand und Umgebungsbedingungen zu interpretieren.
Blutdruckmessungen können zusätzliche Hinweise liefern, sind jedoch im präklinischen Umfeld technisch fehleranfällig und häufig erst in fortgeschrittenen Stadien pathologisch. Bewegungsartefakte, Stressreaktionen oder unzureichende Manschettengröße beeinflussen die Messgenauigkeit erheblich. Der Trend wiederholter Messungen besitzt daher höhere klinische Relevanz als ein isolierter Einzelwert. Ein abfallender Blutdruck in Verbindung mit sich verschlechternder Pulsqualität und verlängerter CRT ist deutlich aussagekräftiger als eine einmalige Grenzwertüberschreitung.
Klinisches Denken bedeutet, Vitalparameter nicht isoliert, sondern integrativ zu bewerten. Mentale Lage, Reaktionsfähigkeit, Pulsqualität, Schleimhautfarbe, CRT und Atmungsmuster ergänzen sich gegenseitig und ergeben in ihrer Gesamtschau ein robustes Bild der Kreislauf- und Atemsituation. Wiederholte Messungen im Minutenabstand ermöglichen die Identifikation von Trends und schaffen Entscheidungsgrundlagen für weitere Maßnahmen. Sobald eine lebensbedrohliche Abweichung erkannt wird, erfolgt unverzüglich die priorisierte Intervention; differenzialdiagnostische Vertiefungen schließen sich erst nach Stabilisierung an.
Gerade bei Hund und Katze ist zu berücksichtigen, dass Stress und Schmerz erhebliche Auswirkungen auf Herz- und Atemfrequenz haben können. Eine scheinbare Tachypnoe kann Ausdruck von Angst sein, während eine reduzierte Atemfrequenz im Kontext von Erschöpfung oder zentralnervöser Beeinträchtigung kritisch zu werten ist. Die Beurteilung muss daher stets unter Berücksichtigung von Verhalten, Umgebung und vorangegangenen Ereignissen erfolgen. Die Bewertung von Trends ist hierbei entscheidend, da Veränderungen häufig aussagekräftiger sind als absolute Zahlenwerte.
Für den Einsatz bedeutet dies, dass die strukturierte Priorisierung der Maßnahmen wichtiger ist als die Optimierung einzelner Messgrößen. Die Einhaltung eines klaren Handlungsablaufs verhindert, dass diagnostische Detailfragen die Behandlung vitaler Probleme verzögern. Eine eindeutige Rollenverteilung innerhalb des Teams reduziert kognitive Belastung, ermöglicht paralleles Arbeiten und erhöht die Versorgungsqualität. Während eine Person Vitalparameter erhebt und dokumentiert, kann eine andere stabilisierende Maßnahmen durchführen, wodurch Zeitverluste vermieden werden.
Dokumentation ist integraler Bestandteil der Patientensicherheit. Zeitpunkte, Messwerte, beobachtete Trends und durchgeführte Interventionen müssen nachvollziehbar festgehalten werden. Dies gewährleistet eine lückenlose Weitergabe relevanter Informationen an die aufnehmende Klinik und unterstützt die dortige Therapieplanung. Strukturierte Kommunikation verhindert Informationsverlust und ermöglicht es der Zielklinik, personelle sowie technische Ressourcen frühzeitig zu mobilisieren.
In der Ausbildung wird daher wiederholt trainiert, Befunde zu priorisieren, klinische Entscheidungen zu begründen und im Verlauf systematisch zu reevaluieren. Jede Intervention ist mit einer erneuten Bewertung der Vitalparameter zu verknüpfen: Welche Veränderungen sind eingetreten? Ist eine Stabilisierung erkennbar oder zeigt sich eine Verschlechterung? Dieses zyklische Vorgehen erhöht die Sicherheit und minimiert das Risiko, relevante Dynamiken zu übersehen. Rechtliche Rahmenbedingungen, insbesondere im Hinblick auf Dokumentationspflicht und Sorgfaltspflicht, sind bekannt und konsequent einzuhalten.
Das übergeordnete Ziel der präklinischen Beurteilung von Vitalparametern besteht nicht in der abschließenden Diagnosestellung am Einsatzort, sondern in der frühzeitigen Erkennung kritischer Zustände, der Einleitung geeigneter Maßnahmen und der strukturierten Vorbereitung auf den Transport in eine geeignete Weiterbehandlung. Die Qualität der Versorgung bemisst sich dabei an der fachlich fundierten Gesamtschau, der kontinuierlichen Verlaufsbeurteilung und der klaren Kommunikation innerhalb der Notfallkette.
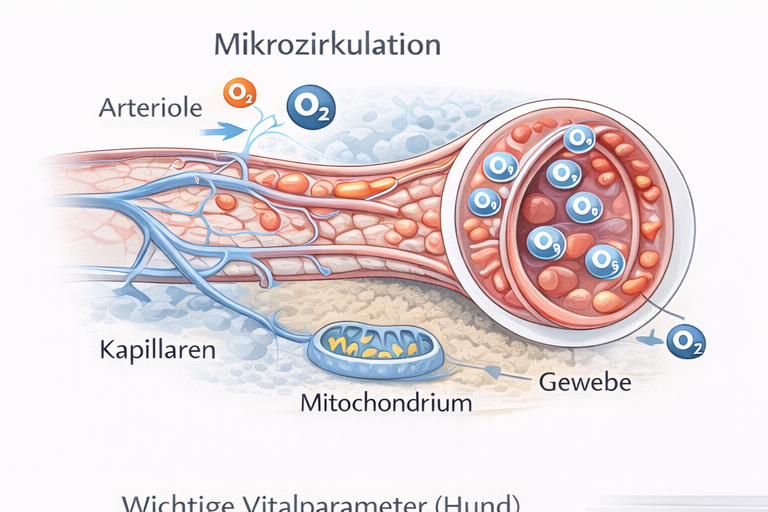
Bei 2er-Team: „Lead + Med“ klar benennen; Dokumentation kurz & chronologisch.
Die Qualität der präklinischen Versorgung wird maßgeblich durch die Teamkommunikation bestimmt. In der Tierrettung entstehen kritische Fehler erfahrungsgemäß seltener durch fehlendes Fachwissen als durch Missverständnisse, unklare Zuständigkeiten oder unvollständige Informationsweitergabe. Ein strukturiertes Kommunikationskonzept ist daher ebenso bedeutsam wie medizinische Expertise. Klare Rollenverteilung zu Einsatzbeginn – beispielsweise Teamleitung, Atemweg/Oxygenierung, Blutungskontrolle/Verbände sowie Dokumentation und externe Kommunikation – schafft Transparenz und reduziert Doppelarbeit oder Versorgungslücken. Jede Funktion ist eindeutig definiert, wodurch paralleles, koordiniertes Arbeiten ermöglicht wird.
Ein bewährtes Instrument ist die konsequente Anwendung der Closed-Loop-Kommunikation. Anweisungen werden klar adressiert, wiederholt und bestätigt. Beispiel: „Druckverband linke Hintergliedmaße anlegen.“ – „Druckverband linke Hintergliedmaße, verstanden.“ – „Bestätigt.“ Dieses Vorgehen minimiert Fehlinterpretationen, insbesondere in stressbelasteten Situationen mit hoher Geräuschkulisse oder emotionaler Dynamik. Die Teamleitung behält dabei den Gesamtüberblick, priorisiert Maßnahmen und sorgt für die Einhaltung des strukturierten Vorgehens. Gleichzeitig bleibt Raum für Rückmeldungen aus dem Team, um situative Veränderungen zeitnah zu berücksichtigen.
Die strukturierte Übergabe an die weiterbehandelnde Klinik ist ein zentraler Bestandteil der Notfallkette. Hier bietet sich beispielsweise das SBAR-Format an: Situation (aktueller Status und Anlass), Background (relevante Vorgeschichte und Ereignisablauf), Assessment (klinische Einschätzung mit Befunden und Trends) sowie Recommendation (empfohlene Maßnahmen oder vermuteter Interventionsbedarf). Entscheidend ist, nicht nur Einzelwerte zu kommunizieren, sondern insbesondere deren Verlauf: Hat sich die Herzfrequenz stabilisiert? Ist die Rekapillarisierungszeit rückläufig? Welche Maßnahmen wurden zu welchem Zeitpunkt durchgeführt, und wie reagierte der Patient darauf? Diese Informationen ermöglichen es der Zielklinik, Operationsbereitschaft, Blutprodukte, Bildgebung oder Intensivkapazitäten frühzeitig zu disponieren.
Dokumentation ist integraler Bestandteil der Teamkommunikation und dient der Patientensicherheit. Erfasst werden Einsatzzeiten, Vitalparameter, erhobene Befunde, durchgeführte Maßnahmen, applizierte Medikamente sowie besondere Ereignisse oder Komplikationen. Eine präzise, chronologische Dokumentation erleichtert die klinische Weiterbehandlung und besitzt zugleich rechtliche Relevanz. Rechtliche Rahmenbedingungen – insbesondere im Hinblick auf Sorgfaltspflicht, Tierschutz und Haftung – sind bekannt und werden konsequent beachtet. Sie schaffen einen verbindlichen Handlungsrahmen für alle Beteiligten.
Auch die Kommunikation mit Tierhaltern ist Teil des professionellen Einsatzmanagements. Sie erfolgt ruhig, sachlich und transparent. Informationen werden verständlich vermittelt, ohne falsche Sicherheit oder unbegründete Prognosen zu geben. Gleichzeitig wird die emotionale Belastung der Halter berücksichtigt. Klare Aussagen zu geplanten Maßnahmen und zum weiteren Ablauf schaffen Orientierung und Vertrauen. Eine strukturierte Kommunikation nach außen reduziert Stressfaktoren, die sich indirekt auf das Einsatzgeschehen auswirken können.
Im operativen Ablauf gilt das Prinzip der Priorisierung: Sobald eine lebensbedrohliche Abweichung erkannt wird, erfolgt die unmittelbare Intervention; differenzierende Überlegungen schließen sich erst nach Stabilisierung an. Die Reihenfolge der Schritte ist wichtiger als die Optimierung einzelner Messwerte. Gerade bei Hund und Katze können Stress und Schmerz Vitalparameter erheblich beeinflussen, weshalb Trends und Gesamtschau entscheidend sind. Die Teamleitung stellt sicher, dass Interventionen regelmäßig reevaluieren werden: Welche Maßnahme war effektiv? Wo besteht weiterhin Handlungsbedarf?
In der Ausbildung wird diese strukturierte Vorgehensweise wiederholt trainiert. Simulationen fördern das Priorisieren unter Zeitdruck, das klare Formulieren von Anweisungen sowie die konsequente Reevaluation nach jeder Intervention. Eine eindeutige Rollenverteilung reduziert kognitive Belastung, verbessert die Übersicht und erhöht die Sicherheit für Mensch und Tier gleichermaßen. Ziel ist nicht die vollständige Problemlösung am Einsatzort, sondern die stabile Vorbereitung des Patienten auf den Transport und die definitive Versorgung ohne vermeidbaren Zeitverlust.
Strukturierte Kommunikation bildet somit das verbindende Element zwischen medizinischer Maßnahme, Teamkoordination, Dokumentation und klinischer Weiterbehandlung. Sie verhindert Informationsverluste, erhöht die Effizienz und trägt wesentlich zur Versorgungsqualität bei. Eine professionelle Teamkommunikation ist daher kein ergänzender Aspekt, sondern ein zentraler Bestandteil der präklinischen Tierrettung.
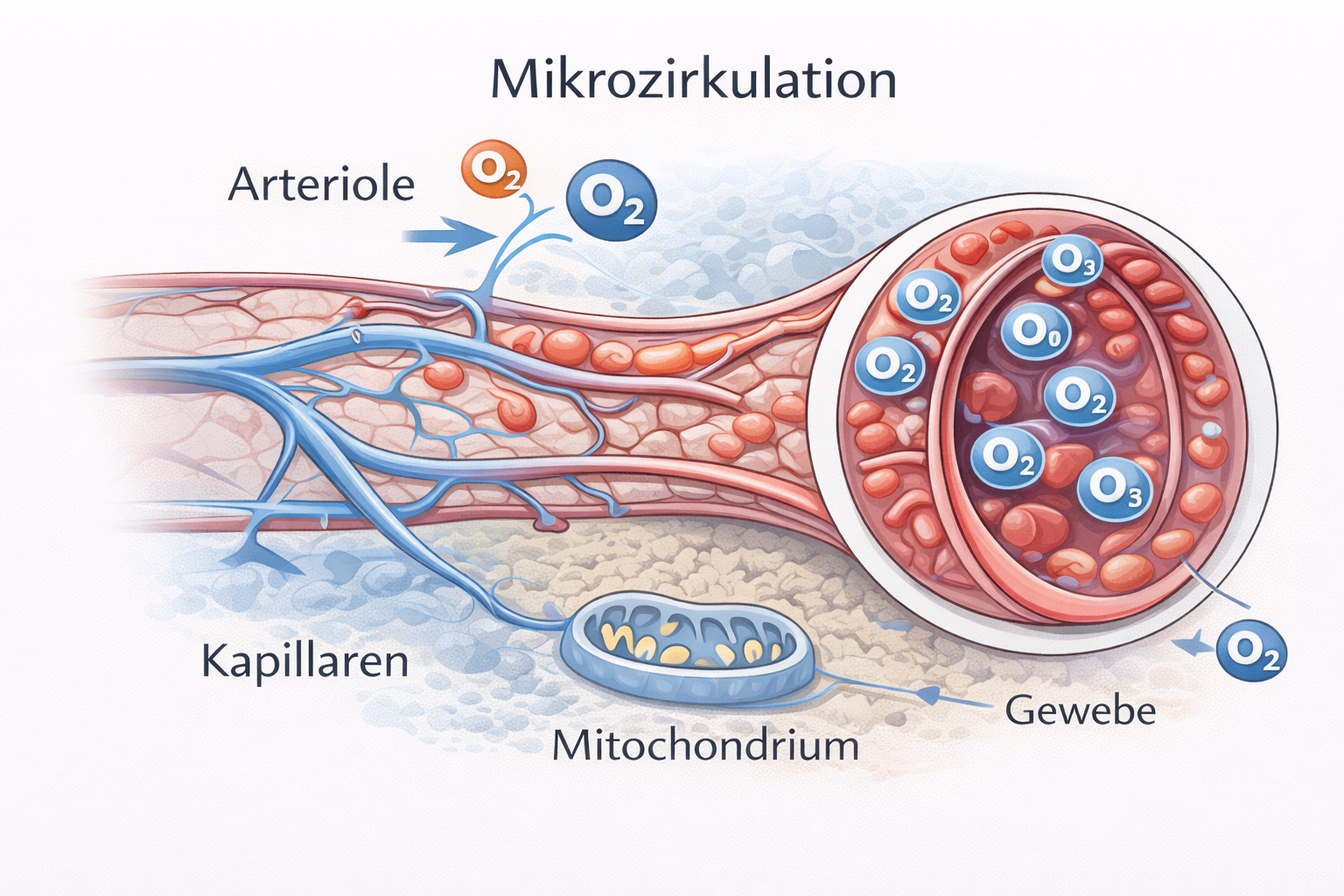
Rechtliche und ethische Grundlagen sind integraler Bestandteil der präklinischen Tierrettung und sichern die professionelle Handlungsfähigkeit im Einsatz. Sie definieren den verbindlichen Rahmen, innerhalb dessen medizinische Entscheidungen getroffen werden. Zentrales Leitprinzip ist das Tierwohl. Ziel ist es, Leiden zu minimieren, Stress zu reduzieren und eine fachlich angemessene Versorgung im Rahmen der eigenen Qualifikation und Kompetenzen sicherzustellen. Jede Maßnahme muss sowohl medizinisch indiziert als auch rechtlich vertretbar und ethisch begründet sein.
Grundsätzlich ist die Einwilligung des Tierhalters anzustreben. Sie bildet die rechtliche Grundlage diagnostischer und therapeutischer Maßnahmen. In akuten Notlagen kann jedoch eine Situation der „Gefahr im Verzug“ vorliegen, in der sofortiges Handeln erforderlich ist, um erhebliche Schäden oder den Tod des Tieres abzuwenden. In solchen Fällen ist eine zeitkritische Intervention auch ohne ausdrückliche Zustimmung gerechtfertigt, sofern sie verhältnismäßig und medizinisch notwendig ist. Die Einschätzung dieser Situation erfordert fachliche Kompetenz und eine sorgfältige Dokumentation der Entscheidungsgrundlage.
Typische Konfliktsituationen sind Bestandteil der Ausbildung und müssen strukturiert bewältigt werden. Hierzu zählt etwa die Ablehnung eines Transports durch den Halter trotz kritischer Befundlage. Ebenso können widersprüchliche Aussagen mehrerer Beteiligter oder gefährliche Umgebungsbedingungen die Entscheidungsfindung erschweren. In solchen Konstellationen ist eine ruhige, sachliche Aufklärung über Risiken, Prognoseunsicherheiten und Behandlungsoptionen erforderlich. Ziel ist eine informierte, tierwohlorientierte Entscheidung unter Wahrung der Professionalität.
Dokumentationspflichten besitzen in diesem Zusammenhang besondere Bedeutung. Ein sachliches, objektives Protokoll mit klaren Zeitangaben, erhobenen Befunden, empfohlenen Maßnahmen und getroffenen Entscheidungen schützt Tier, Halter und Einsatzkräfte gleichermaßen. Spekulationen oder wertende Formulierungen sind zu vermeiden. Die Dokumentation dient nicht nur der rechtlichen Absicherung, sondern ist zugleich Grundlage der klinischen Weiterbehandlung und damit Teil der Patientensicherheit.
Datenschutz ist ebenfalls zu beachten. Es werden ausschließlich solche personenbezogenen Daten erhoben und weitergegeben, die für die medizinische Versorgung erforderlich sind. Die Informationsweitergabe an die Zielklinik erfolgt zweckgebunden und beschränkt sich auf relevante medizinische Inhalte. Ein verantwortungsvoller Umgang mit sensiblen Daten stärkt das Vertrauen der Halter und entspricht den rechtlichen Vorgaben.
Ethisch zentral ist das Prinzip der Verhältnismäßigkeit. Invasive Maßnahmen dürfen nur bei klarer Indikation, entsprechender Qualifikation und unter Berücksichtigung des Risikoprofils durchgeführt werden. Bestehen Zweifel an Kompetenz oder Nutzen-Risiko-Abwägung, stehen Stabilisierung und rascher Transport in eine geeignete Einrichtung im Vordergrund. Ziel ist nicht die vollständige Problemlösung am Einsatzort, sondern die Herstellung von Transportfähigkeit und die Übergabe in definitive Versorgung ohne vermeidbaren Zeitverlust.
Ein professionelles Auftreten umfasst darüber hinaus respektvollen Umgang mit Tierhaltern, Helfern und weiteren Beteiligten. Emotionale Ausnahmesituationen erfordern Empathie, klare Sprache und deeskalierende Kommunikation. Konflikte werden sachlich adressiert, ohne Schuldzuweisungen oder Konfrontation. Eine strukturierte Teamkommunikation verhindert interne Missverständnisse und unterstützt die Einhaltung des prioritätenorientierten Vorgehens. Die Reihenfolge der Maßnahmen ist dabei entscheidender als die Perfektion einzelner Messwerte.
Gerade bei Hund und Katze ist zu berücksichtigen, dass Stress und Schmerz Vitalparameter erheblich beeinflussen können. Die klinische Beurteilung erfolgt daher stets im Kontext von Gesamtschau und Verlauf. Sobald eine lebensbedrohliche Abweichung erkannt wird, erfolgt die unmittelbare Intervention; differenzierende Überlegungen schließen sich erst nach Stabilisierung an. Eine klare Rollenverteilung im Team reduziert kognitive Belastung und erhöht die Sicherheit für alle Beteiligten.
In der Ausbildung wird wiederholt trainiert, ethische und rechtliche Aspekte in Entscheidungsprozesse zu integrieren. Fallbeispiele fördern die Fähigkeit, medizinische Priorisierung, rechtliche Rahmenbedingungen und kommunikative Kompetenz miteinander zu verbinden. Jede Intervention wird mit einer Reevaluation verknüpft: Welche Wirkung wurde erzielt? Besteht weiterer Handlungsbedarf? Dieses strukturierte Vorgehen stärkt die Handlungssicherheit und minimiert Fehlentscheidungen.
Recht und Ethik sind somit keine theoretischen Randthemen, sondern praktische Handlungsinstrumente. Sie schaffen Orientierung in komplexen Situationen, sichern Transparenz und tragen wesentlich zur Qualität der präklinischen Tierrettung bei. Die konsequente Beachtung dieser Grundsätze gewährleistet, dass medizinische Entscheidungen fachlich fundiert, rechtlich abgesichert und ethisch verantwortbar sind.
Single-Choice: pro Frage eine richtige Antwort. Bestehensgrenze: 70%.
Ziel: Prioritäten korrekt setzen (Eigensicherung → ABCDE → Wärmeschutz → Transport/Übergabe).
Seite 10 von 24