SACHVERSTÄNDIGENBÜRO

Ausbildungsplattform (Tier-Notruf)
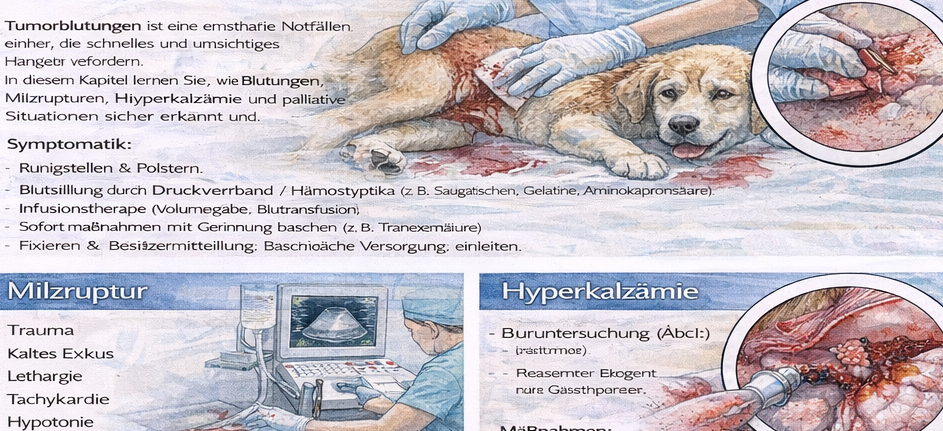
Tumorblutungen stellen im präklinischen Umfeld eine besondere Herausforderung dar, weil sie in sehr unterschiedlichen Ausprägungen auftreten können. Das Spektrum reicht von geringfügigen, intermittierenden Schleimhautblutungen bis hin zu massiven, potenziell lebensbedrohlichen Blutungen, die nur schwer kontrollierbar sind. Typische Blutungsquellen sind ulzerierte Hauttumoren, Tumoren der Maulhöhle, Nasentumoren, Analbeutel- oder Perinealtumoren sowie innere Tumoren, die sekundär zu Gerinnungsstörungen oder Gefäßrupturen führen können. Für den Rettungssanitäter besteht die erste und wichtigste Aufgabe darin, zwischen einer äußeren Blutung und dem Verdacht auf eine innere Blutung zu unterscheiden. Diese Unterscheidung bestimmt maßgeblich das weitere Vorgehen. Während äußere Blutungen zumindest teilweise mechanisch kontrolliert werden können, erfordern innere Blutungen eine besonders rasche klinische Versorgung.
Bei äußeren Tumorblutungen ist das primäre Ziel nicht eine vollständige oder „perfekte“ Hämostase, sondern eine möglichst effektive Reduktion des Blutverlustes bei gleichzeitiger Schonung des Gewebes. Gleichzeitig müssen Kreislaufstabilität und Schockprävention berücksichtigt werden. Das standardisierte Vorgehen beginnt mit direkter Kompression der Blutungsstelle mittels steriler Kompressen oder geeigneter Verbandsmaterialien. Anschließend kann ein Druckverband angelegt werden. Dabei wird in der Ausbildung betont, dass der Verband nur so fest wie notwendig und gleichzeitig so schonend wie möglich angelegt werden soll. Zu starke Kompression kann empfindliches Tumorgewebe zusätzlich schädigen oder Schmerzen verstärken.
Eine besondere Herausforderung stellen Blutungen aus der Maulhöhle dar. Hier sind klassische Druckverbände häufig nicht praktikabel. Stattdessen kann eine vorsichtige Kompression mit sterilen Gazetupfern erfolgen, sofern dies gefahrlos möglich ist. Zusätzlich spielen Stressreduktion, eine ruhige Umgebung und ein schneller Transport eine entscheidende Rolle. Jede unnötige Manipulation kann die Blutung verstärken, da Tumorgewebe häufig stark vaskularisiert und fragil ist.
Ein zentraler Bestandteil der Ausbildung ist die Vermeidung iatrogener Schäden. Häufiges Abnehmen eines Verbandes zur Kontrolle der Blutung ist beispielsweise problematisch, da jedes Entfernen das bereits gebildete Gerinnsel zerstören kann. Ebenso werden aggressive Spülungen oder improvisierte Hausmittel ausdrücklich vermieden. Ziel ist immer eine möglichst stabile Situation bis zur klinischen Versorgung.
Parallel zur lokalen Blutungskontrolle erfolgt eine kontinuierliche Kreislaufbeurteilung. Wichtige Parameter sind Schleimhautfarbe, Kapillarfüllungszeit (CRT), Pulsqualität, Herzfrequenztrend, Atemarbeit und Körpertemperatur. Tumorpatienten haben häufig bereits vor dem akuten Ereignis eine eingeschränkte physiologische Reserve. Anämie, Hypoproteinämie oder chronische Erkrankungen können dazu führen, dass bereits moderate Blutverluste zu einer kritischen Kreislaufsituation führen.
Daher wird in der Ausbildung vermittelt, dass ein scheinbar moderater Blutverlust bei onkologischen Patienten deutlich schwerwiegender sein kann als bei einem ansonsten gesunden Tier. Schon geringe Mengen verlorenen Blutes können zu Hypovolämie und Kreislaufdekompensation führen. Aus diesem Grund wird die frühzeitige Einschätzung des Schockrisikos besonders betont.
Für die strukturierte Übergabe an die Klinik werden mehrere Kerninformationen vermittelt. Dazu gehören die vermutete Blutungsquelle, die Dauer der Blutung, eine grobe Einschätzung der Blutmenge sowie die bereits durchgeführten Maßnahmen. Zusätzlich werden der Verlauf der Vitalparameter und mögliche Hinweise auf eine Gerinnungsstörung dokumentiert. Diese Informationen ermöglichen der Klinik eine gezielte Vorbereitung auf weiterführende Diagnostik und Therapie.
Onkologische Notfälle unterscheiden sich grundlegend von klassischen Traumata. Während traumatische Ereignisse meist abrupt bei zuvor gesunden Patienten auftreten, entwickeln sich tumorbedingte Komplikationen häufig aus einer chronischen Grunderkrankung heraus. Viele Patienten zeigen bereits vor dem Notfall Anzeichen wie schleichenden Gewichtsverlust, reduzierte Leistungsfähigkeit oder intermittierende Schwächeepisoden.
Diese Vorgeschichte führt häufig zu erheblichen physiologischen Reservedefiziten. Anämie, Proteinverlust oder chronische Entzündungsprozesse können die Fähigkeit des Körpers zur Kompensation erheblich einschränken. Deshalb ist ein besonders strukturiertes präklinisches Vorgehen erforderlich. Die zentralen Ziele sind Blutungskontrolle, Sicherung der Perfusion, Schmerzreduktion, Stressminimierung sowie ein rascher Transport in eine geeignete Klinik.
Das Kapitel trainiert eine Priorisierung nach dem ABCDE-Schema. Bei onkologischen Patienten steht häufig der Punkt „C“ für Circulation im Vordergrund. Okkulte Blutungen, Hämoperitoneum, Gerinnungsstörungen oder tumorassoziierte Anämien können schnell zu Kreislaufproblemen führen. Ein scheinbar ruhiger oder apathischer Patient kann daher trotz geringer äußerer Symptome kritisch sein.
Besonders wichtige klinische Hinweise sind blasse Schleimhäute, verlängerte Kapillarfüllungszeit und ein schwacher Puls. Diese Kombination deutet auf eine unzureichende Gewebeperfusion hin und muss als Schockzustand bis zum Beweis des Gegenteils betrachtet werden. Auch kalte Extremitäten oder eine zunehmende Tachykardie können frühe Warnzeichen sein.
Ein didaktischer Schwerpunkt liegt auf der Differenzialdiagnostik. Bestimmte Symptomkombinationen liefern wertvolle Hinweise auf mögliche Ursachen. Blasse Schleimhäute, kalte Extremitäten und Tachykardie sprechen beispielsweise stark für einen Schockzustand. Ein akutes Abdomen in Kombination mit Kollaps kann auf eine innere Blutung hinweisen. Polyurie und Polydipsie mit Schwäche und Herzrhythmusstörungen können hingegen auf Elektrolytstörungen hindeuten.
Auch Schmerz spielt eine wichtige Rolle in der präklinischen Beurteilung. Tumorpatienten können starke Schmerzen entwickeln, insbesondere bei infiltrierenden Tumoren oder Knochenmetastasen. Schmerzbedingte Unruhe erhöht den Stresslevel des Patienten und kann Kreislaufprobleme verstärken. Daher wird in der Ausbildung vermittelt, dass eine ruhige Umgebung und minimalinvasive Manipulationen einen wichtigen Beitrag zur Stabilisierung leisten.
Ein weiterer zentraler Aspekt ist die Kommunikation mit den Tierhaltern. Onkologische Patienten befinden sich häufig in einem emotional sensiblen Umfeld. Halterinnen und Halter sind oft stark belastet und verunsichert. Die Ausbildung vermittelt daher eine klare und ruhige Kommunikationsstrategie. Kurze, verständliche Sätze und eine sachliche Erklärung der Situation helfen, Vertrauen zu schaffen und gleichzeitig die notwendige Dringlichkeit zu vermitteln.
Darüber hinaus wird auch der Umgang mit möglichen palliativen Situationen thematisiert. Nicht jeder onkologische Notfall hat das Ziel einer langfristigen Heilung. In manchen Fällen steht die Stabilisierung oder die Reduktion von Leiden im Vordergrund. Diese Aspekte werden sensibel angesprochen, ohne jedoch präklinisch endgültige Therapieentscheidungen vorwegzunehmen.
Onkologische Patienten haben zudem ein erhöhtes Risiko für iatrogene Komplikationen. Tumorerkrankungen können mit thromboembolischen Ereignissen, Infektionsanfälligkeit oder einer erhöhten Stresssensibilität einhergehen. Auch Hypothermie kann schneller auftreten, insbesondere bei geschwächten oder anämischen Patienten.
Daher wird Wärmemanagement als wichtiger Bestandteil der präklinischen Versorgung vermittelt. Decken, Wärmematten oder ein geschützter Transport können helfen, eine weitere Auskühlung zu verhindern. Gleichzeitig wird auf eine sanfte Fixation geachtet, um unnötige Schmerzen oder Stress zu vermeiden.
Für die Übergabe an die Klinik wird ein onkologiespezifisches Schema trainiert. Wenn bekannt, werden Tumorart und Lokalisation genannt. Zusätzlich sind Informationen über den bisherigen Behandlungsstand wichtig, etwa Operationen, Chemotherapie, Bestrahlung oder laufende medikamentöse Therapien wie Steroide oder NSAIDs.
Auch aktuelle Symptome müssen klar beschrieben werden. Dazu gehören Blutungen, Kollaps, Atemnot oder Schmerzen. Ergänzend werden Vitalparameter wie Herzfrequenz, Atemfrequenz, Kapillarfüllungszeit und Temperatur übermittelt. Schließlich werden alle präklinischen Maßnahmen dokumentiert, etwa Kompression, Druckverband, Sauerstoffgabe oder Wärmeschutz.
Die Ausbildung nutzt realistische Fallbeispiele, um diese Prinzipien zu trainieren. Ein häufiges Szenario ist ein Hund mit Verdacht auf Hämangiosarkom, der plötzlich kollabiert. Hier muss der Lernende rasch an eine innere Blutung denken und entsprechend handeln. Ein anderes Szenario ist ein Maulhöhlentumor mit massiver Blutung, bei dem die lokale Blutungskontrolle und der schnelle Transport entscheidend sind.
Weitere Fallbeispiele umfassen Patienten mit Lymphomen, die durch Hyperkalzämie geschwächt sind, oder Tumorpatienten mit ausgeprägter Dyspnoe und Schmerzen. Jede dieser Situationen erfordert eine klare Priorisierung, sichere Maßnahmen und eine strukturierte Übergabe.
Gleichzeitig werden die Grenzen der präklinischen Therapie deutlich vermittelt. Definitive Blutstillung, chirurgische Maßnahmen, Transfusionen oder komplexe Elektrolyttherapien können nur in einer Klinik erfolgen. Die Aufgabe des präklinischen Teams besteht daher darin, Zeit zu gewinnen und den Patienten möglichst stabil zur weiterführenden Behandlung zu bringen.
Die wichtigsten präklinischen Maßnahmen bleiben daher grundlegende Stabilisierungstechniken: ruhige Lagerung, Wärmeschutz, Blutungskontrolle, Sauerstoffgabe wenn toleriert sowie eine möglichst kurze Zeitspanne bis zur klinischen Versorgung. Diese scheinbar einfachen Maßnahmen haben oft den größten Einfluss auf das Überleben des Patienten.

Milzrupturen und das daraus resultierende Hämoperitoneum gehören zu den klassischen onkologischen Notfällen in der Kleintiermedizin. Besonders häufig treten sie im Zusammenhang mit Milztumoren beim Hund auf, wobei das Hämangiosarkom eine der bekanntesten Ursachen darstellt. Diese Tumorart ist hochgradig vaskularisiert und kann spontan rupturieren, wodurch es zu einer massiven Einblutung in die Bauchhöhle kommt. Die klinische Situation ist deshalb besonders gefährlich, weil sich der Blutverlust zunächst unbemerkt entwickeln kann und erst spät dramatische Symptome hervorruft. Viele Tiere zeigen in der Frühphase lediglich unspezifische Symptome wie Müdigkeit, reduzierte Aktivität oder eine kurzzeitige Schwäche. Diese scheinbar harmlosen Veränderungen können jedoch innerhalb kurzer Zeit in einen schweren Kreislaufkollaps übergehen.
Der typische Verlauf ist deshalb tückisch: Ein Tier wirkt zunächst lediglich abgeschlagen oder bewegt sich langsamer als gewohnt. Wenige Minuten oder Stunden später kann es plötzlich kollabieren. Die Ursache ist der rasche Verlust von Blut in die Bauchhöhle. Präklinisch ist es daher entscheidend, diese Situation frühzeitig zu erkennen und richtig einzuordnen. Das klinische Bild wird häufig von Schockzeichen dominiert. Zu den wichtigsten Hinweisen gehören blasse Schleimhäute, eine verlängerte Kapillarfüllungszeit, Tachykardie, ein schwacher oder kaum tastbarer Puls sowie kalte Extremitäten. Zusätzlich kann der Bauchumfang vergrößert erscheinen oder das Tier zeigt Anzeichen eines schmerzhaften Abdomens. Allerdings ist ein schmerzhaftes Abdomen nicht zwingend vorhanden, weshalb sich der Verdacht auf eine innere Blutung oft nur aus den Kreislaufparametern ergibt.
Die zentrale präklinische Kompetenz besteht darin, eine mögliche innere Blutung zu erkennen und sofort ein strukturiertes Schockmanagement einzuleiten. Da jede unnötige Bewegung die Blutung verstärken kann, wird ein möglichst schonender Umgang mit dem Patienten trainiert. Umlagerungen erfolgen vorsichtig und nur wenn unbedingt erforderlich. Ziel ist es, zusätzliche mechanische Belastungen des Abdomens zu vermeiden. Eine ruhige Lagerung, Wärmeschutz und eine stressarme Umgebung sind essenziell, um den Kreislauf nicht weiter zu destabilisieren.
Wärmemanagement spielt eine besondere Rolle, da Patienten mit inneren Blutungen rasch auskühlen können. Hypothermie verschlechtert die Gerinnungsfähigkeit des Blutes und verstärkt somit die Blutungsproblematik. Daher werden Decken, isolierende Unterlagen oder Wärmematten eingesetzt, um einen weiteren Temperaturverlust zu verhindern. Gleichzeitig wird darauf geachtet, das Tier möglichst wenig zu manipulieren, um Stressreaktionen zu vermeiden.
Eine Sauerstoffgabe kann in vielen Fällen sinnvoll sein. Bei Hämoperitoneum entsteht häufig eine akute Anämie, wodurch die Sauerstofftransportkapazität des Blutes reduziert ist. Durch die Gabe von Sauerstoff kann zumindest vorübergehend die Gewebeoxygenierung verbessert werden. Es wird jedoch klar vermittelt, dass Sauerstoff keine definitive Therapie darstellt. Die eigentliche Behandlung – einschließlich möglicher Bluttransfusionen und chirurgischer Intervention – kann nur in einer Klinik erfolgen.
Wenn im jeweiligen System eine präklinische Flüssigkeitstherapie erlaubt ist, wird diese sehr vorsichtig eingesetzt. In der Ausbildung wird häufig das Konzept der sogenannten „permissiven Resuscitation“ vermittelt. Dabei wird nur so viel Flüssigkeit verabreicht, dass eine minimale Kreislaufstabilität erreicht wird. Ziel ist es, einen kritischen Blutdruckabfall zu verhindern, ohne gleichzeitig frisch gebildete Gerinnsel auszuwaschen. Eine aggressive Volumentherapie könnte die Blutung verstärken und die Situation verschlechtern.
Ein weiterer wichtiger Bestandteil der präklinischen Versorgung ist die frühzeitige Voranmeldung der Klinik. Wenn der Verdacht auf ein Hämoperitoneum oder eine Milzruptur besteht, sollte dies klar kommuniziert werden. Die Voranmeldung enthält Informationen über den aktuellen Kreislaufstatus, mögliche Kollapsereignisse und den allgemeinen Zustand des Patienten. Diese Informationen ermöglichen es der Klinik, notwendige diagnostische und therapeutische Maßnahmen vorzubereiten.
Bei der Übergabe werden mehrere zentrale Parameter strukturiert weitergegeben. Dazu gehören der zeitliche Verlauf der Symptome, mögliche Kollapsereignisse, bekannte Tumordiagnosen sowie aktuelle Medikamente wie NSAIDs oder Steroide. Zusätzlich werden Vitalparameter wie Herzfrequenz, Atemfrequenz, Kapillarfüllungszeit und Temperatur dokumentiert. Auch bereits durchgeführte präklinische Maßnahmen werden klar kommuniziert.
Onkologische Notfälle unterscheiden sich grundsätzlich von klassischen Traumata. Während traumatische Verletzungen meist plötzlich auftreten, entwickeln sich tumorbedingte Komplikationen häufig aus einer chronischen Erkrankung heraus. Viele Patienten zeigen bereits zuvor unspezifische Symptome wie Gewichtsverlust, reduzierte Belastbarkeit oder intermittierende Schwächeepisoden.
Diese chronischen Veränderungen führen häufig zu einer eingeschränkten physiologischen Reserve. Anämie, Hypoproteinämie oder chronische Entzündungsprozesse können die Fähigkeit des Körpers zur Kompensation erheblich reduzieren. Deshalb kann selbst ein moderater Blutverlust bei onkologischen Patienten schnell lebensbedrohlich werden.
Das Kapitel vermittelt daher ein besonders strukturiertes präklinisches Vorgehen. Die wichtigsten Ziele sind die Stabilisierung der Perfusion, die Reduktion von Stress und Schmerzen sowie ein möglichst schneller Transport in eine geeignete Klinik. Jede unnötige Verzögerung kann den Zustand des Patienten verschlechtern.
Die Ausbildung orientiert sich dabei konsequent am ABCDE-Schema. Bei Tumorpatienten steht häufig der Buchstabe „C“ für Circulation im Mittelpunkt. Okkulte Blutungen, Hämoperitoneum oder tumorassoziierte Anämien können schnell zu einer kritischen Kreislaufsituation führen. Ein scheinbar ruhiger Patient darf daher niemals automatisch als stabil betrachtet werden.
Ein didaktischer Schwerpunkt liegt auf der Interpretation robuster klinischer Zeichen. Blasse Schleimhäute in Kombination mit kalten Extremitäten und Tachykardie müssen immer als möglicher Schockzustand interpretiert werden, bis das Gegenteil bewiesen ist. Auch ein plötzlich kollabierendes Tier mit akutem Abdomen sollte immer den Verdacht auf eine innere Blutung wecken.
Weitere Differenzialdiagnosen werden ebenfalls trainiert. Beispielsweise können Elektrolytstörungen Symptome wie Schwäche oder Herzrhythmusstörungen verursachen. Ebenso können starke Schmerzen zu Unruhe und Tachykardie führen. Die Fähigkeit, diese unterschiedlichen Ursachen voneinander zu unterscheiden, ist ein zentraler Bestandteil der Ausbildung.
Ein weiterer wichtiger Aspekt ist die Kommunikation mit den Tierhaltern. Onkologische Notfälle sind häufig emotional belastend, da viele Halter bereits wissen, dass ihr Tier an einer schweren Erkrankung leidet. Die Ausbildung vermittelt deshalb eine ruhige und klare Kommunikationsstrategie. Kurze, verständliche Aussagen helfen, Vertrauen aufzubauen und gleichzeitig die Dringlichkeit der Situation zu vermitteln.
Auch mögliche palliative Situationen werden thematisiert. In manchen Fällen steht nicht mehr die langfristige Heilung, sondern die Stabilisierung oder die Reduktion von Leiden im Vordergrund. Diese Aspekte werden sensibel angesprochen, ohne präklinisch endgültige Therapieentscheidungen zu treffen.
Onkologische Patienten haben zudem ein erhöhtes Risiko für iatrogene Komplikationen. Thromboembolische Ereignisse, Infektionen oder eine erhöhte Stressanfälligkeit können die Situation zusätzlich verschlechtern. Deshalb wird ein möglichst schonendes Handling des Patienten als Qualitätsmerkmal vermittelt.
Die Ausbildung nutzt realistische Fallbeispiele, um diese Prinzipien zu trainieren. Ein typisches Szenario ist ein älterer Hund, der plötzlich kollabiert und blasse Schleimhäute zeigt. Der Lernende muss den Verdacht auf ein Hämoperitoneum erkennen, Schockmaßnahmen einleiten und den Transport organisieren.
Weitere Szenarien umfassen Patienten mit Maulhöhlentumoren, die stark bluten, oder Tiere mit Lymphomen, die durch metabolische Komplikationen geschwächt sind. Jede dieser Situationen verlangt eine klare Priorisierung und eine strukturierte Übergabe.
Gleichzeitig wird deutlich vermittelt, dass die definitive Therapie dieser Erkrankungen nur in der Klinik erfolgen kann. Chirurgische Eingriffe, Bluttransfusionen oder komplexe Intensivtherapien liegen außerhalb des präklinischen Handlungsspielraums. Die Aufgabe des präklinischen Teams besteht darin, Zeit zu gewinnen und den Patienten möglichst stabil zur weiterführenden Behandlung zu bringen.
Die effektivsten Maßnahmen bleiben daher grundlegende Stabilisierungstechniken: ruhige Lagerung, Wärmeschutz, Sauerstoffgabe wenn toleriert und eine möglichst kurze Transportzeit. Diese scheinbar einfachen Maßnahmen haben häufig den größten Einfluss auf das Überleben des Patienten.

Hyperkalzämie der Malignität ist ein metabolischer onkologischer Notfall, der vor allem bei Lymphomen, Analbeutel-/Apokrinen Drüsenkarzinomen, multiplen Myelomen und weiteren Neoplasien auftreten kann. Pathophysiologisch steht nicht „zu viel Calcium im Futter“ im Vordergrund, sondern eine tumorgetriebene Dysregulation: Tumoren können parathormonähnliche Faktoren (insbesondere PTH-related peptide) freisetzen, osteoklastische Knochenresorption fördern oder die renale Calciumrückresorption verändern. Das Ergebnis ist ein systemischer Zustand, der mehrere Organsysteme gleichzeitig belastet: Niere, Herz-Kreislauf, Gastrointestinaltrakt und Nervensystem. Präklinisch ist die Herausforderung, dass das klinische Bild selten „wie ein Elektrolytproblem“ aussieht, sondern häufig wie ein unspezifischer Leistungsknick oder „Magen-Darm“. Genau diese Unspezifität macht Hyperkalzämie in der Ausbildung zu einem wichtigen Denkmodell: Der Rettungssanitäter soll lernen, aus wenigen Signalen eine plausible Hypothese zu bilden und diese konsequent als Verdacht zu kommunizieren, ohne im Feld eine definitive Diagnose zu erzwingen.
Die Symptomatik entsteht durch die Kombination aus Hyperkalzämie und sekundärer Dehydratation. Typisch sind Polyurie/Polydipsie (viel Trinken und viel Urin), Appetitverlust, Übelkeit/Erbrechen, Obstipation, Muskelzittern oder Muskelschwäche, Lethargie und ein „träge-benommenes“ Verhalten. Viele Tiere wirken nicht dramatisch krank, sondern eher „leer“ oder „ausgeschaltet“. Das Risiko liegt jedoch in kardialen und neurologischen Komplikationen, besonders wenn Dehydratation, Azotämie und Elektrolytverschiebungen hinzukommen. In schweren Fällen kann es zu Brady- oder Tachyarrhythmien, Schwächekollaps, Hypotonie, zentralnervösen Störungen bis hin zu stuporösen Zuständen kommen. Präklinisch wird deshalb ein Verdachtscluster gelehrt, das bewusst einfach und robust ist: Tumorpatient + auffälliges Trinken/Urinieren + Schwäche/Erbrechen → Hyperkalzämie/DD. Dieses Cluster ersetzt keine Diagnostik, verhindert aber den typischen Denkfehler, die Situation als „gewöhnliche Gastritis“ abzutun.
Ein didaktischer Kernpunkt ist der Teufelskreis aus Calcium und Niere: Hyperkalzämie verschlechtert die Fähigkeit der Niere, Urin zu konzentrieren. Dadurch kommt es zu Polyurie, was Dehydratation verstärkt. Dehydratation wiederum reduziert die glomeruläre Filtration und damit die renale Calciumausscheidung. Das führt zu weiter steigenden Calciumspiegeln und noch mehr Polyurie – ein sich selbst verstärkender Kreislauf. Präklinisch wird daraus eine klare Konsequenz abgeleitet: Der Patient wird nicht durch „irgendein Mittel“ im Feld stabil, sondern durch konsequente Basismaßnahmen (Perfusion schützen, Stress reduzieren, Wärmemanagement, Transport) und durch frühzeitige klinische Therapie (gezielte Flüssigkeitstherapie, Monitoring, ggf. Diuretika/Anti-Resorptiva nach Diagnostik). Das präklinische Team wirkt primär dadurch, dass es den Zustand richtig erkennt, iatrogene Schäden vermeidet und die Behandlungskette ohne Zeitverlust in Gang setzt.
Das Vorgehen folgt dem ABCDE-Denken. In onkologischen Elektrolyt-Notfällen dominiert häufig „C“ (Circulation), weil Dehydratation, Hypovolämie und potenzielle Arrhythmien die Perfusion gefährden. Der Kurs trainiert, dass ein „ruhiger“ Patient keineswegs stabil sein muss: Ein Tier kann apathisch daliegen, leise atmen und dennoch kritisch sein, wenn Schleimhäute blass-grau wirken, die Kapillarfüllungszeit verlängert ist oder die Pulsqualität schwach wird. Gleichzeitig wird „D“ (Disability) betont: Neurologische Auffälligkeiten (Apathie, Desorientierung, Muskelzittern, Schwäche, reduzierte Reaktion) sind in Kombination mit Tumoranamnese ein starkes Warnsignal. „E“ (Exposure/Environment) umfasst Wärmeschutz und das Erkennen begleitender Auslöser wie Fieber, Schmerz, Tumorprogress oder Nebenwirkungen von Medikamenten.
Präklinisch wird keine definitive Elektrolyttherapie durchgeführt. Selbst wenn im Feld Infusionen erlaubt sind, ist das Ziel nicht „Calcium senken“, sondern Perfusion und Kreislauf zu stabilisieren. Der Kurs legt Wert auf klare Grenzen: Kein Versuch, durch „irgendwelche Zusätze“ oder unprotokollierte Medikamente die Hyperkalzämie zu behandeln. Hyperkalzämie ist zudem kein Notfall, der durch orale „Hausmittel“ verbessert wird. Im Gegenteil: forcierte orale Gabe bei Übelkeit oder reduzierter Wachheit erhöht das Aspirationsrisiko. Ein weiterer Stop-Rule-Block lautet daher: keine forcierte orale Flüssigkeit, kein Einflößen, keine hektischen Manipulationen, keine aggressiven Belastungen. Maßnahmen sollen ruhig, strukturiert und minimalinvasiv bleiben.
Die präklinische Stabilisierung konzentriert sich auf vier Achsen: (1) Stressreduktion, (2) Wärmemanagement, (3) Schonung/Transportlogistik, (4) strukturierte Anamnese + Übergabe. Stress ist bei Tumorpatienten nicht nur „unangenehm“, sondern physiologisch gefährlich: Sympathikotonus steigert Herzarbeit, verschlechtert die Kooperation (O₂-Maske, Lagerung), erhöht die Muskelaktivität und kann Arrhythmierisiken verstärken. Daher werden wenige Personen am Tier, ruhige Ansprache, leise Umgebung und kurze Handgriffe als Qualitätskriterien definiert. Wärmemanagement ist ebenso zentral: Dehydrierte, schwache Patienten kühlen leicht aus; Hypothermie kann die Kreislaufleistung mindern und die Prognose verschlechtern. Decken, Isolation gegen kalten Boden, Windschutz und – wenn verfügbar – eine sichere Wärmematte mit Abstand gehören zum Standard.
Transportlogistik wird bewusst als „Therapie“ vermittelt. Ein Patient mit Verdacht auf Hyperkalzämie sollte möglichst sanft bewegt werden; ruckartige Bewegungen, Treppenstress oder hektisches Umsetzen erhöhen den physiologischen Druck. Das Team trainiert, Transportwege freizumachen, eine stabile Lagerung zu wählen (sternal oder Seitenlage je nach Atemarbeit/Komfort), und Monitoringpunkte im Verlauf festzulegen. Da onkologische Patienten häufiger thromboembolische Ereignisse oder kardiale Komplikationen entwickeln, wird Re-Evaluation alle 5–10 Minuten als Standard gelehrt: Bewusstsein, Atemarbeit, Schleimhautfarbe, Pulsqualität, Herzfrequenztrend, Temperatur (wenn sinnvoll) und ein kurzer „Gesamttrend“ (besser/gleich/schlechter). Es zählt nicht der einzelne Messwert, sondern die Dynamik.
Eine besondere Rolle spielt die strukturierte Anamnese. Hyperkalzämie wird selten als erste Vermutung von Haltern geäußert; oft berichten sie „er trinkt so viel“ oder „er ist plötzlich so schlapp“. Der Kurs vermittelt, gezielt und effizient zu fragen, ohne zu verlieren: (1) Tumordiagnose bekannt? Welche Lokalisation? (2) letzter Behandlungsstand (OP, Chemo, Bestrahlung, Cortison, NSAIDs)? (3) Trinkmenge/Urinsituation seit wann verändert? (4) Erbrechen/Obstipation/Appetitverlust? (5) Schmerzzeichen? (6) bekannte Nierenprobleme? (7) Medikamente/Umstellungen in den letzten Tagen? (8) Verlauf: schleichend vs. plötzlich. Diese Fragen dienen nicht der Diagnose im Feld, sondern der Priorisierung und der Vorbereitung der Klinik. Die Übergabe wird dadurch belastbar und reduziert Informationsverlust – besonders in emotionalen Situationen.
In der Ausbildung wird zudem die Differenzialdiagnostik auf robuste Muster reduziert, um Überforderung zu vermeiden. Polyurie/Polydipsie + Schwäche kann auch Diabetes mellitus, Cushing, Niereninsuffizienz oder Pyometra bedeuten; Erbrechen + Apathie kann Pankreatitis, GI-Obstruktion oder Sepsis sein. Das Ziel ist nicht, im Feld „die richtige Krankheit zu erraten“, sondern eine gefährliche metabolische Entgleisung als plausible Hypothese zu markieren, Schockzeichen zu erkennen und die Klinik so zu informieren, dass Labor und Monitoring vorbereitet werden. Ein didaktischer Satz lautet: „Wenn du ein Elektrolytproblem vermutest, behandelst du es präklinisch nicht – du beschleunigst den Weg zur Messung und Therapie.“
Kommunikation mit Halter*innen ist onkologische Notfallmedizin. Viele Halter stehen unter chronischem Stress, haben Angst vor „dem Ende“ oder sind erschöpft von Diagnostik und Therapien. Gleichzeitig können sie die Dringlichkeit unterschätzen, wenn das Tier „nur schlapp“ wirkt. Der Kurs trainiert daher eine Kommunikationsstruktur: zuerst beruhigen, dann informieren, dann anleiten. Beispiel: „Ich sehe, er ist sehr schwach und ausgetrocknet. Bei Tumorpatienten kann das auch durch Stoffwechselverschiebungen kommen. Wir halten ihn jetzt warm und ruhig und fahren sofort in die Klinik, damit Blutwerte und Kreislauf überwacht werden.“ Dazu kommen klare Do-and-Don’t-Anweisungen: nicht füttern oder trinken aufzwingen, keine Hausmittel, Transportweg freihalten, Unterlagen/Medikamentenliste bereitlegen. Der Ton bleibt deeskalierend, aber bestimmt.
Die Übergabe an die Klinik folgt einem onkologie-spezifischen Schema, das im Kurs wiederholt eingeübt wird. Es enthält: (1) Verdacht (z. B. „Hyperkalzämie der Malignität in DD“), (2) Cluster/Leitsymptome (PD/PU, Erbrechen, Schwäche, Obstipation), (3) Kreislaufstatus (HF-Trend, Pulsqualität, CRT, Schleimhautfarbe), (4) Hydratationsgrad (Schleimhäute/Hautturgor), (5) neurologischer Status (Apathie/Ataxie/Zittern), (6) Temperatur (Hypothermie/Normothermie/Hyperthermie), (7) bekannte Tumordiagnose + Therapieverlauf + Medikamente, (8) präklinische Maßnahmen (Wärmeschutz, Lagerung, O₂ wenn toleriert, ggf. Infusion nach Protokoll), (9) Zeitachse (seit wann Symptome, Verlauf, Verschlechterung). Diese Struktur ist bewusst kompakt, damit sie unter Stress zuverlässig abrufbar bleibt.
Die Ausbildung betont außerdem iatrogene Risiken: Tumorpatienten reagieren empfindlicher auf Hypothermie, auf unnötigen Stress und auf wiederholte Manipulation. Auch häufiges „Nachschauen“ (Verband lösen, Tier ständig aufrichten, dauernd umpositionieren) kann mehr Schaden als Nutzen bringen. Deshalb werden „wenige, aber gute“ Handgriffe trainiert. Wenn Sauerstoffgabe das Tier stresst, wird sie nicht erzwungen. Wenn eine Maßnahme die Atemarbeit verschlechtert, wird sie abgebrochen. Die Stop-Rules lauten: Wenn Stress steigt, Atemarbeit zunimmt oder der Kreislauf kippt, reduziere Maßnahmen, stabilisiere die Basics und transportiere.
Fallbeispiele machen das Konzept greifbar. Ein typisches Szenario ist der bekannte Lymphompatient, der in den letzten zwei Tagen extrem viel trinkt, häufig uriniert, jetzt erbricht und kaum noch laufen mag. Der Lernende soll nicht „Magen-Darm“ als Enddiagnose wählen, sondern die Kombination mit Tumoranamnese als metabolische Entgleisung interpretieren. Er prüft Perfusion, erkennt Dehydratation, hält das Tier warm, reduziert Stress, organisiert Transport und meldet der Klinik „Hyperkalzämie/DD“ an. Ein weiteres Szenario ist der Analbeuteltumorpatient, der plötzlich obstipiert und schwach wirkt: Auch hier ist das Ziel, das Cluster zu erkennen, nicht zu „behandeln“.
Didaktisch wird konsequent zwischen Schadensbegrenzung und definitiver Therapie unterschieden. Definitive Maßnahmen – Labor, EKG/Monitoring, aggressive Rehydrierung, ggf. diuretische und antiresorptive Therapien, Behandlung der Tumorursache – gehören in die Klinik. Präklinisch wirkt man durch Basics: sichere Lagerung, Wärmeschutz, Stressreduktion, Perfusionsbeurteilung, klare Zeitachse und Voranmeldung. Gerade bei Hyperkalzämie ist „zu viel tun“ im Feld selten hilfreich, „das Richtige früh erkennen“ aber prognoseentscheidend. Der Lernende soll am Ende nicht nur die Pathophysiologie grob verstehen, sondern vor allem handlungssicher sein: Verdacht bilden, Risiken erklären, Stop-Rules anwenden, Transportkette führen und sauber übergeben.

Palliativkrisen sind onkologische Notfälle, bei denen Ethik, Kommunikation und Leidensreduktion mindestens so wichtig sind wie „klassische“ Vitalparameter. In vielen Einsätzen geht es nicht nur um die Frage „überlebt der Patient die nächsten Stunden?“, sondern auch um „wie erträglich sind die nächsten Stunden?“ und „welche Ziele verfolgt die Familie – Stabilisierung, Diagnostik, Symptomkontrolle oder ein würdiger Abschied?“. Der Kurs ordnet Palliativkrisen deshalb nicht als „Randthema“ ein, sondern als integralen Teil präklinischer Onkologie: Tumorpatienten eskalieren häufig aus einer chronischen Grunderkrankung heraus, haben reduzierte physiologische Reserven (Anämie, Hypoproteinämie, Kachexie, Organbeteiligung) und reagieren empfindlicher auf Stress, Hypothermie und iatrogene Fehlmaßnahmen. Präklinisch ist das Ziel doppelt: lebensbedrohliche Zustände erkennen und stabilisieren und gleichzeitig Leiden akut reduzieren, ohne die Behandlungskette zu verzögern oder Therapieziele vorwegzunehmen.
Typische Palliativkrisen sind (1) akute Schmerzexazerbationen (Tumorinfiltration, Nerveneinwuchs, Ulzerationen, pathologische Frakturen, Tumornekrosen), (2) Dyspnoe (Pleuraerguss, Lungenmetastasen, Tumor im Mediastinum, obstruktive Prozesse, sekundäre Pneumonie), (3) akute Schwäche/Kollaps (Anämie, innere Blutung, Sepsis, Elektrolytstörung wie Hyperkalzämie), (4) Erbrechen/Übelkeit (Metabolik, GI-Kompression, Medikamentennebenwirkungen), (5) neurologische Ausfälle (Hirnmetastasen, Rückenmarkskompression, Krampfanfälle, Schmerz-bedingte Unruhe). Das Kapitel betont: Palliativkrise bedeutet nicht automatisch „Terminalphase“, aber die Wahrscheinlichkeit für rasche Verschlechterung ist höher – und die Kommunikation muss diesem Spannungsfeld gerecht werden: professionell, klar, deeskalierend und respektvoll.
Die Ausbildung arbeitet mit einem praxistauglichen Rahmen aus drei Bausteinen: (A) medizinische Priorisierung nach ABCDE, (B) symptomorientierte Leidensreduktion, (C) Kommunikationsführung. ABCDE bleibt die Sicherheitsbasis: Atemweg und Atmung werden beurteilt, bevor man sich im Detail „am Tumor“ aufhängt. Gleichzeitig wird gelernt, dass bei Palliativpatienten oft mehrere Probleme parallel laufen: Eine Katze mit Pleuraerguss kann gleichzeitig schmerzhaft, hypotherm und dehydriert sein; ein Hund mit pathologischer Fraktur kann zusätzlich anämisch sein und bei Stress kollabieren. Der Rettungssanitäter soll nicht „alles lösen“, sondern robust priorisieren: Was tötet zuerst? Was lindert am meisten? Was darf ich präklinisch sicher tun, ohne Schaden zu verursachen?
Dyspnoe ist in Palliativkrisen häufig das dominierende Symptom und wird als „Atemarbeit-Notfall“ vermittelt. Beurteilt werden Körperhaltung (Orthopnoe, gestreckter Hals, Abstützen), Atemfrequenz, Atemtiefe, Geräusche, Einsatz der Bauchpresse, Zyanose und der Trend über Minuten. Das Kapitel vermittelt: Nicht die Zahl allein entscheidet, sondern die sichtbare Atemarbeit. Palliativpatienten mit Pleuraerguss wirken oft ruhiger als erwartet – sie „sparen“ Atemarbeit, bis sie plötzlich entgleisen. Präklinische Kernmaßnahmen sind daher: Stressminimierung (wenige Handgriffe, ruhige Stimme, kein Zwang), kühle Umgebungsluft, kurze Wege, sichere Lagerung (häufig sternal), und Transport mit Voranmeldung, damit in der Klinik eine Thorakozentese/Analgesie/Monitoring vorbereitet wird. Sauerstoffgabe kann hilfreich sein, aber nur, wenn sie toleriert wird. Eine wichtige Stop-Rule lautet: O₂ nicht erzwingen. Wenn Maske oder Flow-by Panik auslöst, verschlechtert sich die Dyspnoe durch Stress – dann sind Ruhe, Lagerung und schnelle Klinik wirksamer als „technisch richtige“ Sauerstoffgabe.
Schmerzkrisen werden ausdrücklich als humanitäre Priorität gelehrt. Der Kurs betont: Schmerz ist nicht nur „unangenehm“, sondern ein physiologischer Treiber von Sympathikotonus, Hyperventilation, Blutdruckschwankungen und Kooperationsverlust. Bei Tumorpatienten kann ein Schmerzanstieg zu massiver Unruhe führen, die wiederum Blutung, Dyspnoe oder Kollapsrisiko erhöht. Präklinisch wird Schmerz strukturiert erkannt: Schonhaltung, Lautäußerung, Abwehr, Tachykardie, Hecheln, Pupillenerweiterung, Unruhe/Apathie und die Reaktion auf Berührung. In der Ausbildung wird vermittelt, Analgesie protokollabhängig, kreislaufsensibel und risikoarm einzusetzen. Dabei stehen drei Prinzipien im Vordergrund: (1) so früh wie sinnvoll, weil „Transport ohne Schmerzkontrolle“ die Situation eskalieren kann; (2) so wenig wie möglich, so viel wie nötig, weil tumorassoziierte Hypovolämie/Anämie eine Überdosierung riskanter macht; (3) Re-Evaluation nach jeder Maßnahme. Wenn Analgesie präklinisch nicht erlaubt ist, werden Alternativen trainiert: sanfte Lagerung, Immobilisation/Schienung bei Frakturverdacht, Wärmeschutz (ohne Überhitzung), geringe Stimuli, ruhige Umgebung und zügiger Transport zur klinischen Schmerztherapie.
Akute Schwäche, Kollaps und „leiser Schock“ sind bei Palliativpatienten häufig. Das Kapitel stellt heraus, dass onkologische Patienten oft „kompensationsarm“ sind: Ein Blutverlust oder eine Dehydratation, die bei einem gesunden Tier noch toleriert wird, kann hier zum Kreislaufversagen führen. Daher wird Kreislaufassessment parallel zu Symptombehandlung gelehrt: Schleimhäute, CRT, Pulsqualität, Herzfrequenztrend, Extremitätentemperatur, Bewusstsein. Ein didaktischer Schlüssel lautet: „ruhig“ ist nicht gleich „stabil“. Blasse Schleimhäute, kalte Extremitäten und schwacher Puls sind Schockzeichen bis zum Beweis des Gegenteils. Präklinisch stehen Schonung, Wärmeschutz, Stressreduktion und Transport im Vordergrund; wenn Infusionen protokolliert sind, werden sie als Perfusionsstütze verstanden, nicht als definitive Therapie. Gleichzeitig wird die onkologische Differenzialdiagnostik in robusten Clustern trainiert: Kollaps + pralles Abdomen → innere Blutung/DD; Tumorpatient + viel Trinken/Urin + Schwäche → Elektrolytstörung/DD; Tumorpatient + Dyspnoe + gedämpfte Atemgeräusche → Pleuraerguss/DD.
Neurologische Palliativkrisen (Krampf, akute Ataxie, Lähmungen, starke Desorientierung) werden als Sicherheits- und Stressmanagement-Thema vermittelt. Krampfanfälle sind für Halter extrem belastend; präklinisch zählt: sichere Umgebung, Verletzungsprophylaxe, Temperaturkontrolle (Überhitzung nach Krampf vermeiden), kurze Re-Evaluation und Transport mit strukturierter Übergabe. Bei Rückenmarkskompression oder pathologischen Wirbelfrakturen wird „bewegungsarme Logistik“ trainiert: möglichst wenig Umlagern, gerade Achse, sanfte Fixation, schmerzarmes Handling. Der Kurs betont iatrogene Risiken: grobes Ziehen, hektisches Umsetzen oder Zwangspositionen können bei metastatischen Läsionen Schaden verstärken.
Ein zentrales Element in Palliativkrisen ist die Kommunikationsführung. Der Kurs lehrt ein Modell, das in hoch emotionalen Situationen funktioniert: validieren – strukturieren – Optionen erklären. Validieren heißt: Emotionen benennen, ohne zu dramatisieren („Ich sehe, das macht Ihnen große Angst.“). Strukturieren heißt: Führung übernehmen („Ich erkläre kurz, was wir jetzt tun: erst Atemarbeit beurteilen, dann warm und ruhig lagern, dann fahren wir sofort.“). Optionen erklären heißt: realistische nächste Schritte skizzieren, ohne falsche Versprechen („In der Klinik kann man z. B. Flüssigkeit aus dem Brustkorb ablassen und Schmerzmittel geben. Wir sorgen dafür, dass Sie schnell dort hinkommen.“). Wichtig: präklinisch werden Therapieziele nicht entschieden, aber sie werden respektvoll adressierbar gemacht. Der Kurs trainiert Formulierungen, die weder bagatellisieren noch entmündigen: „Wir können jetzt stabilisieren und Leiden reduzieren. Ob es um intensive Behandlung oder um Symptomkontrolle geht, besprechen Sie am besten direkt mit der Klinik – ich gebe alle Informationen strukturiert weiter.“
Recht und Ethik werden praxisnah integriert. Palliativkrisen enthalten häufig Elemente von Entscheidungsdruck („Bitte tun Sie alles!“ vs. „Ich möchte nicht, dass er leidet.“). Der Kurs vermittelt: Die Aufgabe des Rettungssanitäters ist es, im Rahmen der Protokolle sicher zu handeln, Leiden zu mindern und eine saubere Übergabe zu ermöglichen. Gleichzeitig wird Dokumentation als Schutz und als klinische Information gelehrt: Zeitachse, dominante Symptome (Atemnot/Schmerz), Vitaltrend, getroffene Maßnahmen und Reaktion, Aussagen der Halter (z. B. bekannte Diagnose, Medikation, Verlauf). Dokumentation ist hier nicht Bürokratie, sondern Risiko- und Kommunikationsmanagement – insbesondere, wenn Therapieziele in der Klinik diskutiert werden müssen.
Das Kapitel verbindet Palliativkrisen mit den allgemeinen Prinzipien onkologischer Notfälle: Onkologische Patienten eskalieren oft aus einer chronischen Grunderkrankung heraus, mit atypischen Anamnesen (schleichender Gewichtsverlust, intermittierende Schwäche) und deutlichen Reserven-Defiziten (Anämie, Hypoproteinämie). Präklinisch zählt daher ein besonders strukturiertes Vorgehen: Perfusion sichern, Schmerzen reduzieren, Stress minimieren, Wärmemanagement, Transport und Voranmeldung. ABCDE bleibt der Sicherheitsrahmen; bei Tumorpatienten ist „C“ häufig kritisch (okkulte Blutung, Hämoperitoneum, Gerinnungsstörung), bei Palliativkrisen ist zusätzlich „B“ (Dyspnoe) sehr häufig dominant. Der Lernende übt, die Symptomdominanz klar zu benennen und danach zu handeln: „Primär Atemnot, sekundär Schmerz“ oder „Primär Schmerzkrise, sekundär Kreislaufgrenzwertig“.
Die Voranmeldung wird als entscheidender Baustein trainiert, weil sie klinische Vorbereitung ermöglicht. Bei Dyspnoe bedeutet das: Thorakozentese-Set, Monitoring, Sedations-/Analgesie-Plan. Bei Schmerzkrise bedeutet das: Analgesie-Plan, ggf. Bildgebung, Lagerungshilfen. Bei Kollaps bedeutet das: Schockraum-Setup, Blutbild/Ultraschall-Option, Transfusionsbereitschaft. Das Schema für die Übergabe ist onkologie-spezifisch und zugleich knapp: Tumorart/Ort (wenn bekannt), aktueller Behandlungsstand (OP/Chemo/Bestrahlung, Steroide/NSAIDs), dominante Symptome, Vitalparametertrend (HF/AF/CRT/Temperatur/Bewusstsein), präklinische Maßnahmen und deren Wirkung, Zeitachse (Beginn, Eskalation, Reaktion).
Fallbeispiele sind bewusst realistisch und emotional. Ein typisches Szenario: Katze mit bekannten Metastasen entwickelt akute Atemnot. Halter panisch, Tier in Orthopnoe. Der Lernende trainiert: wenige Personen, ruhige Stimme, sternal lagern, kühle Luft, O₂ nur wenn toleriert, Transport ohne Verzögerung, Voranmeldung „Dyspnoe, Verdacht Pleuraerguss“. Zweites Szenario: Hund mit Knochentumor schreit bei Bewegung, kann nicht mehr aufstehen. Der Lernende trainiert: Schmerzerkennung, schonende Immobilisation, Wärmeschutz, Transportlogistik, Kommunikation („Wir bewegen ihn so wenig wie möglich und sorgen dafür, dass er schnell Schmerztherapie bekommt.“). Drittes Szenario: Tumorpatient mit intermittierender Schwäche und akutem Kollaps. Der Lernende trainiert: Schockzeichen erkennen, keine unnötige Manipulation, Wärmeschutz, O₂ wenn toleriert, klare Voranmeldung „onkologischer Patient, Kollaps, Schockzeichen“.
Didaktisch wird konsequent zwischen „Schadensbegrenzung“ und „definitiver Therapie“ unterschieden. Definitive Maßnahmen wie Thorakozentese, Transfusionen, chirurgische Blutstillung, aggressive Analgesie/Sedation oder spezifische onkologische Interventionen gehören in die Klinik. Präklinisch wirkt man durch Basics – aber diese Basics sind in Palliativkrisen oft prognose- und leidensentscheidend: ruhige Lagerung, Wärmeschutz, Stressreduktion, symptomorientierte Maßnahmen im Protokoll, und eine saubere Zeitachse. Der Lernende soll am Ende in der Lage sein, Palliativkrisen im Team zu führen: Rollen verteilen (Kommunikation vs. Monitoring vs. Transportlogistik), Materialmanagement (Decken/Wärmematte, O₂-Option, Fixation), Voranmeldung und strukturierte Übergabe – ohne Übertherapie, ohne Hektik, mit maximaler Patientensicherheit und maximalem Respekt für Halter und Tier.

Der Praxisalgorithmus bündelt die häufigsten onkologischen Notfallmuster im präklinischen Setting zu einer klaren, wiederholbaren Handlungslogik. Ziel ist nicht „Onkologie im Feld“, sondern sichere Schadensbegrenzung, frühes Erkennen kritischer Muster, Teamführung und eine klare, klinikfähige Übergabe. Onkologische Patienten sind dabei besonders anspruchsvoll, weil sie häufig lange kompensieren und dann abrupt dekompensieren. Außerdem liegen oft Reserven-Defizite vor (Anämie, Hypoproteinämie, Kachexie, reduzierte kardiorespiratorische Toleranz), die dazu führen, dass „mittlere“ Belastungen (Stress, Blutverlust, Transporthast, Hypothermie) unverhältnismäßig große klinische Folgen haben. Der Algorithmus arbeitet deshalb mit zwei Leitgedanken: „Trend statt Momentaufnahme“ und „Basics wirken am stärksten“.
Algorithmus – Vier Module: (1) ABCDE als Sicherheitsrahmen, (2) Blutung vs. innere Blutung als häufigstes „C“-Problem in der Onkologie, (3) metabolische Entgleisung (z. B. Hyperkalzämie) und palliative Krise als typische Eskalationsformen, (4) Re-Evaluation + Übergabe als Qualitätsanker. Jedes Modul enthält Stop-Rules, um iatrogene Schäden zu vermeiden (z. B. Verbände nicht ständig lösen, keine aggressive „Korrektur“ im Feld, O₂ nicht erzwingen, keine manipulativen Eingriffe ohne Protokoll). Didaktisch wird betont: Ein gutes präklinisches Ergebnis entsteht meist nicht durch „viel tun“, sondern durch richtig priorisieren, ruhig führen und früh kommunizieren (Team und Klinik).
(1) ABCDE – der Sicherheitsrahmen
A/B: Atemweg und Atmung haben Priorität, auch wenn Blutung oder Tumor dramatisch wirken. Onkologische Patienten entwickeln Dyspnoe durch Pleuraerguss, Metastasen, Anämie oder sekundäre Infektionen. Beurteilt werden Atemarbeit, Körperhaltung (sternal/Orthopnoe), Geräusche, Zyanose, Trend. Prinzip: So wenig Stress wie möglich. Ruhige Umgebung, wenige Handgriffe, kurze Wege, kühle Luft. Sauerstoffgabe nur, wenn toleriert; Panik verschlechtert Dyspnoe und kann die Dekompensation triggern.
C: Kreislaufassessment ist bei Tumorpatienten zentral. Schleimhäute, CRT, Pulsqualität, Herzfrequenztrend, Extremitätentemperatur, Bewusstsein. Der Kurs lehrt explizit: „ruhig“ ist nicht gleich „stabil“. Ein Patient kann apathisch wirken und gleichzeitig im Schock sein. Bei „C“-Problemen wird Schonung priorisiert: sanfte Lagerung, Wärmeschutz, Stressreduktion, Transport. Wenn Infusionen protokolliert sind, werden sie als Perfusionsstütze titriert, nicht als definitive Therapie.
D/E: Neurologischer Status (Apathie, Desorientierung, Krampf), Temperaturmanagement und Gesamtexposition. Hypothermie ist bei onkologischen Patienten häufig (Anämie, Sepsis, Kachexie) und verschlechtert Gerinnung und Kreislauf. Wärmemanagement wird als Therapie verstanden: Decken, Isolation, Wärmematte (sicher), Windschutz, ohne Überhitzung.
(2) Blutung vs. innere Blutung – „C“ mit Stop-Rules
Onkologische Blutungen reichen von ulzerierten Hauttumoren über Maulhöhlen-/Nasentumoren bis zu okkulten Blutungen (Hämoperitoneum, tumorassoziierte Koagulopathie). Präklinisch entscheidet die erste Weiche: äußere Blutung mechanisch beeinflussbar oder Verdacht innere Blutung?
Äußere Blutung: Ziel ist nicht perfekte Hämostase, sondern Blutverlust reduzieren, Gewebe schützen, Schock vermeiden, Transport. Standard: direkte Kompression (sterile Kompressen), dann Druckverband „so fest wie nötig, so locker wie möglich“. Stop-Rules: Verband nicht ständig abnehmen (Gerinnselabriss), keine aggressiven Spülungen, keine Hausmittel. In Maulhöhle/Nase sind Verbände schwierig; hier dominieren Kompression (nur wenn sicher), kühle Umgebung, Stressreduktion, schnelle Klinik.
Innere Blutung: Verdacht entsteht durch Kollaps, blasse Schleimhäute, schwachen Puls, kalte Extremitäten, evtl. prallen/gespannten Bauch. Bewegung kann Blutung verstärken; deshalb werden sanfte Umlagerung, Schonung, Wärmeschutz und rascher Transport trainiert. Sauerstoff kann bei Anämie sinnvoll sein, ersetzt aber nicht Transfusion/Chirurgie. Voranmeldung: „Verdacht Hämoperitoneum/Milztumor, Schockzeichen, Kollaps-Episoden“ – damit Klinik Ressourcen (Schockraum, Ultraschall, Blutprodukte) vorbereitet.
(3) Metabolische Entgleisung und palliative Krise erkennen
Onkologische Notfälle eskalieren nicht nur durch Blutung, sondern auch durch metabolische Syndrome und palliative Krisen. Der Algorithmus lehrt, aus wenigen robusten Befunden eine plausible Verdachtshypothese zu formulieren und diese klar zu kommunizieren.
Hyperkalzämie-Verdacht: „Tumorpatient + Polyurie/Polydipsie + Schwäche/Erbrechen/Obstipation“ ist ein Verdachtscluster. Präklinisch wird keine definitive Elektrolyttherapie durchgeführt; Stabilisierung und Voranmeldung sind entscheidend. Dehydratation verschlechtert die Nierenfunktion, reduzierte Nierenfunktion verschlechtert die Hyperkalzämie – ein Teufelskreis. Deshalb: Wärmeschutz, Stressreduktion, vorsichtige Lagerung, Transport; Infusionen (wenn erlaubt) zur Perfusion, nicht als „Heilung“.
Palliative Krise: Dominante Symptome sind häufig Dyspnoe (Pleuraerguss/Metastasen), Schmerzexazerbation (Tumorinfiltration, Fraktur), akute Schwäche oder neurologische Ausfälle. Präklinisch gilt: lebensbedrohliche Zustände erkennen und stabilisieren und Leiden reduzieren. Kommunikation folgt einem Trainingsmodell: validieren („Ich sehe, das ist gerade sehr belastend.“), strukturieren („Wir gehen jetzt Schritt für Schritt vor.“), Optionen erklären („In der Klinik kann man z. B. Flüssigkeit ablassen oder Schmerztherapie geben.“). Der Algorithmus verhindert Übertherapie: keine erzwungene O₂-Maske bei Panik, keine hektischen Manipulationen, keine unnötigen Transporteinbauten, die Stress steigern.
(4) Re-Evaluation und Übergabe – die Qualitätskerne
Der Algorithmus definiert Trendbeobachtung als Kernfertigkeit, weil onkologische Patienten abrupt dekompensieren können. Der Lernende trainiert kurze Re-Check-Intervalle (z. B. alle 5–10 Minuten oder bei jeder Veränderung): HF, AF, CRT, Schleimhautfarbe, Pulsqualität, Temperatur, Bewusstsein und – wenn relevant – Atemarbeit (nicht nur Frequenz). Re-Evaluation ist nicht „optional“, sondern ein aktiver Schutz vor Fehlinterpretationen: Ein Patient kann nach kurzer Beruhigung oder nach Kompression kurzfristig besser wirken, aber weiterhin kritisch bleiben (fortschreitende innere Blutung, Arrhythmie, zunehmende Dyspnoe). Deshalb wird eine Stop-Rule gelehrt: Transport nicht abbrechen, nur weil es kurz besser wird.
Teamführung im Algorithmus
Onkologische Einsätze sind oft chaotisch: emotionale Halter*innen, mehrere Tiere, beengte Wohnsituation, Blut, Geruch, Zeitdruck. Der Kurs trainiert Führung als medizinischen Skill. Rollenverteilung wird explizit geübt: (1) Teamlead/Kommunikation, (2) Monitoring/Vitalwerte/Trend, (3) Maßnahmen (Kompression, Wärmeschutz, Lagerung), (4) Logistik (Transportweg, Trage, Auto, Kliniktelefonat). Materialmanagement ist Teil der Patientensicherheit: Decken/Wärmematte, sterile Kompressen, Verbandsmaterial, O₂-Option, Schutzkragen (bei Reiben/Ulzera), Müllbeutel/Entsorgung. Ein wiederkehrender Punkt ist „kurze Manipulationsdauer“: Jede zusätzliche Minute „Herumprobieren“ erhöht Stress, Hypothermie und Blutungsrisiko.
Voranmeldung – klinische Ressourcen gezielt aktivieren
Die Ausbildung legt Wert darauf, nicht nur Symptome zu melden („blutet“, „atmet schwer“), sondern Verdachtsmuster, die Ressourcen steuern: „Verdacht Hämoperitoneum/Milztumor“, „Tumorblutung schwer kontrollierbar“, „Hyperkalzämie-Verdacht“, „palliative Dyspnoe“, „Schmerzkrise/pathologische Fraktur“. Damit kann die Klinik OP-Bereitschaft, Ultraschall, Blutprodukte, Thorakozentese-Set, Analgesie/Sedation oder Monitoring vorbereiten. Die Voranmeldung wird in einem kurzen Schema trainiert: Was ist die Verdachtshypothese? – Wie ist der aktuelle Status? – Was wurde präklinisch getan? – Wie ist der Trend? – ETA (Ankunft in X Minuten).
Übergabe – onkologie-spezifisch, aber kompakt
Die Übergabe an die Klinik folgt einem onkologie-spezifischen Schema, das Informationsverlust reduziert: (1) Tumorart/Ort (wenn bekannt), (2) letzter Behandlungsstand (OP, Chemo, Bestrahlung), (3) aktuelle Medikation (NSAIDs, Steroide, ggf. Antikoagulanzien/sonstige), (4) dominante Symptome (Blutung/Kollaps/Dyspnoe/Schmerz/neurologisch), (5) Vitalparametertrend (HF/AF/CRT/Temp/Bewusstsein), (6) präklinische Maßnahmen und Reaktion (Kompression/Druckverband, Wärmeschutz, Lagerung, O₂ toleriert ja/nein), (7) Zeitachse (Beginn, Eskalation, Verlauf). Der Kurs betont: Zeitachse objektiviert Dringlichkeit – insbesondere bei Blutungen und Dyspnoe.
Dokumentation und Kommunikation als Patientensicherheit
Dokumentation wird im Algorithmus als Sicherheitsnetz und als klinische Information verstanden, nicht als „Papier“. Erfasst werden Zeitpunkte, Befunde, Maßnahmen, Reaktionen, Aussagen der Halter*innen (z. B. „Tumor seit Monaten“, „letzte Chemo vor 2 Wochen“, „seit heute Morgen Blutung“, „trinkt extrem“). Kommunikation ist dabei ein aktiver Schutz vor iatrogenen Schäden: Halter werden von riskanten Handlungen abgehalten („Bitte nicht am Verband ziehen“, „Bitte nichts einflößen“, „Bitte Tier nicht laufen lassen“, „Transportweg frei“). Die Ausbildung vermittelt „ruhige, klare, kurze Sätze“ und eine informierte Dringlichkeit, ohne Panik zu erzeugen. Gleichzeitig wird Palliativ respektvoll adressiert: Ziel kann Stabilisierung sein, aber auch Leidensreduktion – präklinisch wird das erwähnt, ohne Therapieziele vorwegzunehmen oder Druck auszuüben.
Grenzen präklinischer Therapie – klar benennen
Der Algorithmus betont konsequent die Grenzen: definitive Blutstillung, Transfusionen, Chirurgie, Elektrolyt-/Calcium-Management, Antiarrhythmika, Thorakozentese oder onkologische Interventionen gehören in die Klinik. Präklinisch wirkt man durch Basics: Schonung, Wärmeschutz, Blutungskontrolle, O₂ wenn toleriert, Stressreduktion und eine saubere Zeitachse. Genau diese Basics entscheiden aber oft über Prognose und Leidensniveau, weil sie Dekompensation verhindern oder verzögern, bis die definitive Therapie greift.
Single-Choice: pro Frage eine richtige Antwort. Bestehensgrenze: 70%. (Fragen & Antworten werden gemischt.)
Onko-Notfall – innere Blutung erkennen → schockschonend stabilisieren → Voranmeldung/Transport.
Bereit. Klicke auf „Simulation starten“.