SACHVERSTÄNDIGENBÜRO

Ausbildungsplattform (Tier-Notruf)
Ziel: Trend erkennen (besser/schlechter) statt Einzelwerte „schönrechnen“.
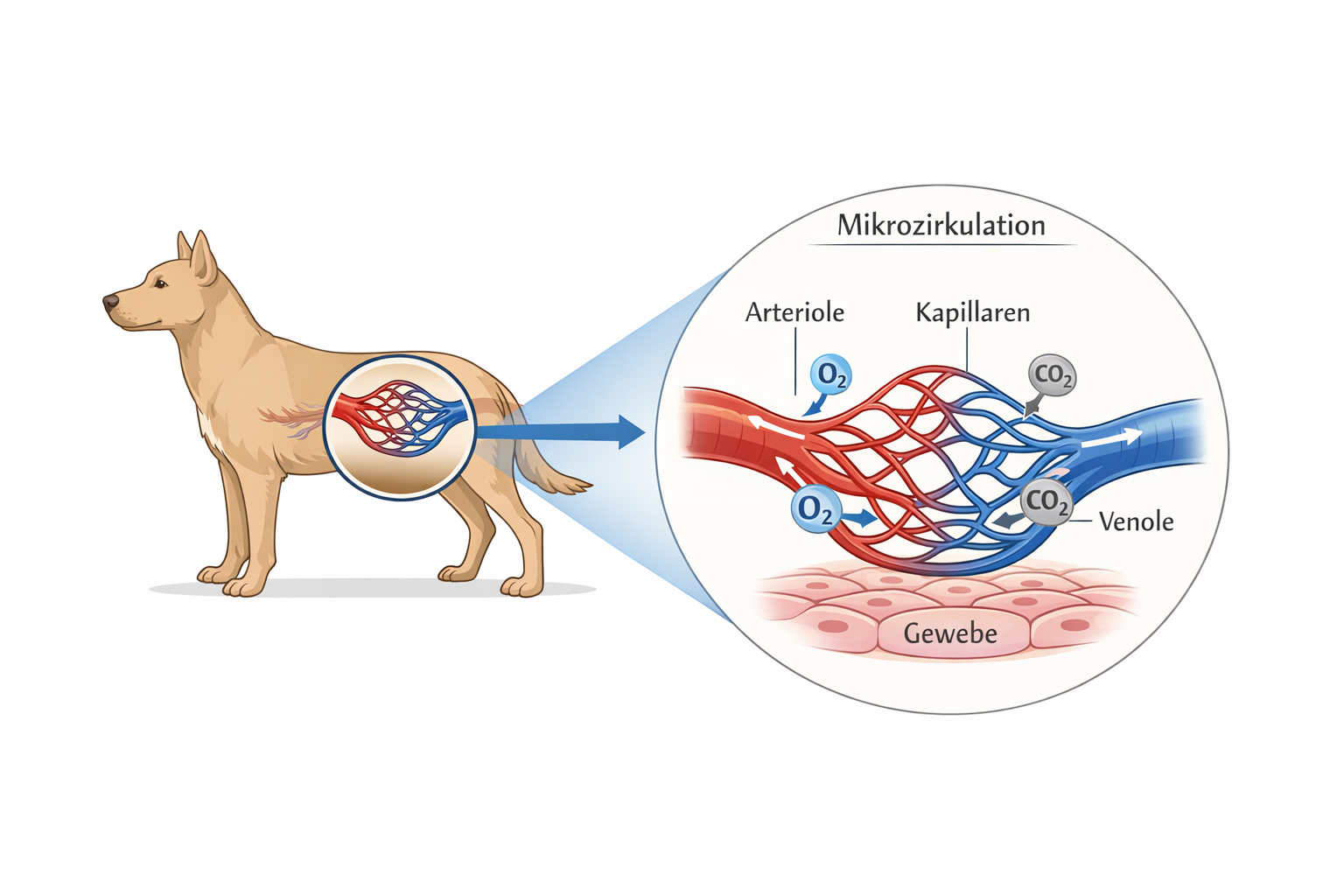
Der Schock stellt in der tiermedizinischen Notfallversorgung kein isoliertes Krankheitsbild dar, sondern ein zeitkritisches, potenziell letales Syndrom, das durch eine unzureichende effektive Gewebeperfusion und damit durch ein Missverhältnis zwischen Sauerstoffangebot (DO₂) und Sauerstoffbedarf der Zellen gekennzeichnet ist. Entscheidend ist das Verständnis, dass ein „akzeptabler Blutdruck“ nicht automatisch eine adäquate Mikrozirkulation bedeutet. Makrozirkulatorische Parameter wie systolischer Druck oder tastbarer Puls können noch im Normbereich liegen, während die Kapillardurchblutung bereits erheblich eingeschränkt ist und die zelluläre Sauerstoffextraktion versagt. Klinische Stabilität kann daher eine trügerische Momentaufnahme sein.
Physiologisch ergibt sich das Sauerstoffangebot aus dem Herzzeitvolumen multipliziert mit dem arteriellen Sauerstoffgehalt. Das Herzzeitvolumen wiederum ist das Produkt aus Herzfrequenz und Schlagvolumen. Das Schlagvolumen hängt von Vorlast, Nachlast und myokardialer Kontraktilität ab. Der arterielle Sauerstoffgehalt wird primär durch die Hämoglobinkonzentration und die Sauerstoffsättigung bestimmt; der physikalisch gelöste Sauerstoff spielt demgegenüber eine untergeordnete Rolle. Jede Störung entlang dieser Kette – Blutverlust, Hypoxämie, Pumpversagen oder ausgeprägte Vasodilatation – kann zu einer Reduktion des effektiven Sauerstoffangebotes führen.
In frühen Schockstadien dominieren kompensatorische Mechanismen des sympathoadrenalen Systems. Durch Freisetzung von Noradrenalin und Adrenalin steigen Herzfrequenz und Kontraktilität, während der systemische Gefäßwiderstand zunimmt. Diese Reaktion stabilisiert kurzfristig den arteriellen Blutdruck, geht jedoch mit einer Umverteilung des Blutflusses einher. Periphere Kompartimente wie Haut, Skelettmuskulatur und Splanchnikusgebiet werden zugunsten lebenswichtiger Organe wie Herz und Gehirn minderdurchblutet. Klinisch äußert sich diese Zentralisation durch blasse oder graue Schleimhäute, verlängerte Rekapillarisierungszeit, kalte Extremitäten, Tachykardie und einen schmalen, häufig „fadenförmigen“ Puls.
Parallel werden das Renin-Angiotensin-Aldosteron-System sowie das antidiuretische Hormon (ADH) aktiviert, um intravasales Volumen zu erhalten. Natrium- und Wasserretention stabilisieren vorübergehend die Kreislaufsituation, können jedoch bei persistierender Ursache die Mikrozirkulation zusätzlich beeinträchtigen. Vasokonstriktion auf Kapillarebene verschlechtert die Gewebeperfusion trotz scheinbar stabiler Makroparameter. Diese Diskrepanz zwischen Makro- und Mikrozirkulation ist klinisch bedeutsam und erklärt, weshalb Hypotonie häufig erst als Spätzeichen eines bereits fortgeschrittenen Schocks auftritt.
Auf zellulärer Ebene führt anhaltende Hypoperfusion zur Umstellung von aerober oxidativer Phosphorylierung auf anaerobe Glykolyse. Die ATP-Produktion sinkt, während Laktat akkumuliert und eine metabolische Azidose entsteht. Azidose reduziert die myokardiale Kontraktilität und die Gefäßreaktivität auf Katecholamine. Gleichzeitig versagen energieabhängige Ionenpumpen, wodurch intrazelluläres Natrium und Wasser ansteigen und ein Zellödem entsteht. Eine Kalziumüberladung aktiviert proteolytische und lipolytische Enzymkaskaden, die strukturelle Zellschäden verstärken. Persistiert dieser Zustand, entwickelt sich eine mitochondriale Dysfunktion mit fortschreitendem Organversagen.
Das Endothel spielt in diesem Prozess eine aktive Rolle. Die endotheliale Glykokalyx und interzelluläre Tight Junctions werden geschädigt, wodurch die Kapillarpermeabilität zunimmt. Es kommt zur Flüssigkeitsverschiebung ins Interstitium und damit zu einer funktionellen Hypovolämie. Gleichzeitig werden proinflammatorische Zytokine wie TNF-α, IL-1 und IL-6 freigesetzt, die eine systemische inflammatorische Antwort (SIRS) auslösen können. Koagulation und Inflammation sind eng miteinander verknüpft; Mikrothromben auf Kapillarebene verschärfen die Perfusionsheterogenität. Trotz makrozirkulatorischer Stabilisierung bleiben Gewebeinseln ischämisch, was die Diskrepanz zwischen gemessenen Druckwerten und tatsächlicher Sauerstoffversorgung erklärt.
Didaktisch ist die Unterscheidung verschiedener Schockstadien hilfreich. Im kompensierten Stadium erscheinen Blutdruck und Bewusstseinslage häufig noch relativ stabil, während Tachykardie und verlängerte Rekapillarisierungszeit frühe Warnzeichen darstellen. Im dekompensierten Stadium treten Hypotonie, deutliche Bewusstseinsstörungen und ein schwacher Puls hinzu. Das irreversible Stadium ist durch schwere mitochondriale Dysfunktion, therapieresistente Hypotonie und Multiorganversagen gekennzeichnet. Ein praxisrelevanter Merksatz lautet: Hypotonie ist meist ein Spätzeichen, während Tachykardie und veränderte Kapillarfüllzeit oft frühe Hinweise liefern.
Für die präklinische Einschätzung ist die konsequente Integration aller Befunde erforderlich. Die Beurteilung der Schleimhäute hinsichtlich Farbe und Feuchtigkeit sowie die Messung der Rekapillarisierungszeit liefern unmittelbare Hinweise auf Perfusionsqualität und sympathischen Tonus. Gleichzeitig müssen Herzfrequenz, Pulsqualität, Atemmuster und mentale Lage in die Bewertung einbezogen werden. Einzelwerte dürfen nicht isoliert interpretiert werden. Ein klinisch scheinbar stabiler Zustand kann eine fragile Kompensation darstellen, die bei zusätzlicher Belastung – beispielsweise Transportstress oder Blutverlustprogression – abrupt kollabiert.
Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter erheblich verschieben. Eine stressbedingte Tachykardie darf nicht mit adäquater Perfusion verwechselt werden. Umgekehrt kann eine nachlassende Herzfrequenz bei fortschreitender Erschöpfung ein Zeichen drohender Dekompensation sein. Die Aussagekraft steigt erheblich, wenn Befunde wiederholt erhoben und im zeitlichen Verlauf dokumentiert werden. Trendbeobachtungen sind in der Notfallmedizin häufig aussagekräftiger als Einzelmessungen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies: Atemwegssicherung und Oxygenierung, konsequente Blutungskontrolle, Wärmeerhalt zur Vermeidung einer hypothermiebedingten Koagulopathie sowie rascher Transport in eine Einrichtung mit Möglichkeiten zur definitiven Blutungskontrolle, Bildgebung und intensivmedizinischen Therapie. Ziel sind nicht „schöne Zahlen“, sondern die Begrenzung sekundärer Schäden wie Hypoxie, Hypothermie und Azidose.
Eine klare Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. hämorrhagisch, distributiv, kardiogen), Schockform, Stadium, Prioritäten und Transportziel müssen eindeutig benannt werden. Strukturierte Dokumentation unterstützt die klinische Weiterbehandlung und schafft Transparenz im Entscheidungsprozess. Die präklinische Versorgung endet nicht mit einer scheinbaren Stabilisierung von Makroparametern, sondern mit der sicheren Übergabe in eine weiterführende Behandlung.
Ziel: „Time to definitive care“ verkürzen – das ist Teil der Therapie.
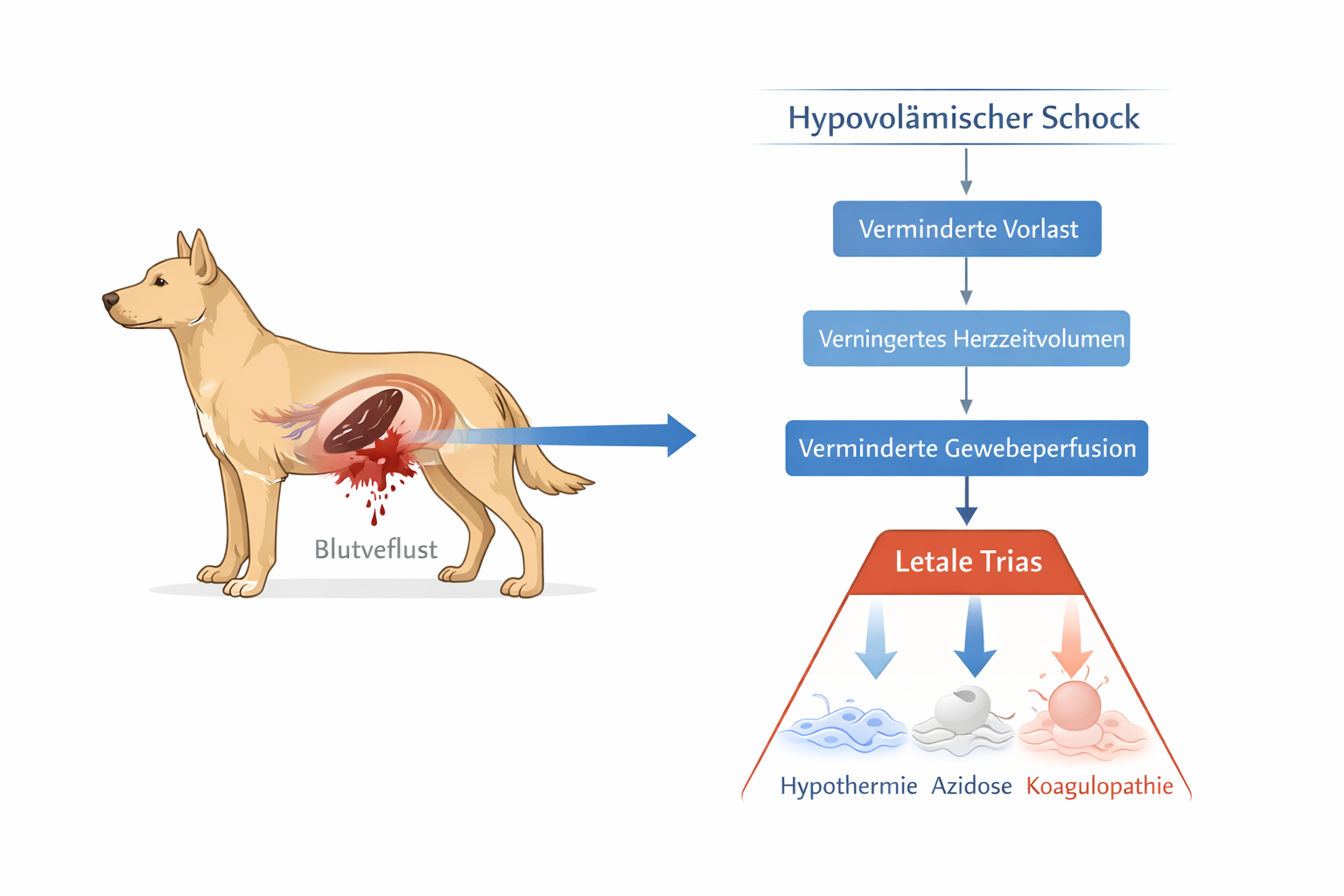
Der hypovolämische Schock ist in der präklinischen Tierrettung die häufigste und zugleich klinisch bedeutsamste Schockform im Kontext von Trauma, inneren Blutungen oder schwerer Dehydratation. Pathophysiologisch beruht er auf einem absoluten Verlust des intravasalen Volumens. Dieser Volumenverlust kann akut durch äußere oder innere Blutungen entstehen oder subakut durch Flüssigkeitsdefizite, etwa infolge massiver gastrointestinaler Verluste. Entscheidend ist, dass die zirkulierende Blutmenge nicht mehr ausreicht, um eine adäquate Vorlast und damit ein ausreichendes Schlagvolumen zu gewährleisten.
Zu Beginn sinkt der venöse Rückstrom zum Herzen. Die reduzierte Ventrikelfüllung führt unmittelbar zu einer Abnahme des Schlagvolumens und somit des Herzzeitvolumens. Der Organismus reagiert mit einer ausgeprägten Aktivierung des sympathoadrenalen Systems. Herzfrequenz und Kontraktilität steigen, während periphere Gefäße vasokonstrigieren, um den systemischen Gefäßwiderstand zu erhöhen. Gleichzeitig werden Renin-Angiotensin-Aldosteron-System und ADH aktiviert, um Flüssigkeit im Gefäßsystem zu halten. Diese Mechanismen stabilisieren kurzfristig den arteriellen Blutdruck, können jedoch die zugrunde liegende Perfusionsstörung nicht kompensieren. Der Blutdruck kann in frühen Phasen noch im Referenzbereich liegen, obwohl die Mikrozirkulation bereits kompromittiert ist.
Klinisch äußert sich der kompensierte hypovolämische Schock typischerweise durch blasse oder graue Schleimhäute, verlängerte Rekapillarisierungszeit, Tachykardie und einen schwachen peripheren Puls. Kalte Akren sind Ausdruck der peripheren Vasokonstriktion. Tiere wirken häufig unruhig, angespannt oder schmerzreaktiv. Mit fortschreitendem Volumenverlust erschöpfen sich die Kompensationsmechanismen. Es folgen Apathie, Hypotonie, Kollaps und gegebenenfalls Bewusstlosigkeit. Hypotonie ist dabei meist ein Spätzeichen und darf nicht als Frühindikator missverstanden werden.
Besonders kritisch sind innere Blutungen, da sie äußerlich nicht erkennbar sind. Splenische oder hepatische Rupturen, retroperitoneale Blutungen bei Beckenfrakturen oder intrathorakale Blutverluste können innerhalb kurzer Zeit ein erhebliches Defizit verursachen. Ein Tier kann initial noch gehfähig und ansprechbar erscheinen, während die Blutung fortschreitet. Diese scheinbare Stabilität beruht auf einer effektiven, jedoch fragilen Kompensation durch Sympathikusaktivierung. Jede zusätzliche Belastung – Stress, Umlagerung, Transport – kann das Gleichgewicht abrupt kippen lassen.
Mit zunehmendem Blutverlust sinkt die Sauerstofflieferung in die Peripherie. Die Zellen wechseln von aerober Energiegewinnung zur anaeroben Glykolyse, wodurch Laktat akkumuliert und eine metabolische Azidose entsteht. Azidose beeinträchtigt die Myokardkontraktilität und reduziert die Gefäßreaktivität auf Katecholamine. Gleichzeitig verschlechtert sich die Gerinnungsfunktion. An diesem Punkt entwickelt sich die sogenannte „letale Trias“ des Traumas: Hypothermie, Azidose und Koagulopathie. Diese drei Faktoren verstärken sich gegenseitig und bilden einen selbstverstärkenden Kreislauf.
Hypothermie entsteht präklinisch leicht. Schockbedingte periphere Vasokonstriktion reduziert die Wärmeverteilung, während verminderte Stoffwechselaktivität die Wärmeproduktion senkt. Zusätzlich wirken Umgebungseinflüsse wie kalter Untergrund, Nässe oder Wind. Hypothermie hemmt enzymatische Gerinnungsreaktionen und verstärkt die Blutungsneigung. Die Koagulopathie resultiert nicht nur aus Verdünnung durch Flüssigkeitsverschiebungen, sondern auch aus Verbrauch von Gerinnungsfaktoren und endothelialer Schädigung. Mikrothromben können die Mikrozirkulation zusätzlich beeinträchtigen, sodass trotz Makrostabilisierung weiterhin ischämische Gewebeareale bestehen.
Die präklinische Konsequenz ist eindeutig: Blutungskontrolle hat höchste Priorität. Sichtbare Blutungen werden mittels Druckverband oder – bei geeigneter Indikation – Tourniquet versorgt. Tiefe Wunden können tamponiert werden. Gleichzeitig ist konsequenter Wärmeerhalt essenziell, um die letale Trias zu unterbrechen. Sauerstoffgabe unterstützt die Maximierung des arteriellen Sauerstoffgehalts. Stressreduktion und zügiger Transport sind zentrale Maßnahmen, da die definitive Blutungskontrolle in der Regel chirurgisch erfolgen muss. Bei Verdacht auf innere Blutung ist die Zeit bis zur operativen Versorgung prognoseentscheidend. Eine übermäßige Vor-Ort-Diagnostik ohne therapeutische Konsequenz verschlechtert die Überlebenschancen.
Die Unterscheidung zwischen Makro- und Mikrozirkulation bleibt auch beim hypovolämischen Schock bedeutsam. Ein tastbarer Puls oder ein noch akzeptabler systolischer Druck schließen eine kritische Kapillarperfusionsstörung nicht aus. Die Beurteilung der Schleimhäute hinsichtlich Farbe und Feuchtigkeit sowie die Messung der Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Qualität der Gewebeperfusion. Wiederholte Reevaluation im Minutenabstand erhöht die diagnostische Sicherheit erheblich. Trendbeobachtungen sind aussagekräftiger als Einzelwerte.
Gerade bei Hund und Katze können Stress und Schmerz Herz- und Atemfrequenz beeinflussen, ohne dass die zugrunde liegende Perfusionsstörung beseitigt wäre. Eine stressbedingte Tachykardie darf nicht als Zeichen hämodynamischer Stabilität interpretiert werden. Ebenso kann eine scheinbare Beruhigung Ausdruck beginnender Dekompensation sein. Die präklinische Einschätzung erfordert daher stets die Integration aller klinischen Parameter in ein konsistentes Gesamtbild.
Eine klare Begrifflichkeit erleichtert die Kommunikation im Team: Ursache (z. B. hämorrhagisch), Stadium (kompensiert oder dekompensiert), Prioritäten (Blutungskontrolle, Wärmeerhalt, Oxygenierung) und Transportziel müssen eindeutig benannt werden. Jede Maßnahme wird mit einer Reevaluation verknüpft: Verbessert sich die Rekapillarisierungszeit? Wird der Puls kräftiger? Verändert sich die mentale Reaktion? Diese strukturierte Vorgehensweise reduziert das Risiko, kritische Dynamiken zu übersehen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies, sekundäre Schäden zu begrenzen und den Patienten so rasch wie möglich einer Einrichtung zuzuführen, die chirurgische Blutungskontrolle und intensivmedizinische Stabilisierung leisten kann. Ein scheinbar stabiler Zustand darf nicht zu trügerischer Sicherheit führen; die Kompensation kann jederzeit in eine rasche Dekompensation übergehen.
Merksatz: „Warme Extremitäten“ schließen kritische Mikrozirkulationsstörung nicht aus.
Der distributive Schock umfasst Zustände, bei denen das Gesamtvolumen im Organismus nicht primär fehlt, der Gefäßtonus und die intravasale Verteilung jedoch so gestört sind, dass das effektive zirkulierende Volumen abnimmt und die Gewebeperfusion zusammenbricht. Im Gegensatz zum hypovolämischen Schock steht nicht der absolute Volumenverlust am Beginn, sondern eine ausgeprägte Vasodilatation mit Fehlverteilung des Blutflusses („Maldistribution“) und häufig zusätzlich ein Kapillarleck, das sekundär zu einer relativen und absoluten Hypovolämie führt. Klinisch ist entscheidend, dass auch bei scheinbar ausreichendem oder sogar erhöhtem Herzzeitvolumen die Mikrozirkulation und die Sauerstoffextraktion im Gewebe schwer gestört sein können. Typische Formen in der Tiernotfallmedizin sind der anaphylaktische und der septische Schock; seltener treten neurogene Mechanismen oder toxische Vasoplegie als Auslöser in den Vordergrund.
Anaphylaktischer Schock: Beim anaphylaktischen Schock handelt es sich um eine akute, systemische Hypersensitivitätsreaktion, die häufig IgE-vermittelt abläuft. Nach Allergenexposition kommt es zur Mastzell- und Basophilen-Degranulation mit Freisetzung von Mediatoren wie Histamin, Leukotrienen, Prostaglandinen und weiteren vasoaktiven Substanzen. Diese führen zu einer generalisierten Vasodilatation, erhöhter Kapillarpermeabilität (Kapillarleck) und häufig zu Bronchokonstriktion sowie Schleimhautödem. Pathophysiologisch resultiert daraus eine rasche Reduktion des venösen Rückstroms (Vorlastabfall) durch Vasodilatation und Flüssigkeitsverschiebung ins Interstitium, während gleichzeitig die Atemwege durch Ödeme oder Bronchospasmus bedroht sein können. Klinisch können innerhalb von Minuten Schwäche, Kollaps, Tachykardie, Hypotonie, Erbrechen, Durchfall, Hypersalivation, Urtikaria, pruritische Hautreaktionen sowie Dyspnoe auftreten. Bei Hund und Katze ist das Erscheinungsbild variabel: Bei Hunden stehen nicht selten gastrointestinale Symptome und Kreislaufversagen im Vordergrund, während bei Katzen respiratorische Symptome (Bronchokonstriktion, Dyspnoe) stärker betont sein können. Präklinisch muss deshalb stets beides konsequent adressiert werden: Kreislaufstabilisierung und Atemwegssicherung/Oxygenierung, wobei eine rasche Verschlechterung jederzeit möglich ist.
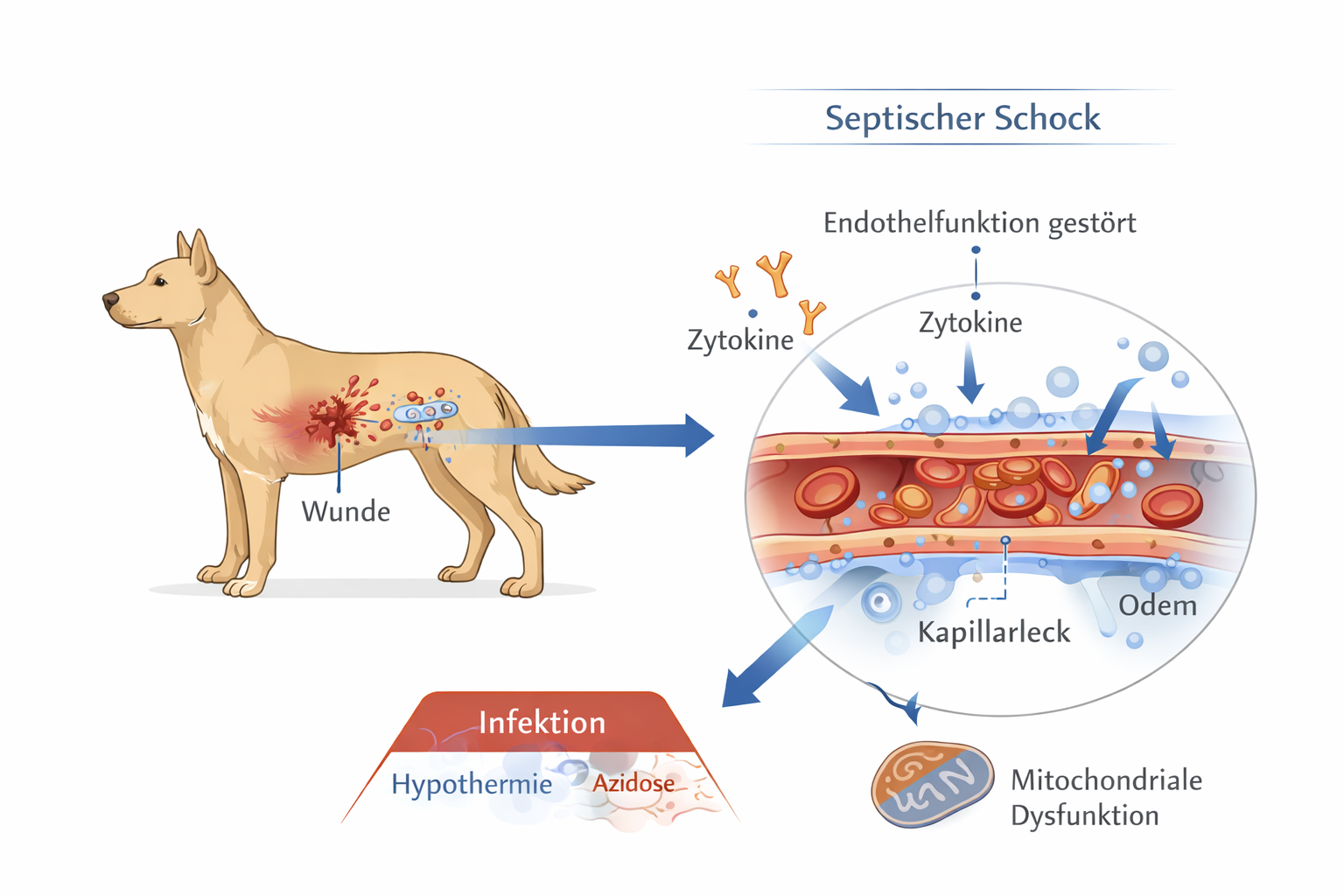
Septischer Schock: Beim septischen Schock liegt eine systemische Infektion mit dysregulierter Immunantwort zugrunde. Pathogenassoziierte Muster (PAMPs) und körpereigene Gefahrensignale (DAMPs) aktivieren über Toll-like-Rezeptoren und andere Sensoren eine Zytokin- und Komplementkaskade. Das Endothel verliert dabei seine Barrierefunktion: Glykokalyx und Tight Junctions werden geschädigt, die Kapillarpermeabilität steigt (Kapillarleck), und es entsteht eine funktionelle Hypovolämie trotz möglicherweise normaler Gesamtkörperflüssigkeit. Parallel entwickelt sich eine ausgeprägte Vasoplegie, bei der die Gefäßmuskulatur auf körpereigene Katecholamine vermindert anspricht (Katecholamin-Refraktärität). Zusätzlich kommt es zu einer tiefgreifenden Störung der Mikrozirkulation: Mikrothromben, endotheliale Dysfunktion und regionale Flussumverteilungen führen zu einer Perfusionsheterogenität, bei der einzelne Kapillargebiete überperfundiert und andere vollständig ischämisch sind. Diese Konstellation erklärt, warum ein „normaler“ oder sogar hyperdynames Kreislauf (frühes, hyperdynamisches Stadium mit hohem Herzzeitvolumen und warmen Extremitäten) die Gewebeoxygenierung keineswegs garantiert. Hinzu kommt, dass die mitochondriale Sauerstoffverwertung beeinträchtigt sein kann („zytopathische Hypoxie“): Sauerstoff wird zwar geliefert, kann aber nicht mehr effizient in ATP umgewandelt werden. Das erhöht das Risiko irreversibler Zellschäden und Multiorganversagen, selbst wenn makrozirkulatorische Parameter vorübergehend günstig erscheinen.
Diagnostisch zeigen Tiere im septischen Schock häufig Tachykardie, Tachypnoe, veränderte Schleimhautfarbe und fortschreitende mentale Veränderungen. Fieber kann auftreten, ist aber nicht obligat; ebenso sind Hypothermie und eine „unangemessene“ Temperatur (kühl trotz Infektion) klinisch hochrelevant und prognostisch ungünstig. Schleimhäute können initial gerötet und feucht wirken („warm shock“), später marmoriert, grau oder blass werden („cold shock“) – insbesondere bei Katzen kann die Präsentation subtil sein, während eine rasche Dekompensation möglich bleibt. Präklinisch ist es didaktisch und operativ wichtig, bei entsprechenden Zeichen nicht nur „Schock“ zu erkennen, sondern die Ursache zu antizipieren: Bissverletzungen mit Abszessbildung, Pyometra, gastrointestinale Perforation, Aspiration, schwere Parodontitis, Harnwegsinfektion im Kontext einer Obstruktion oder andere septische Herde müssen als Auslöser mitgedacht werden, weil sie die Wahl des Transportziels und die Dringlichkeit der Voranmeldung bestimmen.
Ein entscheidendes Merkmal des distributiven Schocks ist seine häufig kombinierte Pathophysiologie. In der klinischen Realität handelt es sich selten um „reine“ Vasodilatation. Vielmehr treffen mehrere Komponenten zusammen: (1) relative Hypovolämie durch Vasodilatation und Pooling, (2) absolute Hypovolämie durch Kapillarleck und Flüssigkeitsverlust ins Interstitium, (3) inflammationsbedingte Myokarddepression mit reduziertem Schlagvolumen und (4) mikroangiopathische Störungen mit Gerinnungsaktivierung und Mikothromben. Diese Kombination führt zu wechselnden klinischen Stadien, die von „warm und tachykard“ bis „kalt, marmoriert und hypotensiv“ reichen können. Deshalb ist die präklinische Versorgung nicht auf eine Einzelmaßnahme reduzierbar, sondern muss als Bündel verstanden werden, das parallel Vitalfunktionen sichert, sekundäre Schäden begrenzt und die definitive Therapie vorbereitet.
Präklinisch bleibt das ABCDE-Vorgehen die Leitstruktur: Atemweg beurteilen und sichern, Oxygenierung optimieren, Kreislaufzeichen engmaschig bewerten, neurologischen Status einschätzen und eine vollständige, aber zielgerichtete Exposition durchführen, ohne Wärmeverlust zu provozieren. Der Wärmeerhalt ist beim distributiven Schock besonders bedeutsam, da Hypothermie die Kreislaufkompensation, die Gerinnungsfähigkeit und die Wirksamkeit von Medikamenten beeinträchtigen kann. Schon geringe Auskühlung verschlechtert die Prognose, insbesondere bei septischen Patienten mit Kapillarleck und eingeschränkter Thermoregulation. Praktisch bedeutet das: konsequente Isolierung vom Boden, Abdeckung, Minimierung unnötiger Manipulationen, und frühzeitiger, priorisierter Transport.
Die präklinische Diagnostik zielt auf rasche Risikoabschätzung, nicht auf endgültige Ursachenklärung. Die Aussagekraft steigt erheblich, wenn relevante Zeichen wiederholt erhoben und als Trends dokumentiert werden. Schleimhautfarbe, Feuchtigkeit, Rekapillarisierungszeit, Pulsqualität, Atemarbeit, Temperatur und mentale Lage bilden in Kombination ein robustes Bild des Perfusionszustands. Einzelwerte – etwa eine einmalige Blutdruckmessung – können beim distributiven Schock irreführend sein, da Vasoplegie und Messartefakte die Interpretation erschweren. Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verschieben, ohne dass die zugrunde liegende Perfusionsstörung aufgehoben wäre. Ein klinisch scheinbar stabiler Zustand kann daher eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert.
Für den Teamerfolg ist eine saubere Begrifflichkeit zentral. Ursache (Verdacht auf Anaphylaxie vs. Sepsis), Schockform, Schockstadium, Hauptbedrohung (Atemweg vs. Perfusion) sowie Prioritäten und Transportziel müssen klar benannt werden. Strukturierte Kommunikation mit der Zielklinik ist essenziell, um definitive Therapie ohne Verzögerung zu ermöglichen: bei Sepsis z. B. frühzeitige Antibiotikagabe, chirurgische Herdsanierung, Vasopressoren und Intensivmonitoring; bei Anaphylaxie ggf. Atemwegsmanagement, antiinflammatorische und antiallergische Therapie sowie enges Kreislaufmonitoring. Die Voranmeldung sollte daher nicht nur „Schock“ melden, sondern Verdachtsdiagnose, Verlauf, Trends und bereits durchgeführte Maßnahmen in kompakter Form übermitteln. Ziel der präklinischen Phase ist, Vitalfunktionen zu sichern, Wärmeverlust zu vermeiden, den Transport zu priorisieren und die Übergabe so vorzubereiten, dass die Klinik nahtlos weiterbehandeln kann.
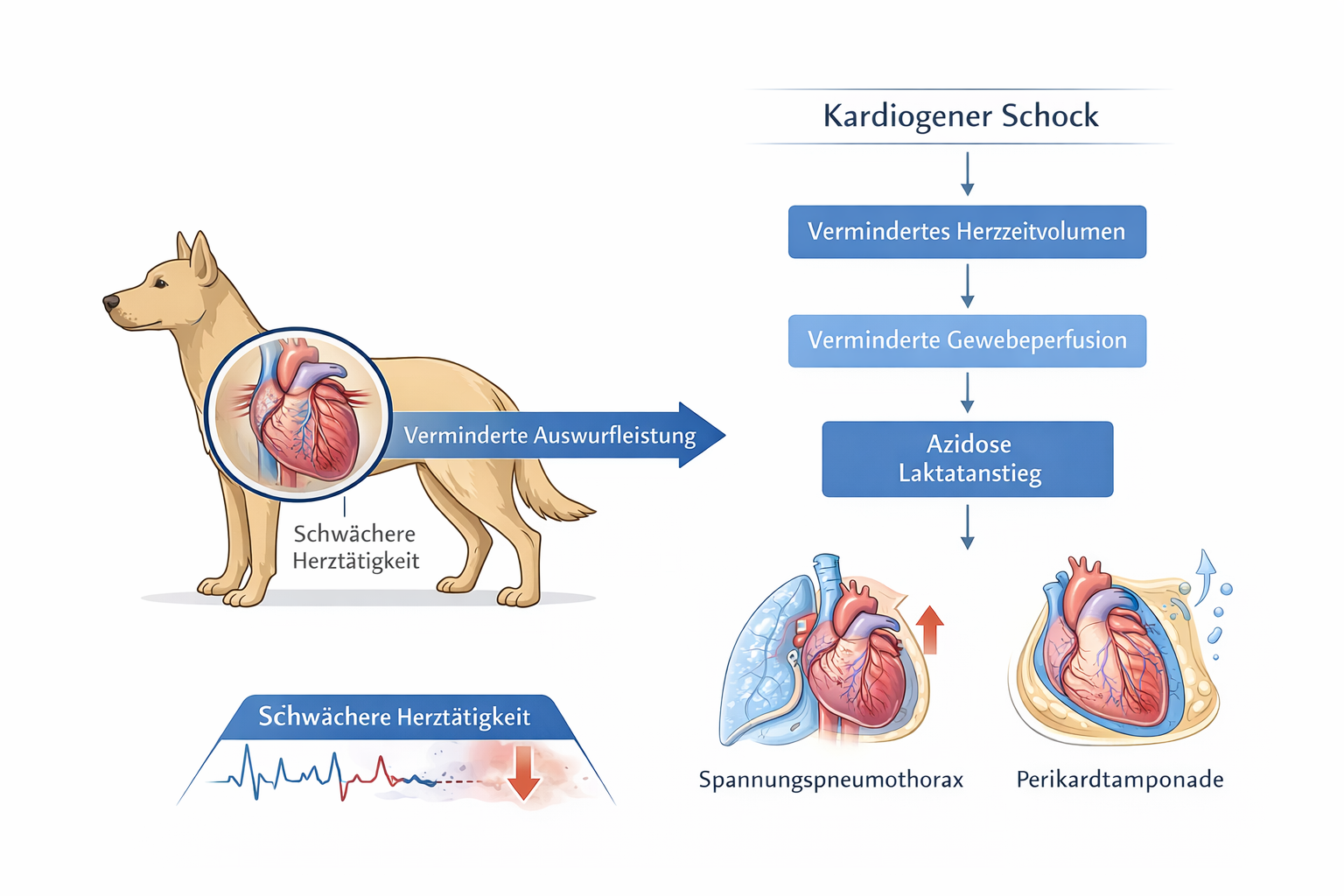
Kardiogener und obstruktiver Schock unterscheiden sich in ihrer Pathophysiologie grundlegend von hypovolämischen oder distributiven Formen. Das primäre Problem liegt weder im absoluten Volumenmangel noch im Gefäßtonus, sondern in der unzureichenden Pumpleistung des Herzens oder in einer mechanischen Behinderung der kardialen Füllung beziehungsweise des Auswurfs. In beiden Fällen resultiert ein vermindertes Herzzeitvolumen mit konsekutiver Reduktion des effektiven Sauerstoffangebotes an die Gewebe. Für die präklinische Einschätzung ist entscheidend, die mechanische Logik zu verstehen: Wenn das Herz nicht ausreichend pumpen kann oder sich nicht ausreichend füllen darf, wird eine rein volumenorientierte Therapie wirkungslos oder sogar schädlich.
Kardiogener Schock: Beim kardiogenen Schock ist die myokardiale Kontraktilität oder das rhythmische Pumpmuster so beeinträchtigt, dass das Herzzeitvolumen nicht mehr ausreicht, um eine adäquate Organperfusion sicherzustellen. Ursachen können schwere Tachyarrhythmien (z. B. ventrikuläre Tachykardie), hochgradige Bradyarrhythmien (z. B. AV-Block III°), akute Myokarditis, dekompensierte dilatative oder hypertrophe Kardiomyopathie sowie akute Klappeninsuffizienzen sein. Pathophysiologisch führt die reduzierte Schlagleistung zu einem Rückstau im venösen System und zu einer Minderdurchblutung peripherer Organe. Klinisch zeigen sich häufig schwache Pulse, verlängerte Rekapillarisierungszeit, kalte Extremitäten und Zeichen der Hypoperfusion. Gleichzeitig können pulmonale Stauungszeichen wie Dyspnoe, Tachypnoe oder Rasselgeräusche bei Lungenödem auftreten.
Ein zentrales klinisches Problem besteht darin, dass aggressive Volumengaben bei kardiogenem Schock die Situation verschlechtern können. Durch die eingeschränkte Pumpfunktion steigt der hydrostatische Druck im Lungenkreislauf, was die Entwicklung oder Progression eines Lungenödems begünstigt. Die Folge sind zunehmende Dyspnoe und Hypoxämie, die wiederum die Myokardfunktion weiter beeinträchtigen. Präklinisch bedeutet dies, dass eine Volumentherapie nur mit großer Zurückhaltung erfolgen darf und die Priorität auf Oxygenierung, Stressreduktion und raschem Transport liegt. Jede Manipulation muss so schonend wie möglich erfolgen, da Stress und Katecholaminanstieg Arrhythmien verstärken können.
Obstruktiver Schock: Der obstruktive Schock entsteht durch eine mechanische Behinderung des venösen Rückstroms oder des kardialen Auswurfs. Klassische Ursachen sind der Spannungspneumothorax, die Perikardtamponade oder – seltener präklinisch diagnostizierbar – die massive Lungenembolie. Beim Spannungspneumothorax erhöht sich der intrathorakale Druck so stark, dass große Venen komprimiert werden. Die Vorlast sinkt abrupt, das Herzzeitvolumen fällt ab, und es entwickelt sich rasch eine Kreislaufinstabilität. Klinisch zeigen sich akute Dyspnoe, reduzierte Thoraxexkursion, häufig einseitig abgeschwächte oder fehlende Atemgeräusche sowie Tachykardie und Hypotonie. Zyanose und Agitation können hinzukommen.
Die Perikardtamponade beruht auf einer Flüssigkeitsansammlung im Herzbeutel, die die diastolische Füllung mechanisch behindert. Auch hier sinkt die Vorlast trotz unverändertem Gesamtvolumen. Typische Zeichen können gedämpfte Herztöne, schwache Pulse und eventuell juguläre Stauung sein, wobei diese Befunde beim Tier oft subtil oder schwer zu interpretieren sind. Eine massive Lungenembolie blockiert den pulmonalen Kreislauf, erhöht die rechtsventrikuläre Nachlast und führt sekundär zu einem Abfall des linksventrikulären Auswurfs. Die Differenzierung dieser Ursachen ist präklinisch oft nicht sicher möglich; entscheidend ist das Erkennen der mechanischen Problematik und die Priorisierung des Transports.
Didaktisch zentral ist das Verständnis, dass „mehr Druck“ oder „mehr Volumen“ bei mechanischer Obstruktion nicht die Ursache beseitigt. Wenn Blut nicht zum Herzen zurückkehren kann oder das Herz sich nicht füllen darf, muss die Obstruktion entlastet werden. Eine Notfallentlastung bei Spannungspneumothorax ist eine fortgeschrittene Maßnahme und darf nur bei entsprechender Ausbildung und Ausrüstung durchgeführt werden. In allen anderen Fällen stehen Sauerstoffgabe, stressarme Lagerung, Minimierung von Manipulationen und schnellstmöglicher Transport in eine geeignete Einrichtung im Vordergrund.
Mischformen sind insbesondere im Trauma häufig. Ein Tier kann gleichzeitig einen hypovolämischen Schock durch Blutverlust, einen obstruktiven Schock durch Pneumothorax und eine distributive Komponente infolge inflammatorischer Reaktion entwickeln. Daher ist die wiederholte strukturierte Reevaluation wichtiger als das Festhalten an einer einmal gestellten Schockform-Hypothese. Jede Verschlechterung von Atemarbeit, Pulsqualität oder mentaler Lage muss als Hinweis auf eine dynamische Veränderung interpretiert werden.
Für die präklinische Einschätzung bleibt die Integration aller Befunde entscheidend. Die Unterscheidung zwischen Makrozirkulation (Blutdruck, Puls, Herzzeitvolumen) und Mikrozirkulation (Kapillardurchfluss, Sauerstoffextraktion, Endothelfunktion) hilft, Fehleinschätzungen zu vermeiden. Schleimhautfarbe, Feuchtigkeit und Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Perfusionsqualität. Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verändern, ohne dass die zugrunde liegende Perfusionsstörung behoben wäre. Ein scheinbar stabiler Zustand kann eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert.
Wärmeerhalt ist auch bei kardiogenem und obstruktivem Schock integraler Bestandteil der Versorgung. Hypothermie verschlechtert die Myokardfunktion, beeinflusst die Gerinnung und kann Arrhythmien begünstigen. Schonende Lagerung, Minimierung von Stress und eine ruhige Umgebung sind insbesondere bei kardial vorbelasteten Tieren essenziell. Jede unnötige Manipulation kann die hämodynamische Situation destabilisieren.
Eine präzise Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. Pneumothorax, HCM-Dekompensation), Schockform (kardiogen oder obstruktiv), Stadium, Prioritäten (Atemweg, Oxygenierung, Entlastung, Transport) und Transportziel müssen klar benannt werden. Die Aussagekraft steigt erheblich, wenn Befunde wiederholt erhoben und Trends dokumentiert werden. Einzelwerte dürfen nicht isoliert interpretiert werden, sondern müssen im Kontext des Gesamtbildes stehen.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Präklinisch bedeutet dies, die Ursache zu antizipieren, sekundäre Schäden zu vermeiden und den Patienten rasch einer Einrichtung zuzuführen, die definitive diagnostische und therapeutische Maßnahmen durchführen kann. Die Qualität der Versorgung bemisst sich dabei an der strukturierten Reevaluation, der klaren Kommunikation und der konsequenten Priorisierung lebensrettender Schritte.
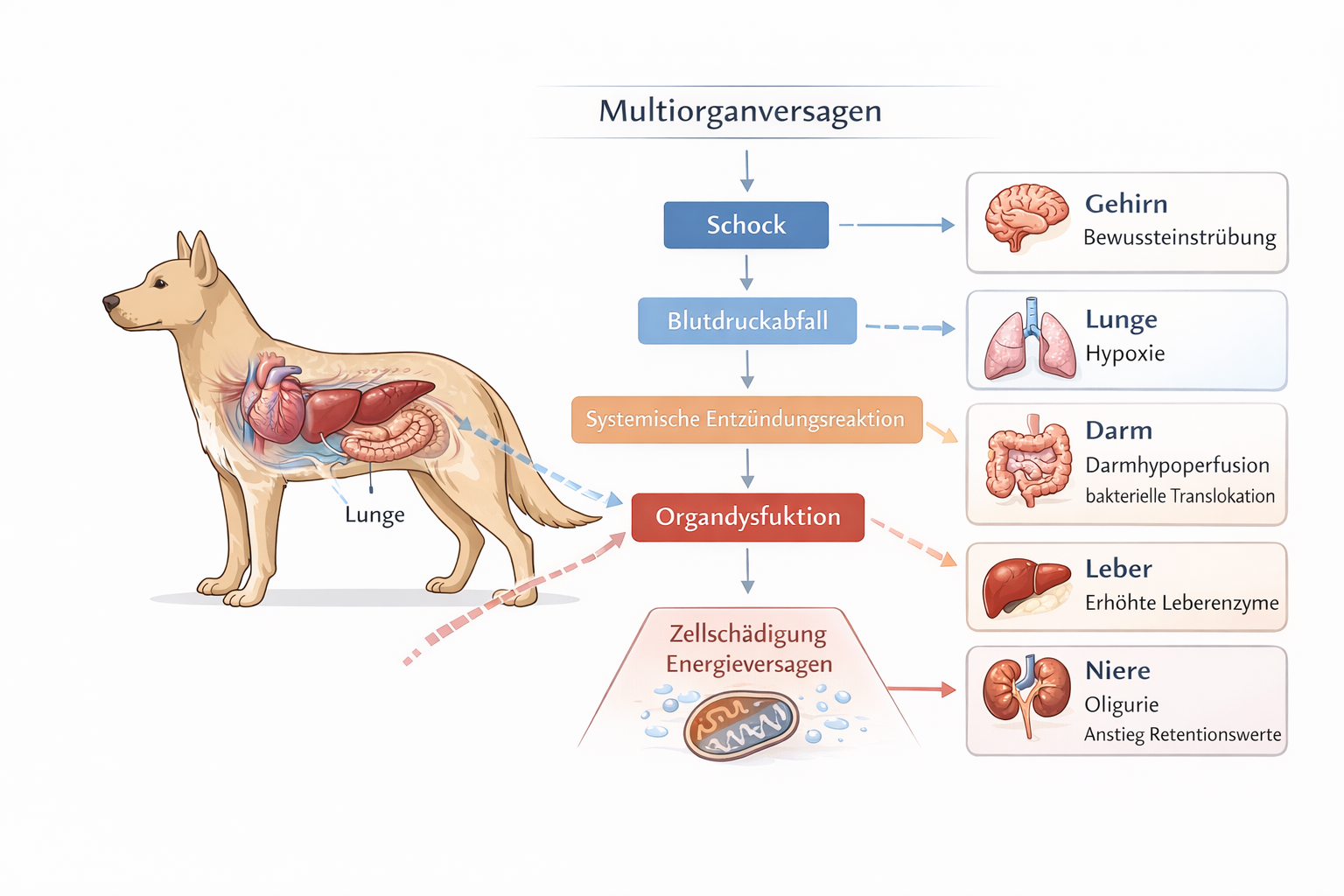
Ziel: Progression in die irreversible Phase verhindern durch frühe Stabilisierung.
Das Multiorganversagen (Multiple Organ Dysfunction Syndrome, MODS) stellt die Endstrecke eines anhaltenden oder wiederkehrenden Schockgeschehens dar und ist Ausdruck einer fortschreitenden systemischen Dysregulation. Es entsteht nicht abrupt, sondern entwickelt sich als dynamischer Prozess infolge kombinierter Hypoperfusion, inflammatorischer Fehlsteuerung, endothelialer Schädigung und zellulärem Energiemangel. Pathophysiologisch ist MODS das Resultat eines Missverhältnisses zwischen Sauerstoffangebot und -verwertung, das über einen kritischen Zeitraum persistiert. Jede Episode von Hypotonie, Hypoxie, Hypothermie oder unkontrollierter Blutung erhöht die Wahrscheinlichkeit, dass kompensatorische Mechanismen erschöpfen und Organsysteme in eine funktionelle Dekompensation übergehen.
Frühe Organfunktionsstörungen sind häufig subtil und werden leicht übersehen. Die Niere reagiert besonders empfindlich auf Durchblutungsmangel. Bereits kurze Phasen reduzierter Perfusion können eine akute Nierenfunktionsstörung initiieren. Klinisch zeigt sich zunächst eine abnehmende Harnproduktion (Oligurie), die präklinisch nur indirekt über Anamnese (kein Urinabsatz), trockene Schleimhäute oder Zeichen der Dehydratation erfasst werden kann. Persistiert die Minderperfusion, droht ein akutes Nierenversagen mit Elektrolytverschiebungen und metabolischer Entgleisung.
Die Leber verliert bei anhaltender Hypoperfusion ihre zentrale Rolle in Entgiftung, Metabolismus und Synthese. Gerinnungsfaktoren werden vermindert gebildet, toxische Metabolite akkumulieren, und die Glukosehomöostase kann gestört sein. In Kombination mit systemischer Inflammation entsteht eine komplexe Koagulopathie, die sowohl Blutungsneigung als auch Mikrothrombenbildung begünstigt. Diese Mikrothromben verschlechtern wiederum die Mikrozirkulation und verstärken die Organischämie.
Die Lunge ist durch ihre ausgedehnte Kapillaroberfläche besonders anfällig für endotheliale Schädigung. Kapillarleck und inflammatorische Prozesse führen zu einem ARDS-ähnlichen Bild mit interstitieller und alveolärer Flüssigkeitsansammlung. Der Gasaustausch wird zunehmend ineffektiv. Klinisch manifestiert sich dies durch Tachypnoe, steigenden Sauerstoffbedarf, Dyspnoe und im Spätstadium Zyanose. Selbst bei scheinbar stabilen Blutdruckwerten kann die Sauerstoffversorgung der Gewebe kritisch reduziert sein.
Das zentrale Nervensystem reagiert sensibel auf globale Perfusionsveränderungen. Frühe Zeichen sind Unruhe, Desorientierung oder veränderte Reaktionslage. Im weiteren Verlauf folgen Apathie, reduzierte Bewusstseinslage bis hin zum Koma. Diese neurologischen Veränderungen sind häufig ein Spiegel der globalen zerebralen Perfusion und sollten als Warnsignal für eine systemische Verschlechterung verstanden werden.
Eine Schlüsselrolle im Prozess des MODS spielt das Endothel. Die Schädigung der endothelialen Glykokalyx führt zu erhöhter Gefäßpermeabilität, interstitieller Flüssigkeitsverschiebung und Verlust der Barrierefunktion. Gleichzeitig entsteht eine prokoagulatorische Oberfläche, die Mikrothromben begünstigt und die Perfusionsheterogenität verstärkt. Selbst wenn makrozirkulatorische Parameter – etwa Blutdruck oder Herzfrequenz – vorübergehend normal erscheinen, kann die Mikrozirkulation weiterhin gestört bleiben. Hinzu kommt eine mögliche mitochondriale Dysfunktion: Trotz ausreichender Sauerstofflieferung gelingt die ATP-Produktion nicht mehr effizient („zytopathische Hypoxie“). Dadurch persistiert die Organfunktionsstörung auch nach scheinbarer Kreislaufstabilisierung.
Didaktisch ist entscheidend, MODS als Prozess zu verstehen, nicht als singuläres Ereignis. Jede Phase unzureichender Perfusion erhöht das Risiko irreversibler Zellschäden. Zeitmanagement wird damit selbst zur medizinischen Intervention. Rasche, strukturierte Entscheidungen und frühzeitige Übergabe in eine intensivmedizinisch ausgestattete Einrichtung sind pathophysiologisch begründet. Je länger Hypoperfusion und Inflammation unkontrolliert bestehen, desto geringer wird die Reversibilität.
Für die Präklinik ergeben sich daraus klare Prinzipien: Schock frühzeitig erkennen, Oxygenierung konsequent sichern, Wärmeerhalt gewährleisten und zusätzliche Stressoren vermeiden. Hypothermie verschlechtert Gerinnung, Myokardfunktion und Medikamentenwirkung und begünstigt die Progression zum Multiorganversagen. Ebenso muss jede vermeidbare Verzögerung minimiert werden. Eine strukturierte Reevaluation entlang eines festen Schemas reduziert das Risiko, kritische Veränderungen zu übersehen.
Die Unterscheidung zwischen Makro- und Mikrozirkulation bleibt auch im Kontext von MODS zentral. Ein „normaler“ Blutdruck bedeutet nicht zwangsläufig adäquate Gewebeoxygenierung. Schleimhautfarbe, Feuchtigkeit und Rekapillarisierungszeit liefern unmittelbare Hinweise auf die Perfusionsqualität und den sympathischen Tonus. Die Aussagekraft steigt erheblich, wenn diese Zeichen wiederholt erhoben und im Verlauf dokumentiert werden. Trendbeobachtungen sind aussagekräftiger als isolierte Einzelmessungen.
Gerade bei Hund und Katze können Stress, Schmerz und Hypoxie Vitalparameter verändern, ohne die zugrunde liegende Perfusionsstörung zu beheben. Ein klinisch scheinbar stabiler Zustand kann daher eine fragile Kompensation darstellen, die unter zusätzlicher Belastung abrupt kollabiert. Die präklinische Einschätzung erfordert stets die Integration aller Befunde in ein konsistentes Gesamtbild. Einzelwerte dürfen nicht isoliert interpretiert werden.
Eine klare Begrifflichkeit erleichtert die Teamkommunikation: Ursache (z. B. Trauma, Sepsis), Schockform, Stadium, betroffene Organsysteme, Prioritäten und Transportziel müssen eindeutig benannt werden. Jede Intervention wird mit einer Reevaluation verknüpft: Verbessern sich mentale Lage, Atemarbeit oder Perfusionszeichen? Bleiben kritische Parameter bestehen? Diese strukturierte Vorgehensweise erhöht die Handlungssicherheit und unterstützt die klinische Kontinuität.
Physiologisch betrachtet ist jede erfolgreiche Schocktherapie der Versuch, Sauerstoffangebot, Sauerstofftransport und Sauerstoffverwertung wieder in ein Gleichgewicht zu bringen. Wird dieses Gleichgewicht nicht rechtzeitig wiederhergestellt, entwickelt sich aus der zunächst reversiblen Organdysfunktion ein irreversibles Multiorganversagen. Die präklinische Phase ist daher ein entscheidender Zeitabschnitt, in dem durch konsequente Stabilisierung, Wärmeschutz, Oxygenierung und priorisierten Transport die Weichen für Prognose und Überleben gestellt werden.
Merksatz: „Intervention ohne Reevaluation“ ist unvollständig.
Präklinische Entscheidungslogik im Schockmanagement bedeutet, unter Zeitdruck und in einer hochdynamischen Lage innerhalb weniger Minuten belastbare Prioritäten zu setzen. Ziel ist nicht, vor Ort eine vollständige Diagnose zu „lösen“, sondern lebensbedrohliche Störungen früh zu erkennen, zu überbrücken und den Patienten so rasch wie möglich in eine geeignete Einrichtung zu überführen. In der Tiernotfallmedizin ist diese Logik besonders wichtig, weil Stress, Schmerz und Umgebungseinflüsse Vitalparameter verfälschen können und weil Schockzustände häufig anfangs kompensiert erscheinen. Der Rahmen für dieses Vorgehen ist das ABCDE-Schema, angepasst an die tiermedizinischen Besonderheiten und konsequent als zyklisches Arbeitsmodell verstanden: beurteilen – intervenieren – erneut beurteilen.
A – Airway (Atemweg): Im ersten Schritt wird geprüft, ob der Atemweg frei und funktionell ist. Dazu gehört die Beurteilung von Schutzreflexen (Schlucken, Husten), das Risiko einer Aspiration sowie mögliche Obstruktionen durch Blut, Erbrochenes, Fremdkörper, Schwellungen oder Zungenlage. Tierartspezifisch relevant sind zudem Maulkorb- und Fixationsprobleme: Sicherungsmaßnahmen dürfen die Ventilation nicht behindern. Die Entscheidungslogik lautet hier: Ein unsicherer Atemweg gefährdet alle nachfolgenden Schritte, weil Hypoxie binnen kurzer Zeit zu Kreislaufkollaps und neurologischem Schaden führt. Deshalb hat die Sicherung eines freien Atemwegs Vorrang vor detaillierten Messungen oder Dokumentationsaufgaben.
B – Breathing (Atmung): Atmung wird nicht nur als Frequenz bewertet, sondern als Atemarbeit und Effektivität. Entscheidend sind Thoraxexkursion, Atemtiefe, Einsatz der Bauchpresse, Atemgeräusche (Stridor, rasselnde Geräusche), Hecheln außerhalb thermoregulatorischer Situationen, Zyanose und Zeichen von Luftnot. Bei Trauma muss früh an thorakale Ursachen gedacht werden (Pneumothorax, Hämatothorax, Lungenkontusion, Rippenverletzungen). Die präklinische Logik lautet: Eine „passable“ Kreislaufsituation nützt nichts, wenn die Ventilation mechanisch oder funktionell versagt. Daher darf bei akuter Dyspnoe der Fokus nicht ausschließlich auf Kreislaufzahlen liegen; Atemmechanik und Oxygenierung sind dann die zeitkritischen Determinanten.
C – Circulation (Kreislauf): Im Schockmanagement ist die Kreislaufbeurteilung primär eine Perfusionsbeurteilung. Pulsqualität (kräftig vs. fadenförmig), Pulsfrequenz, Schleimhautfarbe und -feuchtigkeit, Rekapillarisierungszeit (CRT), Temperatur der Extremitäten sowie offensichtliche Blutungsquellen stehen im Vordergrund. Hypotonie ist häufig ein Spätzeichen; frühere Hinweise sind Tachykardie, verlängerte CRT, blasse/graue Schleimhäute und kalte Akren. Gleichzeitig sind bei distributiven Zuständen auch gerötete Schleimhäute und „bounding pulses“ möglich. Die Entscheidungslogik lautet deshalb: Makrozirkulation (Druck, Puls) und Mikrozirkulation (Kapillarfluss, Sauerstoffextraktion) müssen gemeinsam bewertet werden. Ein einzelner Messwert – etwa ein scheinbar akzeptabler systolischer Blutdruck – schließt eine kritische Mikrozirkulationsstörung nicht aus. Sichtbare Blutungen werden sofort kontrolliert, weil Blutungskontrolle eine ursachennahe, lebensrettende Intervention ist. Bei Verdacht auf innere Blutung gilt: „Time to surgery“ ist prognoseentscheidend; die präklinische Phase muss Transportfähigkeit herstellen, nicht Diagnostik verlängern.
D – Disability (Neurologischer Status): Hier wird die Bewusstseinslage (wach, stuporös, komatös), die Reaktionsfähigkeit, das Schmerzverhalten und das Vorliegen von Krampfaktivität beurteilt. Neurologische Veränderungen sind häufig ein Spiegel globaler Perfusion und Oxygenierung. Die Entscheidungslogik lautet: Eine Verschlechterung des Bewusstseins ist ein Alarmzeichen, das die Prioritäten unmittelbar beeinflusst (z. B. erneute Prüfung von A/B, Intensivierung der Oxygenierung, beschleunigter Transport). Bei klinischem Verdacht auf Hypoglykämie kann eine Messung – sofern verfügbar – entscheidend sein; gleichzeitig darf sie nicht dazu führen, dass A/B/C verzögert werden. Schmerzmanagement ist präklinisch stets sorgfältig abzuwägen und an die vorhandene Qualifikation gebunden; unabhängig davon gilt: stressarme Handhabung reduziert Katecholaminbelastung und damit sekundäre Verschlechterungen.
E – Exposure/Environment (Exposition und Umgebung): Abschließend wird der Patient so weit entkleidet/inspektiert, dass relevante Verletzungen nicht übersehen werden, ohne unnötig Wärme zu verlieren. Gleichzeitig werden Umgebungsfaktoren aktiv gemanagt: Hypothermieprophylaxe, Schutz vor Nässe/Kälte, stabile Lagerung, Minimierung von Stressoren und sichere Transportvorbereitung. Die Entscheidungslogik lautet: Hypothermie ist keine „Nebenvariable“, sondern ein Treiber von Koagulopathie und Kreislaufversagen. Wärmeerhalt ist daher eine Therapie, nicht Komfortmaßnahme. Gerade im Schock ist Wärmeverlust schnell und prognostisch relevant.
Ein zentraler Grundsatz der präklinischen Entscheidungslogik ist die Einsicht, dass Schock in der Praxis selten „rein“ auftritt. Ein Trauma kann gleichzeitig hypovolämisch wirken (Blutung), obstruktiv (Pneumothorax/Thoraxdruck), distributiv (inflammatorische Antwort) und sekundär sogar kardiogen (Myokarddepression, Arrhythmien) werden. Die Konsequenz ist ein zyklisches Vorgehen: Nach jeder Intervention werden die Kernparameter erneut geprüft, um eine Trendbeurteilung zu ermöglichen. Damit wird der Fokus von der Momentaufnahme auf die Dynamik verschoben. Praktisch bedeutet das: Nach Sauerstoffgabe wird Atemarbeit und Schleimhautfarbe erneut bewertet; nach Wärmeschutz werden periphere Temperatur und mentale Lage kontrolliert; nach Druckverband werden Pulsqualität und CRT überprüft. Dieses „Intervention–Reevaluation“-Prinzip ist die wichtigste Sicherheitsbarriere gegen Fehleinschätzungen.
Didaktisch hilfreich ist die klare Trennung zwischen Erkennen und definitiv Behandeln. Präklinisch werden lebensbedrohliche Zustände überbrückt: Atemweg sichern, Oxygenierung optimieren, Blutung kontrollieren, Hypothermie verhindern, patientenschonend lagern und Transport organisieren. Definitive Diagnostik und kausale Therapie (Bildgebung, OP, Antibiotikaregime, Vasopressoren, Intensivmonitoring) liegen in der Regel in der Klinik. Diese Trennung schützt vor dem häufigsten Fehler im Schockmanagement: dem „Diagnostik-Sog“, bei dem vor Ort Zeit in Detailabklärungen investiert wird, ohne dass dadurch eine definitive Maßnahme möglich wird. Präklinische Exzellenz ist daher die Fähigkeit, diagnostische Hypothesen so weit zu formulieren, dass die richtige Klinik vorbereitet werden kann – nicht, die Hypothese vor Ort endgültig zu bestätigen.
Kommunikation ist im Schockmanagement ein medizinischer Bestandteil. Eine Voranmeldung an die Zielklinik ist besonders wertvoll, wenn sie strukturiert erfolgt und nicht nur „Schock“ als Etikett meldet. Relevant sind: Verdacht auf Schockform (hypovolämisch/distributiv/obstruktiv/kardiogen), Stadium (kompensiert vs. dekompensiert), wahrscheinliche Ursache (Trauma, Blutung, Sepsis, Anaphylaxie, kardiale Dekompensation), aktuelle klinische Schlüsselbefunde (Atemarbeit, Schleimhautfarbe, CRT, Pulsqualität, Temperatur, mentale Lage), durchgeführte Maßnahmen und – vor allem – Trends: Wird die CRT kürzer oder länger? Wird der Puls kräftiger oder fadenförmiger? Verbessert sich die Atemarbeit unter Sauerstoff? Diese Trendkommunikation erlaubt der Klinik, Ressourcen zu mobilisieren (OP, Intensivplatz, Bildgebung, Labor, Blutprodukte) und verringert Zeitverluste an der Schnittstelle.
Auch die interne Teamkommunikation folgt der Entscheidungslogik. Rollen und Aufgaben werden früh festgelegt (Teamleitung, Airway/O₂, Blutung/Verbände, Dokumentation/Kommunikation). Kurze, eindeutige Closed-Loop-Kommunikation reduziert Missverständnisse. Die Teamleitung steuert die Prioritäten, achtet auf das zyklische Reevaluationsprinzip und verhindert, dass sich das Team in Nebenaufgaben verliert. Gleichzeitig wird eine minimale, aber konsistente Dokumentation geführt: Zeitpunkte, Befunde, Maßnahmen, Reaktionen. Diese Dokumentation ist keine Bürokratie, sondern klinische Sicherheitsreserve, weil sie die Übergabe stützt und spätere Entscheidungen an Trends anknüpfen lässt.
Die präklinische Entscheidungslogik berücksichtigt außerdem typische Fallstricke. Erstens: „Gehfähig“ oder „wach“ schließt Schock nicht aus, weil kompensatorische Mechanismen beim Tier kurzfristig sehr effektiv sein können. Zweitens: Stress und Schmerz können Tachykardie und Tachypnoe verursachen, ohne dass Perfusion ausreichend ist; umgekehrt kann scheinbare Beruhigung eine beginnende Dekompensation anzeigen. Drittens: Blutdruckmessungen sind hilfreich, aber fehleranfällig und häufig spätpathologisch; deshalb werden sie immer in den Kontext von Pulsqualität, CRT, Schleimhäuten und mentaler Lage eingeordnet. Viertens: Bei akuter Dyspnoe nach Trauma muss früh an obstruktive Ursachen gedacht werden; ein „falscher“ Fokus auf Kreislaufzahlen ohne Beachtung der Atemmechanik kostet lebensbedrohliche Minuten.
Zusammengefasst ist präklinische Qualität im Schockmanagement die Summe aus strukturiertem Denken, sauberer Beobachtung, zeitkritischer Priorisierung und klarer Kommunikation. Das ABCDE-Schema liefert die Prioritäten, die zyklische Reevaluation liefert die Sicherheit, und die konsequente Trennung von Überbrückung und definitiver Therapie verhindert Verzögerungen. Wer diese Logik beherrscht, schafft die entscheidende Brücke zwischen Einsatzort und Klinik: Der Patient wird nicht „diagnostiziert“, sondern stabilisiert, richtig zugeordnet und ohne Zeitverlust in definitive Versorgung überführt.
Hinweis: Single-Choice (jeweils eine richtige Antwort). Bestehensgrenze: 70%.
Ziel: in kurzer Zeit korrekte Prioritäten setzen. Die Simulation bewertet Kernentscheidungen (Oxygenierung, Blutungskontrolle, Wärmeschutz, Transport).
Merksatz: „Transport ist Therapie“, wenn definitive Maßnahmen nur in der Klinik möglich sind.